ثوريوم
 | |||||||||||||||
| Thorium | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| المظهر | فضي | ||||||||||||||
| الوزن الذري العياري Ar°(Th) | |||||||||||||||
| Thorium في الجدول الدوري | |||||||||||||||
| |||||||||||||||
| الرقم الذري (Z) | 90 | ||||||||||||||
| المجموعة | n/a | ||||||||||||||
| الدورة | period 7 | ||||||||||||||
| المستوى الفرعي | f-block | ||||||||||||||
| التوزيع الإلكتروني | [Rn] 6d2 7s2 | ||||||||||||||
| الإلكترونات بالغلاف | 2, 8, 18, 32, 18, 10, 2 | ||||||||||||||
| الخصائص الطبيعية | |||||||||||||||
| الطور at د.ح.ض.ق | solid | ||||||||||||||
| نقطة الانصهار | 2023 K (1750 °س، 3182 °F) | ||||||||||||||
| نقطة الغليان | 5061 K (4788 °س، 8650 °ف) | ||||||||||||||
| حرارة الانصهار | 13.81 kJ/mol | ||||||||||||||
| حرارة التبخر | 514 kJ/mol | ||||||||||||||
| السعة الحرارية المولية | 26.230 J/(mol·K) | ||||||||||||||
ضغط البخار
| |||||||||||||||
| الخصائص الذرية | |||||||||||||||
| الكهرسلبية | مقياس پاولنگ: 1.3 | ||||||||||||||
| طاقات التأين |
| ||||||||||||||
| نصف القطر الذري | empirical: 179.8 pm | ||||||||||||||
| نصف قطر التكافؤ | 206±6 pm | ||||||||||||||
| خصائص أخرى | |||||||||||||||
| البنية البلورية | face-centred cubic (fcc) | ||||||||||||||
| سرعة الصوت قضيب رفيع | 2490 م/ث (عند 20 °س) | ||||||||||||||
| قضيب رفيع | 54.0 W/(m·K) | ||||||||||||||
| التمدد الحراري | 11.0 µm/(m⋅K) (عند 25 °س) | ||||||||||||||
| المقاومة الكهربائية | 157 nΩ⋅m (at 0 °C) | ||||||||||||||
| الترتيب المغناطيسي | مغناطيسية مسايرة[1] | ||||||||||||||
| القابلية المغناطيسية | 132.0×10−6 cm3/mol (293 K)[2] | ||||||||||||||
| معامل يونگ | 79 GPa | ||||||||||||||
| معامل القص | 31 GPa | ||||||||||||||
| معاير الحجم | 54 GPa | ||||||||||||||
| نسبة پواسون | 0.27 | ||||||||||||||
| صلادة موز | 3.0 | ||||||||||||||
| صلادة ڤيكرز | 295–685 MPa | ||||||||||||||
| صلادة برينل | 390–1500 MPa | ||||||||||||||
| رقم كاس | 7440-29-1 | ||||||||||||||
| التاريخ | |||||||||||||||
| التسمية | على اسم ثور، الإله النوردي للرعد | ||||||||||||||
| الاكتشاف | يونس ياكوب برزليوس (1829) | ||||||||||||||
| نظائر الThorium | |||||||||||||||
| قالب:جدول نظائر Thorium غير موجود | |||||||||||||||
الثوريوم (thorium)، هو أحد عناصر الجدول الدوري وله الرمز Th، وعدده الذري 90. ونظراً لأنه فلز له نشاط إشعاعي طفيف، ويوجد بصورة طبيعية فإنه يعتبر من أنواع الوقود النووي البديلة لليورانيوم. الثوريوم فضي فاتح، ويتغير لونه إلى الرمادي الزيتوني عند تعرضه للهواء، مكوناً ثاني أكسيد الثوريوم؛ وهو لين نسبياً ومطيلي، ونقطة انصهاره عالية. الثوريوم هو أكتينيد موجب الشحنة، تهيمن على تركيبه الكيميائي حالة الأكسدة +4؛ وهو شديد التفاعل، ويمكن أن يشتعل في الهواء عند انقسامه بدقة.
جميع نظائر الثوريوم المعروفة غير مستقرة. أكثرها استقراراً، وهو الثوريوم-232، يبلغ عمر النصفي 14.05 بليون سنة، أي ما يعادل تقريباً عمر الكون؛ وهو يتحلل ببطء شديد عبر انحلال ألفا، بادئاً سلسلة انحلال تُسمى سلسلة الثوريوم، وتنتهي عند نظير الرصاص المستقر 208. على الأرض، الثوريوم واليورانيوم هما العنصران الوحيدان المشعان بشكل كبير واللذان لا يزالان موجودين بشكل طبيعي بكميات كبيرة العناصر الأزلية. [أ] يُقدر أن الثوريوم أكثر وفرة في الطبيعة بثلاث مرات من اليورانيوم في قشرة الأرض، ويُعدن بشكل أساسي من رمال المونازيت كمنتج ثانوي لاستخراج الفلزات الأرضية النادرة.
اكتُشف الثوريوم عام 1828 على يد عالم المعادن النرويجي الهاوي مورتن ثرين إسمارك، وحدده الكيميائي السويدي يونس ياكوب برزليوس، الذي أطلق عليه اسم ثور، إله الرعد النوردي. طُوّرت تطبيقاته الأولى في أواخر القرن التاسع عشر. حظي النشاط الإشعاعي للثوريوم باعتراف واسع النطاق خلال العقود الأولى من القرن العشرين. في النصف الثاني من القرن، استُبدل الثوريوم في العديد من الاستخدامات بسبب المخاوف المتعلقة بنشاطه الإشعاعي.
لا يزال الثوريوم يُستخدم كعنصر سبائك في أقطاب لحام TIG، لكنه يُستبدل تدريجياً بتركيبات مختلفة. كما استُخدم أيضاً في البصريات المتطورة والأجهزة العلمية، وفي بعض الصمامات المفرغة للبث، وكمصدر للضوء في الوشاح الغازي، إلا أن هذه الاستخدامات أصبحت هامشية. اقتُرح استخدامه كبديل لليورانيوم كوقود نووي في المفاعلات النووية، وقد بُنيت العديد من مفاعلات الثوريوم. كما يُستخدم الثوريوم في تقوية المغنسيوم، وطلاء أسلاك التنگستن في المعدات الكهربائية، والتحكم في حجم حبيبات التنگستن في المصابيح الكهربائية، وفي البوتقات عالية الحرارة، وفي العدسات الزجاجية، بما في ذلك عدسات الكاميرات والأجهزة العلمية. ومن الاستخدامات الأخرى للثوريوم: السيراميك المقاوم للحرارة، ومحركات الطائرات، والمصابيح المتوهجة. وقد استخدم علم المحيطات نسب نظائر الپروتكتينيوم 231/230 لفهم المحيط القديم.[4]
خصائص الحجم
Thorium is a moderately soft, paramagnetic, bright silvery radioactive actinide metal that can be bent or shaped. In the periodic table, it lies to the right of actinium, to the left of protactinium, and below cerium. Pure thorium is very ductile and, as normal for metals, can be cold-rolled, swaged, and drawn.[5] At room temperature, thorium metal has a face-centred cubic crystal structure; it has two other forms, one at high temperature (over 1360 °C; body-centred cubic) and one at high pressure (around 100 GPa; body-centred tetragonal).[5]
Thorium metal has a bulk modulus (a measure of resistance to compression of a material) of 54 GPa, about the same as tin's (58.2 GPa). Aluminium's is 75.2 GPa; copper's is 137.8 GPa; and mild steel's is 160–169 GPa.[6] Thorium is about as hard as soft steel, so when heated it can be rolled into sheets and pulled into wire.[7]
Thorium is nearly half as dense as uranium and plutonium and is harder than both.[7] Thorium has a magnetic susceptibility of 0.412 × 4π × 10−9 m3⋅kg−1 at room temperature. This susceptibility is mostly temperature-independent, however impurities and dopants can affect this value.[5] It becomes superconductive below 1.4 K.[5] Thorium's melting point of 1750 °C is above both those of actinium (1227 °C) and protactinium (1568 °C). At the start of period 7, from francium to thorium, the melting points of the elements increase (as in other periods), because the number of delocalised electrons each atom contributes increases from one in francium to four in thorium, leading to greater attraction between these electrons and the metal ions as their charge increases from one to four. After thorium, there is a new downward trend in melting points from thorium to plutonium, where the number of f-electrons increases from about 0.4 to about 6: this trend is due to the increasing hybridisation of the 5f and 6d orbitals and the formation of directional bonds resulting in more complex crystal structures and weakened metallic bonding.[7][8] (The f-electron count for thorium metal is a non-integer due to a 5f–6d overlap.)[8] Among the actinides up to californium, which can be studied in at least milligram quantities, thorium has the highest melting and boiling points and second-lowest density; only actinium is lighter. Thorium's boiling point of 4788 °C is the fifth-highest among all the elements with known boiling points.[ب]
The properties of thorium vary widely depending on the degree of impurities in the sample. The major impurity is usually thorium dioxide (ThO
2); even the purest thorium specimens usually contain about a tenth of a per cent of the dioxide.[5] Experimental measurements of its density give values between 11.5 and 11.66 g/cm3: these are slightly lower than the theoretically expected value of 11.7 g/cm3 calculated from thorium's lattice parameters, perhaps due to microscopic voids forming in the metal when it is cast.[5] These values lie between those of its neighbours actinium (10.1 g/cm3) and protactinium (15.4 g/cm3), part of a trend across the early actinides.[5]
Thorium can form alloys with many other metals. Addition of small proportions of thorium improves the mechanical strength of magnesium, and thorium–aluminium alloys have been considered as a way to store thorium in proposed future thorium nuclear reactors. Thorium forms eutectic mixtures with chromium and uranium, and it is completely miscible in both solid and liquid states with its lighter congener cerium.[5]
النظائر
جميع العناصر باستثناء عنصرين حتى البيزموث (العنصر 83) لها نظير مستقر عملياً لجميع الأغراض ("مستقر كلاسيكياً")، باستثناء التكنيشيوم والپروميثيوم (العنصرين 43 و61). جميع العناصر من الپولونيوم (العنصر 84) فصاعداً قابلة للقياس من حيث النشاط الإشعاعي. 232Th هو أحد النيوكليدين اللذين يليان البيزموت (الآخر هو 238U واللذين يبلغ عمرهما النصفي بلايين السنين؛ إذ يبلغ عمره النصفي 14.05 بليون سنة، أي ما يقارب ثلاثة أضعاف عمر الأرض، وأطول بقليل من عمر الكون. وقد نجا أربعة أخماس الثوريوم الموجود عند تكون الأرض حتى يومنا هذا.[10][11][12] 232Th هو النظير الوحيد للثوريوم الموجود بكميات كبيرة في الطبيعة.[10] ويُعزى استقراره إلى غلافه النووي المغلق الذي يحتوي على 142 نيوتروناً.[13][14] يتميز الثوريوم بتركيب نظائري أرضي مميز، مع وزن ذري يبلغ 232.0377±0.0004.[15] وهو واحد من أربعة عناصر مشعة فقط (إلى جانب البيزموث والپروتاكتينيوم واليورانيوم) التي توجد بكميات كبيرة كافية على الأرض لتحديد الوزن الذري القياسي.[citation needed]
تكون نوى الثوريوم عرضة لانحلال ألفا لأن القوة النووية القوية لا تستطيع التغلب على التنافر الكهرومغناطيسي بين پروتوناته.[16] انحلال ألفا للنظير 232Th يبدأ سلسلة انحلال 4n التي تشمل نظائر ذات عدد كتلي يقبل القسمة على 4 (ومن هنا جاء الاسم؛ وتُسمى أيضاً سلسلة الثوريوم نسبةً إلى سلفها). تبدأ هذه السلسلة من انحلالات ألفا وبيتا المتتالية بانحلال 232Th إلى 228Ra وتنتهي عند 208Pb.[10]
تحتوي أي عينة من الثوريوم أو مركباته على آثار من هذه النظائر، وهي نظائر للثاليوم، الرصاص، البيزموث، الپولونيوم، الرادون، الراديوم، والأكتينيوم.[10] يمكن تنقية عينات الثوريوم الطبيعية كيميائياً لاستخلاص النويدات الوليدة المفيدة، مثل 212Pb، والذي يستخدم في الطب النووي لعلاج السرطان.[17][18] يمكن أيضاً استخدام 227Th (باعث ألفا بعمر نصفي يبلغ 18.68 يوماً) في علاجات السرطان مثل علاجات ألفا المستهدفة.[19][20][21] كما يخضع 232Th في حالات نادرة جداً للانشطار التلقائي بدلاً من انحلال ألفا الإشعاعي، وقد ترك أدلة على ذلك في معادنه (على شكل غاز زينون محصور ناتج عن الانشطار)، لكن العمر النصفي الجزئي لهذه العملية كبير جداً، إذ يتجاوز 1021 سنة، ويسود انحلال ألفا الإشعاعي.[22][23]
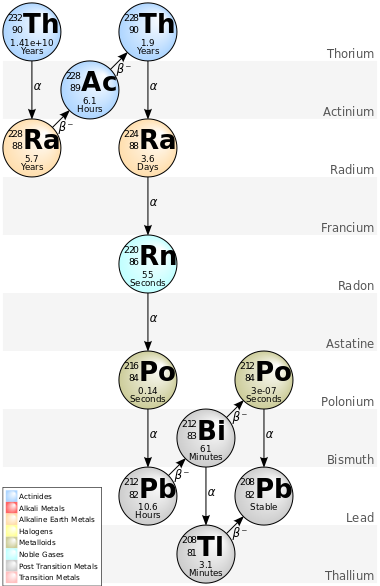
بصفة إجمالية، تم تحديد 32 نظيراً مشعاً في المجموع، وتتراوح أعدادها الكتلية من 207[24] إلى 238.[22] بعد 232Th، فإن أكثرها استقراراً (مع عمرها النصفي) هي 230Th (75.380 سنة)، 229Th (7.917 سنة)، 228Th (1.92 سنة)، 234Th (24.10 يوماً)، و227Th (18.68 يوماً). توجد جميع هذه النظائر في الطبيعة على شكل آثار نظائر مشعة نتيجة وجودها في سلاسل انحلال 232Th، 235U، 238U، و 237Np: آخر هذه النظائر فهو نظير مشع ضئيل بطبيعته نظراً لقصر عمره النصفي (2.14 مليون سنة)، لكنه يُنتج باستمرار بكميات ضئيلة من خلال عملية التقاط النيوترونات في خامات اليورانيوم. أما نظائر الثوريوم المتبقية، فجميعها لها عمر نصفي أقل من ثلاثين يوماً، ومعظمها أعماره النصفية أقل من عشر دقائق.[10]
في مياه البحر العميقة، يشكل النظير 230Th ما يصل إلى 0.02% من الثوريوم الطبيعي.[25] ويعود ذلك إلى أن النظير 238U، وهو النظير الأصلي للثوريوم، قابل للذوبان في الماء، بينما 230Th غير قابل للذوبان ويترسب في الرواسب. ويمكن تنقية خامات اليورانيوم ذات التركيزات المنخفضة من الثوريوم لإنتاج عينات من الثوريوم بحجم الجرام، يشكل نظير 230Th أكثر من ربعها، كونه أحد نواتج تحلل 238U.[22] عام 2013 أعاد الاتحاد الدولي للكيمياء البحتة والتطبيقية تصنيف الثوريوم كعنصر ثنائي النواة؛ وكان يعتبر في السابق عنصر أحادي النواة.[26]
للثوريوم ثلاثة مصاوغات نووية معروفة (أو حالات شبه مستقرة)، وهي: 216m1Th، 216m2Th، و 229mTh. يمتلك 229mTh أدنى طاقة إثارة معروفة بين جميع المصاوغات،[27] إذ يُقدر بنحو 7.6±0.5 eV. ويعتبر هذا منخفض للغاية لدرجة أنه عندما يخضع للانتقال المتزامر، يكون إشعاع گاما المنبعث في نطاق الأشعة فوق البنفسجية.[28][29][ت] يتم التحقيق من الانتقال النووي من النظير 229Th إلى 229mTh من أجل الساعة النووية.[29]
تتشابه النظائر المختلفة للثوريوم كيميائياً، لكنها تختلف قليلاً في خصائصها الفيزيائية: على سبيل المثال، من المتوقع أن تكون كثافة نظائر الثوريوم النقية 228Th، 229Th، 230Th، و232Th على التوالي 11.5، 11.6، 11.6، و11.7 جم/سم3.[31] من المتوقع أن يكون النظير 229Th قابلاً للانشطار بكتلة حرجة أساسية تبلغ 2839 كجم، على الرغم من أنه باستخدام عاكسات النيوترونات الفولاذية، قد تنخفض هذه القيمة إلى 994 كجم.[31][ث] sup>232Th غير قابل للانشطار، لكنه خصباً لأنه يمكن تحويله إلى 233U القابل للانشطار عن طريق التقاط النيوترونات والانحلال اللاحق بجسيمات بيتا.[31][32]
التأريخ الإشعاعي
Two radiometric dating methods involve thorium isotopes: uranium–thorium dating, based on the decay of 234U to 230Th, and ionium–thorium dating, which measures the ratio of 232Th to 230Th.[ج] These rely on the fact that 232Th is a primordial radioisotope, but 230Th only occurs as an intermediate decay product in the decay chain of 238U.[33] Uranium–thorium dating is a relatively short-range process because of the short half-lives of 234U and 230Th relative to the age of the Earth: it is also accompanied by a sister process involving the alpha decay of 235U into 231Th, which very quickly becomes the longer-lived 231Pa, and this process is often used to check the results of uranium–thorium dating. Uranium–thorium dating is commonly used to determine the age of calcium carbonate materials such as speleothem or coral, because uranium is more soluble in water than thorium and protactinium, which are selectively precipitated into ocean-floor sediments, where their ratios are measured. The scheme has a range of several hundred thousand years.[33][34] Ionium–thorium dating is a related process, which exploits the insolubility of thorium (both 232Th and 230Th) and thus its presence in ocean sediments to date these sediments by measuring the ratio of 232Th to 230Th.[35][36] Both of these dating methods assume that the proportion of 230Th to 232Th is a constant during the period when the sediment layer was formed, that the sediment did not already contain thorium before contributions from the decay of uranium, and that the thorium cannot migrate within the sediment layer.[35][36]
الكيمياء
A thorium atom has 90 electrons, of which four are valence electrons. Four atomic orbitals are theoretically available for the valence electrons to occupy: 5f, 6d, 7s, and 7p.[37] Despite thorium's position in the f-block of the periodic table, it has an anomalous [Rn]6d27s2 electron configuration in the ground state, as the 5f and 6d subshells in the early actinides are very close in energy, even more so than the 4f and 5d subshells of the lanthanides: thorium's 6d subshells are lower in energy than its 5f subshells, because its 5f subshells are not well-shielded by the filled 6s and 6p subshells and are destabilized. This is due to relativistic effects, which become stronger near the bottom of the periodic table, specifically the relativistic spin–orbit interaction. The closeness in energy levels of the 5f, 6d, and 7s energy levels of thorium results in thorium almost always losing all four valence electrons and occurring in its highest possible oxidation state of +4. This is different from its lanthanide congener cerium, in which +4 is also the highest possible state, but +3 plays an important role and is more stable. Thorium is much more similar to the transition metals zirconium and hafnium than to cerium in its ionization energies and redox potentials, and hence also in its chemistry: this transition-metal-like behaviour is the norm in the first half of the actinide series.[38][39]
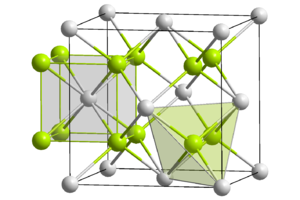
Th4+: __ / O2−: __
Despite the anomalous electron configuration for gaseous thorium atoms, metallic thorium shows significant 5f involvement. A hypothetical metallic state of thorium that had the [Rn]6d27s2 configuration with the 5f orbitals above the Fermi level should be hexagonal close packed like the group 4 elements titanium, zirconium, and hafnium, and not face-centred cubic as it actually is. The actual crystal structure can only be explained when the 5f states are invoked, proving that thorium is metallurgically a true actinide.[8]
Tetravalent thorium compounds are usually colourless or yellow, like those of silver or lead, as the Th4+ ion has no 5f or 6d electrons.[7] Thorium chemistry is therefore largely that of an electropositive metal forming a single diamagnetic ion with a stable noble-gas configuration, indicating a similarity between thorium and the main group elements of the s-block.[40][ح] Thorium and uranium are the most investigated of the radioactive elements because their radioactivity is low enough not to require special handling in the laboratory.[41]
التفاعلات الكيميائية
Thorium is a highly reactive and electropositive metal. With a standard reduction potential of −1.90 V for the Th4+/Th couple, it is somewhat more electropositive than zirconium or aluminium.[42] Finely divided thorium metal can exhibit pyrophoricity, spontaneously igniting in air.[5] When heated in air, thorium turnings ignite and burn with a brilliant white light to produce the dioxide. In bulk, the reaction of pure thorium with air is slow, although corrosion may occur after several months; most thorium samples are contaminated with varying degrees of the dioxide, which greatly accelerates corrosion.[5] Such samples slowly tarnish, becoming grey and finally black at the surface.[5]
At standard temperature and pressure, thorium is slowly attacked by water, but does not readily dissolve in most common acids, with the exception of hydrochloric acid, where it dissolves leaving a black insoluble residue of ThO(OH,Cl)H.[5][43] It dissolves in concentrated nitric acid containing a small quantity of catalytic fluoride or fluorosilicate ions;[5][44] if these are not present, passivation by the nitrate can occur, as with uranium and plutonium.[5][45][46]
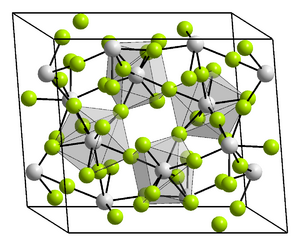
Th4+: __ / F−
: __
المركبات غير العضوية
Most binary compounds of thorium with nonmetals may be prepared by heating the elements together.[47] In air, thorium burns to form ThO
2, which has the fluorite structure.[48] Thorium dioxide is a refractory material, with the highest melting point (3390 °C) of any known oxide.[49] It is somewhat hygroscopic and reacts readily with water and many gases;[50] it dissolves easily in concentrated nitric acid in the presence of fluoride.[51]
When heated in air, thorium dioxide emits intense blue light; the light becomes white when ThO
2 is mixed with its lighter homologue cerium dioxide (CeO
2, ceria): this is the basis for its previously common application in gas mantles.[50] A flame is not necessary for this effect: in 1901, it was discovered that a hot Welsbach gas mantle (using ThO
2 with 1% CeO
2) remained at "full glow" when exposed to a cold unignited mixture of flammable gas[which?] and air.[52] The light emitted by thorium dioxide is higher in wavelength than the blackbody emission expected from incandescence at the same temperature, an effect called candoluminescence. It occurs because ThO
2 : Ce acts as a catalyst for the recombination of free radicals that appear in high concentration in a flame, whose deexcitation releases large amounts of energy. The addition of 1% cerium dioxide, as in gas mantles, heightens the effect by increasing emissivity in the visible region of the spectrum; but because cerium, unlike thorium, can occur in multiple oxidation states, its charge and hence visible emissivity will depend on the region on the flame it is found in (as such regions vary in their chemical composition and hence how oxidising or reducing they are).[52]
Several binary thorium chalcogenides and oxychalcogenides are also known with sulfur, selenium, and tellurium.[53]
All four thorium tetrahalides are known, as are some low-valent bromides and iodides:[54] the tetrahalides are all 8-coordinated hygroscopic compounds that dissolve easily in polar solvents such as water.[55] Many related polyhalide ions are also known.[54] Thorium tetrafluoride has a monoclinic crystal structure like those of zirconium tetrafluoride and hafnium tetrafluoride, where the Th4+ ions are coordinated with F−
ions in somewhat distorted square antiprisms.[54] The other tetrahalides instead have dodecahedral geometry.[55] Lower iodides ThI
3 (black) and ThI
2 (gold-coloured) can also be prepared by reducing the tetraiodide with thorium metal: they do not contain Th(III) and Th(II), but instead contain Th4+ and could be more clearly formulated as electride compounds.[54] Many polynary halides with the alkali metals, barium, thallium, and ammonium are known for thorium fluorides, chlorides, and bromides.[54] For example, when treated with potassium fluoride and hydrofluoric acid, Th4+ forms the complex anion [ThF
6]2− (hexafluorothorate(IV)), which precipitates as an insoluble salt, K
2[ThF
6] (potassium hexafluorothorate(IV)).[44]
Thorium borides, carbides, silicides, and nitrides are refractory materials, like those of uranium and plutonium, and have thus received attention as possible nuclear fuels.[47] All four heavier pnictogens (phosphorus, arsenic, antimony, and bismuth) also form binary thorium compounds. Thorium germanides are also known.[56] Thorium reacts with hydrogen to form the thorium hydrides ThH
2 and Th
4H
15, the latter of which is superconducting below 7.5–8 K; at standard temperature and pressure, it conducts electricity like a metal.[57] The hydrides are thermally unstable and readily decompose upon exposure to air or moisture.[58]
المركبات التساندية
In an acidic aqueous solution, thorium occurs as the tetrapositive aqua ion [Th(H
2O)
9]4+, which has tricapped trigonal prismatic molecular geometry:[59][60] at pH < 3, the solutions of thorium salts are dominated by this cation.[59] The Th4+ ion is the largest of the tetrapositive actinide ions, and depending on the coordination number can have a radius between 0.95 and 1.14 Å.[59] It is quite acidic due to its high charge, slightly stronger than sulfurous acid: thus it tends to undergo hydrolysis and polymerisation (though to a lesser extent than Fe3+), predominantly to [Th
2(OH)
2]6+ in solutions with pH 3 or below, but in more alkaline solution polymerisation continues until the gelatinous hydroxide Th(OH)
4 forms and precipitates out (though equilibrium may take weeks to be reached, because the polymerisation usually slows down before the precipitation).[61] As a hard Lewis acid, Th4+ favours hard ligands with oxygen atoms as donors: complexes with sulfur atoms as donors are less stable and are more prone to hydrolysis.[38]
High coordination numbers are the rule for thorium due to its large size. Thorium nitrate pentahydrate was the first known example of coordination number 11, the oxalate tetrahydrate has coordination number 10, and the borohydride (first prepared in the Manhattan Project) has coordination number 14.[61] These thorium salts are known for their high solubility in water and polar organic solvents.[7]
Many other inorganic thorium compounds with polyatomic anions are known, such as the perchlorates, sulfates, sulfites, nitrates, carbonates, phosphates, vanadates, molybdates, and chromates, and their hydrated forms.[62] They are important in thorium purification and the disposal of nuclear waste, but most of them have not yet been fully characterized, especially regarding their structural properties.[62] For example, thorium nitrate is produced by reacting thorium hydroxide with nitric acid: it is soluble in water and alcohols and is an important intermediate in the purification of thorium and its compounds.[62] Thorium complexes with organic ligands, such as oxalate, citrate, and EDTA, are much more stable. In natural thorium-containing waters, organic thorium complexes usually occur in concentrations orders of magnitude higher than the inorganic complexes, even when the concentrations of inorganic ligands are much greater than those of organic ligands.[59]
-C
8H
8)ThCl
2(THF)
2
In January 2021, the aromaticity has been observed in a large metal cluster anion consisting of 12 bismuth atoms stabilised by a center thorium cation.[63] This compound was shown to be surprisingly stable, unlike many previous known aromatic metal clusters.
مركبات الثوريوم العضوية
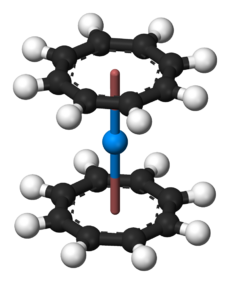
Most of the work on organothorium compounds has focused on the cyclopentadienyl complexes and cyclooctatetraenyls. Like many of the early and middle actinides (up to americium, and also expected for curium), thorium forms a cyclooctatetraenide complex: the yellow Th(C
8H
8)
2, thorocene. It is isotypic with the better-known analogous uranium compound uranocene.[64] It can be prepared by reacting K
2C
8H
8 with thorium tetrachloride in tetrahydrofuran (THF) at the temperature of dry ice, or by reacting thorium tetrafluoride with MgC
8H
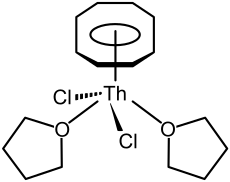
8.[64] It is unstable in air and decomposes in water or at 190 °C.[64] Half sandwich compounds are also known, such as (η8
-C
8H
8)ThCl
2(THF)
2, which has a piano-stool structure and is made by reacting thorocene with thorium tetrachloride in tetrahydrofuran.[38]
The simplest of the cyclopentadienyls are Th(C
5H
5)
3 and Th(C
5H
5)
4: many derivatives are known. The former (which has two forms, one purple and one green) is a rare example of thorium in the formal +3 oxidation state;[64][65] a formal +2 oxidation state occurs in a derivative.[66] The chloride derivative [Th(C
5H
5)
3Cl] is prepared by heating thorium tetrachloride with limiting KC
5H
5 used (other univalent metal cyclopentadienyls can also be used). The alkyl and aryl derivatives are prepared from the chloride derivative and have been used to study the nature of the Th–C sigma bond.[65]
Other organothorium compounds are not well-studied. Tetrabenzylthorium, Th(CH
2C
6H
5)
4, and tetraallylthorium, Th(CH
2CH=CH
2)
4, are known, but their structures have not been determined. They decompose slowly at room temperature. Thorium forms the monocapped trigonal prismatic anion [Th(CH
3)
7]3−, heptamethylthorate(IV), which forms the salt [Li(tmeda)]
3[Th(CH
3)
7] (tmeda = (CH
3)
2NCH
2CH
2N(CH
3)
2). Although one methyl group is only attached to the thorium atom (Th–C distance 257.1 pm) and the other six connect the lithium and thorium atoms (Th–C distances 265.5–276.5 pm), they behave equivalently in solution. Tetramethylthorium, Th(CH
3)
4, is not known, but its adducts are stabilised by phosphine ligands.[38]
التواجد
التشكل
232Th is a primordial nuclide formed in the r-process, which probably occurs in supernovae and neutron star mergers. These violent events scattered it across the galaxy.[67][68] The letter "r" stands for "rapid neutron capture", and occurs in core-collapse supernovae, where heavy seed nuclei such as 56Fe rapidly capture neutrons, running up against the neutron drip line, as neutrons are captured much faster than the resulting nuclides can beta decay back toward stability. Neutron capture is the only way for stars to synthesise elements beyond iron because of the increased Coulomb barriers that make interactions between charged particles difficult at high atomic numbers and the fact that fusion beyond 56Fe is endothermic.[69] Because of the abrupt loss of stability past 209Bi, the r-process is the only process of stellar nucleosynthesis that can create thorium and uranium; all other processes are too slow and the intermediate nuclei alpha decay before they capture enough neutrons to reach these elements.[67][70][71]
التوافر
In the universe, thorium is among the rarest of the primordial elements at rank 77th in cosmic abundance[67][72] because it is one of the two elements that can be produced only in the r-process (the other being uranium), and also because it has slowly been decaying away from the moment it formed. The only primordial elements rarer than thorium are thulium, lutetium, tantalum, and rhenium, the odd-numbered elements just before the third peak of r-process abundances around the heavy platinum group metals, as well as uranium.[67][69][خ] In the distant past the abundances of thorium and uranium were enriched by the decay of plutonium and curium isotopes, and thorium was enriched relative to uranium by the decay of 236U to 232Th and the natural depletion of 235U, but these sources have long since decayed and no longer contribute.[73]
In the Earth's crust, thorium is much more abundant: with an abundance of 8.1 g/tonne, it is one of the most abundant of the heavy elements, almost as abundant as lead (13 g/tonne) and more abundant than tin (2.1 g/tonne).[74] This is because thorium is likely to form oxide minerals that do not sink into the core; it is classified as a lithophile under the Goldschmidt classification, meaning that it is generally found combined with oxygen. Common thorium compounds are also poorly soluble in water. Thus, even though the refractory elements have the same relative abundances in the Earth as in the Solar System as a whole, there is more accessible thorium than heavy platinum group metals in the crust.[75]
على الأرض
Natural thorium is usually almost pure 232Th, which is the longest-lived and most stable isotope of thorium, having a half-life comparable to the age of the universe.[22] Its radioactive decay is the largest single contributor to the Earth's internal heat; the other major contributors are the shorter-lived primordial radionuclides, which are 238U, 40K, and 235U in descending order of their contribution. (At the time of the Earth's formation, 40K and 235U contributed much more by virtue of their short half-lives, but they have decayed more quickly, leaving the contribution from 232Th and 238U predominant.)[80] Its decay accounts for a gradual decrease of thorium content of the Earth: the planet currently has around 80% of the amount present at the formation of the Earth.[81] The other natural thorium isotopes are much shorter-lived; of them, only 230Th is usually detectable, occurring in secular equilibrium with its parent 238U, and making up at most 0.04% of natural thorium.[22][د]
Thorium only occurs as a minor constituent of most minerals, and was for this reason previously thought to be rare.[83][84] In fact, it is the 37th most abundant element in the Earth's crust with an abundance of 12 parts per million.[85] In nature, thorium occurs in the +4 oxidation state, together with uranium(IV), zirconium(IV), hafnium(IV), and cerium(IV), and also with scandium, yttrium, and the trivalent lanthanides which have similar ionic radii.[83] Because of thorium's radioactivity, minerals containing it are often metamict (amorphous), their crystal structure having been damaged by the alpha radiation produced by thorium.[86] An extreme example is ekanite, (Ca,Fe,Pb)
2(Th,U)Si
8O
20, which almost never occurs in nonmetamict form due to the thorium it contains.[87]
Monazite (chiefly phosphates of various rare-earth elements) is the most important commercial source of thorium because it occurs in large deposits worldwide, principally in India, South Africa, Brazil, Australia, and Malaysia and is mined for its rare earth content. It contains around 2.5% thorium on average, although some deposits may contain up to 20%.[83][88] Monazite is a chemically unreactive mineral that is found as yellow or brown sand; its low reactivity makes it difficult to extract thorium from it.[83] Allanite (chiefly silicates-hydroxides of various metals) can have 0.1–2% thorium and zircon (chiefly zirconium silicate, ZrSiO
4) up to 0.4% thorium.[83]
Thorium dioxide occurs as the rare mineral thorianite. Due to its being isotypic with uranium dioxide, these two common actinide dioxides can form solid-state solutions and the name of the mineral changes according to the ThO
2 content.[83][ذ] Thorite (chiefly thorium silicate, ThSiO
4), also has a high thorium content and is the mineral in which thorium was first discovered.[83] In thorium silicate minerals, the Th4+ and SiO4−
4 ions are often replaced with M3+ (where M = Sc, Y, or Ln) and phosphate (PO3−
4) ions respectively.[83] Because of the great insolubility of thorium dioxide, thorium does not usually spread quickly through the environment when released. The Th4+ ion is soluble, especially in acidic soils, and in such conditions the thorium concentration can be higher.[49]
التاريخ

Erroneous report
In 1815, the Swedish chemist Jöns Jacob Berzelius analysed an unusual sample of gadolinite from a copper mine in Falun, central Sweden. He noted impregnated traces of a white mineral, which he cautiously assumed to be an earth (oxide in modern chemical nomenclature) of an unknown element. Berzelius had already discovered two elements, cerium and selenium, but he had made a public mistake once, announcing a new element, gahnium, that turned out to be zinc oxide.[90] Berzelius privately named the putative element "thorium" in 1817[91] and its supposed oxide "thorina" after Thor, the Norse god of thunder.[92] In 1824, after more deposits of the same mineral in Vest-Agder, Norway, were discovered, he retracted his findings, as the mineral (later named xenotime) proved to be mostly yttrium orthophosphate.[32][90][93][94]
الإكتشاف
In 1828, Morten Thrane Esmark found a black mineral on Løvøya island, Telemark county, Norway. He was a Norwegian priest and amateur mineralogist who studied the minerals in Telemark, where he served as vicar. He commonly sent the most interesting specimens, such as this one, to his father, Jens Esmark, a noted mineralogist and professor of mineralogy and geology at the Royal Frederick University in Christiania (today called Oslo).[95] The elder Esmark determined that it was not a known mineral and sent a sample to Berzelius for examination. Berzelius determined that it contained a new element.[32] He published his findings in 1829, having isolated an impure sample by reducing K[ThF
5] (potassium pentafluorothorate(IV)) with potassium metal.[96][97][98] Berzelius reused the name of the previous supposed element discovery[96][99] and named the source mineral thorite.[32]

Berzelius made some initial characterisations of the new metal and its chemical compounds: he correctly determined that the thorium–oxygen mass ratio of thorium oxide was 7.5 (its actual value is close to that, ~7.3), but he assumed the new element was divalent rather than tetravalent, and so calculated that the atomic mass was 7.5 times that of oxygen (120 Da); it is actually 15 times as large.[ر] He determined that thorium was a very electropositive metal, ahead of cerium and behind zirconium in electropositivity.[100] Metallic thorium was isolated for the first time in 1914 by Dutch entrepreneurs Dirk Lely Jr. and Lodewijk Hamburger.[ز]
التصنيف الكيميائي الأولي
In the periodic table published by Dmitri Mendeleev in 1869, thorium and the rare-earth elements were placed outside the main body of the table, at the end of each vertical period after the alkaline earth metals. This reflected the belief at that time that thorium and the rare-earth metals were divalent. With the later recognition that the rare earths were mostly trivalent and thorium was tetravalent, Mendeleev moved cerium and thorium to group IV in 1871, which also contained the modern carbon group (group 14) and titanium group (group 4), because their maximum oxidation state was +4.[103][104] Cerium was soon removed from the main body of the table and placed in a separate lanthanide series; thorium was left with group 4 as it had similar properties to its supposed lighter congeners in that group, such as titanium and zirconium.[105][س]
الاستخدامات الأولية

While thorium was discovered in 1828 its first application dates only from 1885, when Austrian chemist Carl Auer von Welsbach invented the gas mantle, a portable source of light which produces light from the incandescence of thorium oxide when heated by burning gaseous fuels.[32] Many applications were subsequently found for thorium and its compounds, including ceramics, carbon arc lamps, heat-resistant crucibles, and as catalysts for industrial chemical reactions such as the oxidation of ammonia to nitric acid.[106]
النشاط الإشعاعي
Thorium was first observed to be radioactive in 1898, by the German chemist Gerhard Carl Schmidt and later that year, independently, by the Polish-French physicist Marie Curie. It was the second element that was found to be radioactive, after the 1896 discovery of radioactivity in uranium by French physicist Henri Becquerel.[107][108][109] Starting from 1899, the New Zealand physicist Ernest Rutherford and the American electrical engineer Robert Bowie Owens studied the radiation from thorium; initial observations showed that it varied significantly. It was determined that these variations came from a short-lived gaseous daughter of thorium, which they found to be a new element. This element is now named radon, the only one of the rare radioelements to be discovered in nature as a daughter of thorium rather than uranium.[110]
After accounting for the contribution of radon, Rutherford, now working with the British physicist Frederick Soddy, showed how thorium decayed at a fixed rate over time into a series of other elements in work dating from 1900 to 1903. This observation led to the identification of the half-life as one of the outcomes of the alpha particle experiments that led to the disintegration theory of radioactivity.[111] The biological effect of radiation was discovered in 1903.[112] The newly discovered phenomenon of radioactivity excited scientists and the general public alike. In the 1920s, thorium's radioactivity was promoted as a cure for rheumatism, diabetes, and sexual impotence. In 1932, most of these uses were banned in the United States after a federal investigation into the health effects of radioactivity.[113] 10,000 individuals in the United States had been injected with thorium during X-ray diagnosis; they were later found to suffer health issues such as leukaemia and abnormal chromosomes.[49] Public interest in radioactivity had declined by the end of the 1930s.[113]

التصنيف الإضافي
Up to the late 19th century, chemists unanimously agreed that thorium and uranium were the heaviest members of group 4 and group 6 respectively; the existence of the lanthanides in the sixth row was considered to be a one-off fluke. In 1892, British chemist Henry Bassett postulated a second extra-long periodic table row to accommodate known and undiscovered elements, considering thorium and uranium to be analogous to the lanthanides. In 1913, Danish physicist Niels Bohr published a theoretical model of the atom and its electron orbitals, which soon gathered wide acceptance. The model indicated that the seventh row of the periodic table should also have f-shells filling before the d-shells that were filled in the transition elements, like the sixth row with the lanthanides preceding the 5d transition metals.[103] The existence of a second inner transition series, in the form of the actinides, was not accepted until similarities with the electron structures of the lanthanides had been established;[114] Bohr suggested that the filling of the 5f orbitals may be delayed to after uranium.[103]
It was only with the discovery of the first transuranic elements, which from plutonium onward have dominant +3 and +4 oxidation states like the lanthanides, that it was realised that the actinides were indeed filling f-orbitals rather than d-orbitals, with the transition-metal-like chemistry of the early actinides being the exception and not the rule.[115] In 1945, when American physicist Glenn T. Seaborg and his team had discovered the transuranic elements americium and curium, he proposed the actinide concept, realising that thorium was the second member of an f-block actinide series analogous to the lanthanides, instead of being the heavier congener of hafnium in a fourth d-block row.[105][ش]
Phasing out
In the 1990s, most applications that do not depend on thorium's radioactivity declined quickly due to safety and environmental concerns as suitable safer replacements were found.[32][119] Despite its radioactivity, the element has remained in use for applications where no suitable alternatives could be found. A 1981 study by the Oak Ridge National Laboratory in the United States estimated that using a thorium gas mantle every weekend would be safe for a person,[119] but this was not the case for the dose received by people manufacturing the mantles or for the soils around some factory sites.[120] Some manufacturers have changed to other materials, such as yttrium.[121] As recently as 2007, some companies continued to manufacture and sell thorium mantles without giving adequate information about their radioactivity, with some even falsely claiming them to be non-radioactive.[119][122]
الطاقة النووية

Thorium has been used as a power source on a prototype scale. The earliest thorium-based reactor was built at the Indian Point Energy Center located in Buchanan, New York, United States in 1962.[123] China may be the first to have attempted to commercialise the technology.[124] The country with the largest estimated reserves of thorium in the world is India, which has sparse reserves of uranium. In the 1950s, India targeted achieving energy independence with their three-stage nuclear power programme.[125][126] In most countries, uranium was relatively abundant and the progress of thorium-based reactors was slow; in the 20th century, three reactors were built in India and twelve elsewhere.[127] Large-scale research was begun in 1996 by the International Atomic Energy Agency to study the use of thorium reactors; a year later, the United States Department of Energy started their research. Alvin Radkowsky of Tel Aviv University in Israel was the head designer of Shippingport Atomic Power Station in Pennsylvania, the first American civilian reactor to breed thorium.[128] He founded a consortium to develop thorium reactors, which included other laboratories: Raytheon Nuclear Inc. and Brookhaven National Laboratory in the United States, and the Kurchatov Institute in Russia.[129]
In the 21st century, thorium's potential for reducing nuclear proliferation and its waste characteristics led to renewed interest in the thorium fuel cycle.[130][131][132] India has projected meeting as much as 30% of its electrical demands through thorium-based nuclear power by 2050. In February 2014, Bhabha Atomic Research Centre (BARC), in Mumbai, India, presented their latest design for a "next-generation nuclear reactor" that burns thorium as its fuel core, calling it the Advanced Heavy Water Reactor (AHWR). In 2009, the chairman of the Indian Atomic Energy Commission said that India has a "long-term objective goal of becoming energy-independent based on its vast thorium resources."
On 16 June 2023 China's National Nuclear Safety Administration issued a licence to the Shanghai Institute of Applied Physics (SINAP) of the Chinese Academy of Sciences to begin operating the TMSR-LF1, 2 MWt liquid fuel thorium-based molten salt experimental reactor which was completed in August 2021.[133] China is believed to have one of the largest thorium reserves in the world. The exact size of those reserves has not been publicly disclosed, but it is estimated to be enough to meet the country's total energy needs for more than 20,000 years.[134]
الأسلحة النووية
عند إنتاج كميات بالجرام من پلوتونيوم لأول مرة في مشروع منهاتن، اكتُشف أن نظيراً ثانوياً (240Pu) خضع لانشطار تلقائي كبير، مما أثار الشكوك حول جدوى استخدام سلاح نووي يعمل بالپلوتونيوم. وبينما بدأ فريق لوس ألاموس العمل على تصميم سلاح نووي داخلي الانفجار لتجاوز هذه المشكلة، ناقش فريق شيكاغو حلولاً لتصميم المفاعلات. اقترح يوجين ويگنر استخدام الپلوتونيوم الملوث بالنظير 240Pu لتحفيز تحويل الثوريوم إلى 233U في مفاعل تحويل خاص. وافتُرض أن 233U سيكون قابلاً للاستخدام في سلاح ناري، على الرغم من وجود مخاوف بشأن التلوث بالنظير 232U. كان التقدم المحرز في سلاح الانفجار الداخلي كافياً، ولم يُطوَّر هذا المحول أكثر من ذلك، لكن تصميمه كان له تأثير هائل على تطوير الطاقة النووية. وكان هذا أول وصف تفصيلي لمفاعل عالي التخصيب، مُبرَّد بالماء، ومُهدَّأ بالماء، يُشبه مفاعلات الطاقة البحرية والتجارية المستقبلية.[135]
عام 1943، تعاقد مشروع منهاتن مع شركتين خاصتين، هما يونيون كاربايد وشڤرون، لإجراء مسح سري لرواسب اليورانيوم والثوريوم حول العالم. كان التركيز الأساسي على اليورانيوم، لكن في المراحل الأولى من العملية، أُضيف الثوريوم أيضاً. تم تحديد رواسب رمال المونازيت في البرازيل، جزر الهند الشرقية الهولندية، وتراڤنكور في الهند، لكن لم يتابع المشروع أياً منها.[136]
أثناء الحرب الباردة، استكشفت الولايات المتحدة إمكانية استخدام 232Th كمصدر لـ 233U لاستخدامه في قنبلة نووية، وأطلقت قنبلة تجريبية عام 1955.[137] وخلصت الدراسة إلى أن القنبلة التي ستُصنع بواسطة 233U ستكون سلاحاً قوياً للغاية، لكنها لا تتمتع إلا بمزايا تقنية قليلة مستدامة مقارنة بالقنابل المعاصرة التي تحتوي على اليورانيوم والپلوتونيوم،[138] خاصة وأن إنتاج 233U في صورة نقية نظائرياً أمر صعب.[137]
أُستخدم فلز الثوريوم في الحالة الإشعاعية لتصميم سلاح نووي واحد على الأقل نشرته الولايات المتحدة (W71).[139]
الإنتاج
| البلد | الاحتياطيات |
|---|---|
| الهند | 846 |
| البرازيل | 632 |
| أستراليا | 595 |
| الولايات المتحدة | 595 |
| مصر | 380 |
| تركيا | 374 |
| ڤنزويلا | 300 |
| كندا | 172 |
| روسيا | 155 |
| جنوب أفريقيا | 148 |
| الصين | 100 |
| النرويج | 87 |
| گرينلاند | 86 |
| فنلندا | 60 |
| السويد | 50 |
| قزخستان | 50 |
| بلدان أخرى | 1725 |
| الإجمالي العالمي | 6355 |
يؤدي انخفاض الطلب إلى عدم جدوى تشغيل المناجم لاستخراج الثوريوم وحده، ويُستخرج دائماً تقريباً مع العناصر الأرضية النادرة، والتي قد تكون بدورها منتجات ثانوية لإنتاج معادن أخرى.[140] يعود الاعتماد الحالي على المونازيت في الإنتاج إلى أن الثوريوم يُنتج بشكل كبير كمنتج ثانوي؛ بينما تحتوي مصادر أخرى مثل الثوريت على كميات أكبر من الثوريوم، ويمكن استخدامها بسهولة في الإنتاج إذا ارتفع الطلب.[141] المعرفة الحالية بتوزيع موارد الثوريوم ضعيفة، حيث أدى انخفاض الطلب إلى أن تكون جهود الاستكشاف ضئيلة نسبياً.[142] عام 2014، بلغ الإنتاج العالمي من مركز المونازيت، الذي سيُستخرج الثوريوم منه، 2.700 طن.[143]
تتضمن طريقة الإنتاج الشائعة للثوريوم تركيز معادن الثوريوم؛ واستخلاص الثوريوم من المركز؛ وتنقية الثوريوم؛ وتحويله (اختيارياً) إلى مركبات، مثل ثاني أكسيد الثوريوم.[144]
التركيز
توجد فئتان من معادن الثوريوم المستخدمة في استخلاصه: أولية وثانوية. تتواجد الرواسب الأولية في الصهارة الگرانيتية الحمضية والپگماتيت، وهي رواسب مركزة لكنها صغيرة الحجم. أما الرواسب الثانوية فتتواجد عند مصبات الأنهار في المناطق الجبلية الگرانيتية، حيث يزداد تركيز الثوريوم فيها مع معادن ثقيلة أخرى.[42] يختلف التركيز الأولي باختلاف نوع الرواسب.[144]
بالنسبة للرواسب الأولية، تٌقسم موارد الپگماتيت، التي تُستخرج عادةً من التعدين، إلى أجزاء صغيرة ثم تُخضع لعملية التعويم. ويمكن إزالة كربونات الفلزات القلوية الأرضية بعد تفاعلها مع كلوريد الهيدروجين، ثم تُجرى عمليات التثخين والترشيح والتكليس. والنتيجة هي مُركّز يحتوي على نسبة من العناصر الأرضية النادرة تصل إلى 90%.[144] أما المواد الثانوية (مثل الرمال الساحلية) فتُفصل بالجاذبية، ثم تُفصل مغناطيسياً باستخدام سلسلة من المغناطيسات ذات قوة متزايدة. ويمكن أن تصل نقاوة المونازيت المُستخلص بهذه الطريقة إلى 98%.[144]
اعتمد الإنتاج الصناعي في القرن العشرين على المعالجة بحمض الكبريتيك المركز الساخن في أوعية من الحديد الزهر، متبوعةً بالترسيب الانتقائي عن طريق التخفيف بالماء، كما هو الحال في الخطوات اللاحقة. كانت هذه الطريقة تعتمد على خصائص التقنية وحجم حبيبات المركز؛ وقد طُرحت العديد من البدائل، ولكن واحدة فقط أثبتت فعاليتها الاقتصادية: الهضم القلوي بمحلول هيدروكسيد الصوديوم الساخن. هذه الطريقة أغلى من الطريقة الأصلية، لكنها تُنتج ثوريوم بنقاوة أعلى؛ وعلى وجه الخصوص، فهي تزيل الفوسفات من المركز.[144]
الهضم الحمضي
الهضم الحمضي عملية ثنائية المراحل، تتضمن استخدام حمض الكبريتيك بتركيز يصل إلى 93% عند درجة حرارة تتراوح بين 210 و230°س. في المرحلة الأولى، يُضاف حمض الكبريتيك بكمية تزيد عن 60% من كتلة الرمل، مما يُكثّف مزيج التفاعل مع تكوّن النواتج. ثم يُضاف حمض الكبريتيك المُدخّن ويُحفظ المزيج عند نفس درجة الحرارة لمدة خمس ساعات أخرى لتقليل حجم المحلول المتبقي بعد التخفيف. يُختار تركيز حمض الكبريتيك بناءً على سرعة التفاعل واللزوجة، حيث تزداد كلتاهما مع زيادة التركيز، مع العلم أن اللزوجة تُبطئ التفاعل. كما أن رفع درجة الحرارة يُسرّع التفاعل، ولكن يجب تجنب درجات الحرارة التي تبلغ 300°س وما فوق، لأنها تُسبب تكوّن پيروفوسفات الثوريوم غير القابل للذوبان. ولأن عملية الذوبان طاردة للحرارة بشدة، لا يُمكن إضافة رمل المونازيت إلى الحمض بسرعة كبيرة. على النقيض، عند درجات حرارة أقل من 200 درجة مئوية، لا يسير التفاعل بالسرعة الكافية لجعل العملية عمليةً عملية. ولضمان عدم تكوّن أي رواسب تسد سطح المونازيت المتفاعل، يجب أن تكون كتلة الحمض المستخدم ضعف كتلة الرمل، بدلاً من 60% المتوقعة من حسابات التكافؤ الكيميائي. ثم يُبرّد المزيج إلى 70°س ويُخفف بعشرة أضعاف حجمه من الماء البارد، بحيث يترسب أي مونازيت متبقٍ في القاع بينما تبقى العناصر الأرضية النادرة والثوريوم في المحلول. بعد ذلك، يمكن فصل الثوريوم بترسيبه على شكل فوسفات عند درجة حموضة 1.3، لأن العناصر الأرضية النادرة لا تترسب إلا عند درجة حموضة 2.[144]
الهضم القلوي
تُجرى عملية الهضم القلوي في محلول هيدروكسيد الصوديوم بتركيز 30-45% عند درجة حرارة 140°س لمدة ثلاث ساعات تقريباً. تؤدي درجة الحرارة المرتفعة للغاية إلى تكوّن أكسيد الثوريوم قليل الذوبان وزيادة اليورانيوم في الرشاحة، بينما يؤدي انخفاض تركيز القلوي إلى تفاعل بطيء للغاية. تُعدّ ظروف التفاعل هذه معتدلة نسبياً وتتطلب رمل مونازيت بحجم حبيبات أقل من 45 ميكرومتر. بعد الترشيح، تحتوي كعكة الترشيح على الثوريوم والعناصر الأرضية النادرة على هيئة هيدروكسيداتها، واليورانيوم على هيئة ثنائي يورانات الصوديوم، والفوسفات على هيئة فوسفات ثلاثي الصوديوم. يتبلور فوسفات ثلاثي الصوديوم المائي عند تبريده إلى أقل من 60°س. تزداد شوائب اليورانيوم في هذا المنتج مع كمية ثاني أكسيد السليكون في خليط التفاعل، مما يستلزم إعادة التبلور قبل الاستخدام التجاري. تُذاب الهيدروكسيدات عند درجة حرارة 80°س في حمض الهيدروكلوريك بتركيز 37%. يؤدي ترشيح الرواسب المتبقية، متبوعاً بإضافة هيدروكسيد الصوديوم بتركيز 47%، إلى ترسيب الثوريوم واليورانيوم عند درجة حموضة تقارب 5.8. يجب تجنب التجفيف الكامل للراسب، لأن الهواء قد يؤكسد السريوم من حالة الأكسدة +3 إلى +4، ويمكن للسريوم (IV) المتكون أن يُحرر الكلور الحر من حمض الهيدروكلوريك. تترسب العناصر الأرضية النادرة مرة أخرى عند درجة حموضة أعلى. تُعادل الرواسب بواسطة محلول هيدروكسيد الصوديوم الأصلي، على الرغم من أنه يجب إزالة معظم الفوسفات أولًا لتجنب ترسيب فوسفات العناصر الأرضية النادرة. يمكن أيضًا استخدام الاستخلاص بالمذيبات لفصل الثوريوم واليورانيوم، وذلك بإذابة الكعكة المُرشحة الناتجة في حمض النيتريك. إن وجود هيدروكسيد التيتانيوم ضار لأنه يرتبط بالثوريوم ويمنعه من الذوبان بشكل كامل.[144]
التنقية
تتطلب التطبيقات النووية تركيزات عالية من الثوريوم. وعلى وجه الخصوص، يجب أن تكون تركيزات الذرات ذات المقطع العرضي العالي لالتقاط النيوترونات منخفضة للغاية (على سبيل المثال، يجب أن تكون تركيزات الگادولينيوم أقل من جزء واحد في المليون وزناً). سابقاً، كان يُستخدم التكرار في إذابة وإعادة التبلور لتحقيق نقاء عالي. أما اليوم، فتُستخدم إجراءات استخلاص بالمذيبات السائلة تتضمن تكوين معقدات انتقائية للثوريوم (Th⁴⁺). على سبيل المثال، بعد الهضم القلوي وإزالة الفوسفات، يمكن فصل معقدات النترات الناتجة من الثوريوم واليورانيوم والعناصر الأرضية النادرة عن طريق الاستخلاص باستخدام فوسفات ثلاثي البوتيل في الكيروسين.[144]
التطبيقات الحديثة
تراجعت استخدامات الثوريوم غير المرتبطة بالنشاط الإشعاعي منذ الخمسينيات[145] بسبب المخاوف البيئية الناجمة إلى حد كبير عن النشاط الإشعاعي للثوريوم ونواتج اضمحلاله.[32][119]
تستخدم معظم تطبيقات الثوريوم ثاني أكسيده (الذي يُسمى أحياناً "ثوريا" في الصناعة)، بدلاً من الفلز نفسه. يتميز هذا المركب بنقطة انصهار تبلغ 3.300°س (6000°ف)، وهي أعلى نقطة انصهار بين جميع الأكاسيد المعروفة؛ ولا تتجاوزها في نقاط الانصهار سوى عدد قليل من المواد.[49] يساعد هذا المركب على البقاء صلباً في اللهب، ويزيد بشكل كبير من سطوع اللهب؛ وهذا هو السبب الرئيسي لاستخدام الثوريوم في رتائن مصابيح الغاز.[146] جميع المواد تُصدر طاقة (توهجاً) عند درجات حرارة عالية، لكن الضوء المنبعث من الثوريوم يقع بالكامل تقريباً في الطيف المرئي، ومن هنا يأتي سطوع رتائن الثوريوم.[52]
تُطلق الطاقة، بعضها على شكل ضوء مرئي، عند تعريض الثوريوم لمصدر طاقة، مثل أشعة المهبط أو الحرارة أو الأشعة فوق البنفسجية. ويشترك ثاني أكسيد السريوم في هذه الخاصية، إذ يحول الأشعة فوق البنفسجية إلى ضوء مرئي بكفاءة أعلى، لكن ثاني أكسيد الثوريوم يُعطي درجة حرارة لهب أعلى، ويُصدر كمية أقل من الأشعة تحت الحمراء.[146] على الرغم من أن الثوريوم في الرتائن لا يزال شائعاً، إلا أنه أُستبدل تدريجياً بالإتريوم منذ أواخر التسعينيات.[147] وفقًا لمراجعة عام 2005 التي أجراها المجلس الوطني للحماية من الإشعاع في المملكة المتحدة، "على الرغم من أن [رتائن غاز الثوريا] كانت متوفرة على نطاق واسع قبل بضع سنوات، إلا أنها لم تعد كذلك الآن".[148] يُستخدم الثوريوم أيضاً في صنع مولدات الأيونات السالبة الدائمة الرخيصة، كما هو الحال في الأساور الصحية العلمية الزائفة.[149]
أثناء إنتاج الخيوط المتوهجة، تُقلل إعادة تبلور التنگستن بشكل كبير عن طريق إضافة كميات صغيرة من ثاني أكسيد الثوريوم إلى مسحوق تلبيد التنگستن قبل سحب الخيوط.[145] تؤدي إضافة كمية صغيرة من الثوريوم إلى المهبط الحراري للتنگستن إلى تقليل دالة الشغل للإلكترونات بشكل كبير؛ ونتيجة لذلك، تنبعث الإلكترونات عند درجات حرارة أقل بكثير.[32] يشكل الثوريوم طبقة بسمك ذرة واحدة على سطح التنگستن. تنخفض دالة الشغل لسطح الثوريوم، ربما بسبب المجال الكهربائي المتولد على السطح الفاصل بين الثوريوم والتنگستن نتيجةً لزيادة كهروإيجابية الثوريوم.[150] منذ العشرينيات، استُخدمت أسلاك التنگستن المُثوَّرة في الأنابيب الإلكترونية وفي المهابط والمهابد المضادة لأنابيب الأشعة السينية والمقومات. وقد استلزم تفاعل الثوريوم مع أكسجين الغلاف الجوي إدخال طبقة من المغنيسيوم المُبَخَّر مستأصل للشوائب في الأنابيب المُفرَّغة، مما أكسبها غلافها الداخلي المعدني المميز.[151] أدى إدخال الترانزستورات في الخمسينيات إلى تقليل هذا الاستخدام بشكل كبير، لكن ليس تماماً.[145] يُستخدم ثاني أكسيد الثوريوم في لحام قوسي غاز خامل-التنگستن (GTAW) لزيادة قوة أقطاب التنگستن عند درجات الحرارة العالية وتحسين استقرار القوس.[32] يُستبدل أكسيد الثوريوم في هذا الاستخدام بأكاسيد أخرى، مثل أكاسيد الزركونيوم والسريوم واللانثانم.[152][153]
يوجد ثاني أكسيد الثوريوم في السيراميك الحراري، مثل بوتقات المعامل المقاومة لدرجات الحرارة العالية،[32] يُستخدم إما كمكون أساسي أو يضاف إلى ثاني أكسيد الزركونيوم. تُعد سبيكة من 90% الپلاتين و10% الثوريوم محفزاً فعالاً لأكسدة الأمونيا إلى أكاسيد النيتروجين، لكنها أُستبدلة بسبيكة من 95% الپلاتين و5% الروديوم نظراً لخصائصها الميكانيكية الأفضل ومتانتها الأكبر.[145]

عند إضافته إلى الزجاج، يساعد ثاني أكسيد الثوريوم على زيادة معامل انكساره وتقليل تشتته. يُستخدم هذا النوع من الزجاج في صناعة عدسات عالية الجودة للكاميرات والأجهزة العلمية.[43] قد يؤدي الإشعاع المنبعث من هذه العدسات إلى تعتيمها وتحويلها إلى اللون الأصفر على مدى سنوات، كما أنه يؤدي إلى تلف الفيلم، لكن المخاطر الصحية ضئيلة.[154] يمكن استعادة العدسات المصفرة إلى حالتها الأصلية عديمة اللون عن طريق التعرض المطول للأشعة فوق البنفسجية الشديدة. وقد استُبدل ثاني أكسيد الثوريوم في هذا التطبيق بأكاسيد العناصر الأرضية النادرة، مثل اللانثانم، لأنها توفر تأثيرات مماثلة وليست مشعة.[145]
يُستخدم رباعي فلوريد الثوريوم كمادة مضادة للانعكاس في الطلاءات البصرية متعددة الطبقات. وهو شفاف للموجات الكهرومغناطيسية ذات الأطوال الموجية في نطاق 0.350-12 ميكرومتر، وهو نطاق يشمل الأشعة فوق البنفسجية القريبة والضوء المرئي والأشعة تحت الحمراء المتوسطة. وينتج إشعاعه بشكل أساسي عن جسيمات ألفا، التي يمكن إيقافها بسهولة بواسطة طبقة رقيقة من مادة أخرى.[155] يجري تطوير بدائل لرباعي فلوريد الثوريوم منذ ع. 2010،[156] والتي تشمل ثلاثي فلوريد اللانثانم.
وجدت سبائك المغنسيوم-ثوريوم (وتسمى أيضاً المغنسيوم المثور) استخداماً في بعض تطبيقات الفضاء الجوي، على الرغم من أن هذه الاستخدامات قد تم التخلص منها تدريجياً بسبب المخاوف بشأن النشاط الإشعاعي.
الاستخدام المحتمل للطاقة النووية
المصدر الرئيسي للطاقة النووية في المفاعل هو الانشطار النووي الناتج عن النيوترونات للنواة النووية؛ الانشطاري الاصطناعي [ث] للنواة 233U و 239Pu يمكن توليدها بواسطة مفاعل الاستنسال من خلال التقاط النيوترونات بواسطة النويدات التي تتواجد طبيعياً 232Th و 238U. 235U بكميات كبيرة وهي قابلة للانشطار أيضاً.[157][158][ص] في دورة وقود الثوريوم، يتم قصف النظير الخصب 232Th بواسطة النيوترونات البطيئة، ويخضع لالتقاط النيوترون ليصبح 233Th، والذي يخضع لتحللين بيتا متتاليين ليصبح أولاً 233Pa ثم اليورانيوم الانشطاري 233U:[32]
التحولات في دورة وقود الثوريوم
| ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 237Np | ||||||||||||||
| ↑ | ||||||||||||||
| 231U | ← | 232U | ↔ | 233U | ↔ | 234U | ↔ | 235U | ↔ | 236U | → | 237U | ||
| ↓ | ↑ | ↑ | ↑ | |||||||||||
| 231Pa | → | 232Pa | ← | 233Pa | → | 234Pa | ||||||||
| ↑ | ↑ | |||||||||||||
| 230Th | → | 231Th | ← | 232Th | → | 233Th | ||||||||
| ||||||||||||||
233U قابل للانشطار ويمكن استخدامه كوقود نووي بنفس طريقة 235U أو 239Pu. عندما يخضع 233U للانشطار النووي، يمكن للنيوترونات المنبعثة أن تصطدم بنوى 232Th، مما يُكمل الدورة. يُشابه هذا دورة وقود اليورانيوم في مفاعلات الاستنسال السريع، حيث يخضع 238U لالتقاط النيوترونات ليصبح 239U، ثم يتحلل بيتا إلى 239Np أولاً، ثم إلى 239Pu القابل للانشطار.[159]
ينتج عن انشطار اليورانيوم-233 ما معدله 2.48 نيوترون.[160] يلزم نيوترون واحد لاستمرار تفاعل الانشطار. ولإتمام دورة تكاثر مستمرة ذاتية الاكتفاء، يلزم نيوترون إضافي لتكوين ذرة جديدة من 233U من ذرة 232Th الخصبة. وهذا يترك هامشاً قدره 0.45 نيوترون (أو 18% من تدفق النيوترونات) للفقد.
المزايا
يُعد الثوريوم أكثر وفرة من اليورانيوم، ويمكنه تلبية احتياجات العالم من الطاقة لفترة أطول.[161] وهو مناسب بشكل خاص لاستخدامه كمادة خصبة في مفاعلات الملح المنصهر.
يمتص 232Th النيوترونات بسهولة أكبر من 238U، و233U لديه احتمالية أعلى للانشطار عند التقاط النيوترون (92.0%) من 235U (85.5٪) أو 239Pu (73.5%).[162] في المتوسط، يطلق أيضاً المزيد من النيوترونات عند الانشطار.[161] ينتج عن امتصاص نيوترون واحد بواسطة 238U نفايات عابرة لليورانيوم بالإضافة إلى 239Pu القابل للانشطار، بينما لا ينتج 232Th هذه النفايات إلا بعد خمس عمليات امتصاص، مكوناً 237Np. لا يحدث هذا العدد من عمليات الامتصاص في 98-99% من نوى 232Th لأن النواتج الوسيطة، 233U أو 235U، تخضع للانشطار، مما يؤدي إلى إنتاج عدد أقل من العناصر العابرة لليورانيوم طويلة العمر. لهذا السبب، يُعد الثوريوم بديلاً جذاباً محتملاً لليورانيوم في وقود الأكاسيد المختلطة لتقليل إنتاج العناصر العابرة لليورانيوم إلى أدنى حد وزيادة تدمير الپلوتونيوم إلى أقصى حد.[163]
يؤدي وقود الثوريوم إلى قلب مفاعل أكثر أماناً وأفضل أداءً[32] لأن ثاني أكسيد الثوريوم يتميز بنقطة انصهار أعلى، وتوصيل حراري أعلى، ومعامل تمدد حراري أقل. وهو أكثر استقراراً كيميائياً من ثاني أكسيد اليورانيوم، وهو وقود شائع الاستخدام حالياً، لأن الأخير يتأكسد إلى ثماني أكسيد اليورانيوم الثلاثي (U
3O
8)، مما يجعله أقل كثافة بشكل ملحوظ.[164]
العيوب
يُعدّ إعادة معالجة الوقود المستهلك أمراً صعباً وخطيراً، لأن العديد من نواتج تحلل 232Th و 233U تُصدر أشعة گاما قوية[161] تُنتج جميع طرق إنتاج 233U شوائب من 232U، إما من تفاعلات الطرد الطفيلية (n،2n) على 232Th، 233Pa، أو 233U، والتي ينتج عنها فقدان نيوترون، أو من عملية التقاط نيوترون مزدوج لـ 230Th، وهي شوائب موجودة في 232Th الطبيعي:[165]
- 23090Th + n → 23190Th + γ 23191Pa ( 22789Ac )
- 23191Pa + n → 23291Pa + γ 23292U
لا يُعد 232U بحد ذاته ضاراً بشكل خاص، لكنه يتحلل بسرعة لينتج 208Tl، وهو نظير قويّ يُصدر أشعة گاما. (يتبع 232Th نفس سلسلة الاضمحلال، لكن عمره النصفي الأطول بكثير يعني أن كميات 208Tl الناتجة ضئيلة للغاية). تجعل هذه الشوائب من 232U، 233U سهل الكشف عنه وخطيراً عند التعامل معه، كما أن صعوبة فصلهما تحدّ من إمكانيات الانتشار النووي باستخدام 233U كمادة انشطارية.[165]
يتمتع 233Pa بعمر نصفي طويل نسبياً يبلغ 27 يوماً، وله مقطع عرضي مرتفع لالتقاط النيوترونات. ولذلك، يُعتبر ساماً للنيوترونات: فبدلاً من أن يتحلل بسرعة إلى 233U المفيد، يتحول جزء كبير من 233Pa إلى 234U ويستهلك النيوترونات، مما يُقلل من كفاءة المفاعل. ولتجنب ذلك، يُستخرج 233Pa من المنطقة النشطة لمفاعلات الملح المنصهر التي تعمل بالثوريوم أثناء تشغيلها، بحيث لا تتاح له فرصة التقاط نيوترون، ويضمحل فقط إلى نظير 233U.[166]
إن تشعيع 232Th بالنيوترونات، متبوعاً بمعالجته، يجب إتقانه قبل أن التحقق من هذه المزايا، وهذا يتطلب تكنولوجيا أكثر تقدماً من دورة وقود اليورانيوم والپلوتونيوم؛[32] ولا تزال الأبحاث جارية في هذا المجال. ويشير آخرون إلى انخفاض الجدوى التجارية لدورة وقود الثوريوم:[167][168][169] تتوقع وكالة الطاقة النووية أن دورة الثوريوم لن تكون مجدية تجارياً طالما أن اليورانيوم متوفر بوفرة - وهو وضع قد يستمر "في العقود القادمة".[170] معظم النظائر المنتجة في دورة وقود الثوريوم ليست من العناصر العابرة لليورانيوم، لكن بعضها لا يزال شديد الخطورة، مثل 231Pa، الذي يبلغ عمره النصفي 32.760 عاماً، وهو مساهم رئيسي في السمية الإشعاعية طويلة الأمد للوقود النووي المستهلك.[166]
المخاطر والآثار الصحية

الإشعاعية
يتحلل الثوريوم الطبيعي ببطء شديد مقارنة بالعديد من المواد المشعة الأخرى، ولا يستطيع الإشعاع المنبعث منه (أشعة ألفا) اختراق جلد الإنسان. نتيجة لذلك، يُعتبر التعامل مع كميات صغيرة من الثوريوم، مثل تلك الموجودة في رتائن الغاز، آمنًا، على الرغم من أن استخدام هذه المواد قد ينطوي على بعض المخاطر.[171] قد يؤدي التعرض لرذاذ الثوريوم، مثل الغبار الملوث، إلى زيادة خطر الإصابة بسرطانات الرئة والپنكرياس والدم، حيث يمكن أن تخترق أشعة ألفا الرئتين والأعضاء الداخلية الأخرى.[171] يؤدي التعرض الداخلي للثوريوم إلى زيادة خطر الإصابة بأمراض الكبد.[172]
تشمل نواتج اضمحلال 232Th نظائر مشعة أكثر خطورة مثل الراديوم والرادون. ورغم أن كمية قليلة نسبياً من هذه النواتج تنتج عن الاضمحلال البطيء للثوريوم، إلا أن التقييم الصحيح للسمية الإشعاعية لـ 232Th يجب أن يشمل مساهمة نواتج اضمحلاله، والتي يُعد بعضها مصادر خطيرة لأشعة گاما،[173] والتي تتراكم بسرعة بعد الاضمحلال الأولي لـ 232Th بسبب غياب النويدات طويلة العمر على امتداد سلسلة الاضمحلال.[174]
نظراً لأن نواتج انبعاثات الثوريوم الخطيرة تتميز بانخفاض درجة انصهارها مقارنة بثاني أكسيد الثوريوم، فإنها تتبخر في كل مرة يتم فيها تسخين الرتينة لاستخدامه. في الساعة الأولى من الاستخدام، تنطلق كميات كبيرة من نواتج انبعاثات الثوريوم، وهي: 224Ra، 228Ra، 212Pb، و 212Bi.[175] معظم جرعة الإشعاع التي يتعرض لها المستخدم العادي تأتي من استنشاق الراديوم، مما يؤدي إلى جرعة إشعاع تصل إلى 0.2 ملي سيڤرت لكل استخدام، أي حوالي ثلث الجرعة التي يتم التعرض لها أثناء تصوير الثدي.[176]
تقدم بعض وكالات السلامة النووية توصيات بشأن استخدام رتائن الثوريوم، وقد أثارت مخاوف تتعلق بالسلامة فيما يتعلق بتصنيعها والتخلص منها؛ فالجرعة الإشعاعية من غطاء واحد ليست مشكلة خطيرة، ولكن الجرعة الإشعاعية من العديد من الرتائن المجمعة معاً في المصانع أو مكبات النفايات تشكل مشكلة.[172]
الحيوية
الثوريوم عديم الرائحة والطعم.[177] السمية الكيميائية للثوريوم منخفضة لأن الثوريوم ومركباته الأكثر شيوعاً (وخاصة ثاني أكسيده) ضعيف الذوبان في الماء،[178] يترسب قبل دخوله الجسم على شكل هيدروكسيد.[179] بعض مركبات الثوريوم سامة كيميائياً بشكل معتدل، خاصة في وجود أيونات قوية مكونة للمركبات المعقدة مثل السترات التي تحمل الثوريوم إلى الجسم في شكل قابل للذوبان.[174] إذا مُضغ الثوريوم أو أُمتص جسم يحتوي عليه، فإنه يفقد 0.4% من الثوريوم و90% من نواتج تحلله الخطيرة إلى الجسم.[122] يتراكم ثلاثة أرباع الثوريوم الذي اخترق الجسم في الهيكل العظمي. الامتصاص عبر الجلد ممكن، لكنه ليس وسيلة محتملة للتعرض.[171] انخفاض ذوبان الثوريوم في الماء يعني أيضاً أن إفرازه عن طريق الكلى والبراز يكون بطيئاً نسبياً.[174]
أظهرت اختبارات امتصاص الثوريوم لدى العاملين في معالجة المونازيت مستوياتٍ من الثوريوم أعلى من الحدود الموصى بها في أجسامهم، لكن لم تُلاحظ أي آثار ضارة على الصحة عند هذه التركيزات المنخفضة نسبياً. ولم تُلاحظ حتى الآن أي سمية كيميائية في القصبة الهوائية والرئتين نتيجة التعرض للثوريوم.[179] الأشخاص الذين يعملون بمركبات الثوريوم عرضة لخطر الإصابة بالتهاب الجلد. وقد يستغرق ظهور الأعراض ما يصل إلى ثلاثين عاماً بعد التعرضة للثوريوم.[49] لا يوجد دور حيوي معروف للثوريوم.[49]
الكيميائية
فلز الثوريوم المسحوق يشتعل تلقائياً: فهو يشتعل تلقائياً في الهواء.[5] عام 1964، صنّفت وزارة الداخلية الأمريكية الثوريوم ضمن المواد "الخطرة" في جدول "اشتعال وانفجار مساحيق الفلزات". وبلغت درجة حرارة اشتعاله 270°س لسحب الغبار، و280°س للطبقات. وبلغ الحد الأدنى لتركيزه المتفجر 0.075 كجم/م³، بينما بلغت طاقة الاشتعال الدنيا للغبار (غير الميكروني) 5 جول/مللي جول.[180]
عام 1956، وقع انفجار شركة سيلڤانيا للمنتجات الكهربائية أثناء إعادة معالجة وحرق حمأة الثوريوم في مدينة نيويورك بالولايات المتحدة. وأصيب تسعة أشخاص، وتوفي أحدهم نتيجة مضاعفات ناجمة عن حروق من الدرجة الثالثة.[181][182][183]
مسارات التعرض
يوجد الثوريوم بكميات ضئيلة جداً في جميع أنحاء الأرض، على الرغم من وجود كميات أكبر في بعض المناطق: يحتوي جسم الإنسان العادي على حوالي 40 ميكروگراماً من الثوريوم، ويستهلك عادةً ثلاثة ميكروگرامات يومياً.[49] يحدث معظم التعرض للثوريوم عن طريق استنشاق الغبار؛ ويأتي بعض الثوريوم مع الطعام والماء، لكن نظراً لانخفاض ذوبانه، فإن هذا التعرض ضئيل للغاية.[174]
تزداد احتمالية التعرض للإشعاع بالنسبة للأشخاص الذين يعيشون بالقرب من رواسب الثوريوم أو مواقع التخلص من النفايات المشعة، وأولئك الذين يعيشون بالقرب من مصانع معالجة اليورانيوم أو الفوسفات أو القصدير أو يعملون فيها، وأولئك الذين يعملون في إنتاج رتائن الغاز.[184] يُعد الثوريوم شائعاً بشكل خاص في المناطق الساحلية لولاية تاميل نادو الهندية، حيث قد يتعرض السكان لجرعة إشعاعية طبيعية أعلى بعشر مرات من المتوسط العالمي.[185] كما أنه شائع في المناطق الساحلية الشمالية للبرازيل، من جنوب باهيا إلى گواراپاري، وهي مدينة بها شواطئ رملية من المونازيت المشع، بمستويات إشعاع تصل إلى 50 ضعفاً من متوسط الإشعاع الخلفي العالمي.[186]
يُعد غبار الثوريوم الناتج عن ميادين اختبار الأسلحة مصدراً محتملاً آخر للتعرض، إذ يُستخدم الثوريوم في أنظمة توجيه بعض الصواريخ. وقد نُسبت إليه نسبة عالية من التشوهات الخلقية والسرطان في سالتو دي كويرا بجزيرة سردينيا الإيطالية.[187]
انظر أيضاً
المصادر
- ^ Bismuth is very slightly radioactive, but its half-life (1.9×1019 years) is so long that its decay is negligible even over geological timespans.
- ^ Behind osmium, tantalum, tungsten, and rhenium;[5] higher boiling points are speculated to be found in the 6d transition metals, but they have not been produced in large enough quantities to test this prediction.[9]
- ^ Gamma rays are distinguished by their origin in the nucleus, not their wavelength; hence there is no lower limit to gamma energy derived from radioactive decay.[30]
- ^ أ ب A fissionable nuclide is capable of undergoing fission (even with a low probability) after capturing a high-energy neutron. Some of these nuclides can be induced to fission with low-energy thermal neutrons with a high probability; they are referred to as fissile. A fertile nuclide is one that could be bombarded with neutrons to produce a fissile nuclide. Critical mass is the mass of a ball of a material which could undergo a sustained nuclear chain reaction.
- ^ The name ionium for 230Th is a remnant from a period when different isotopes were not recognised to be the same element and were given different names.
- ^ Unlike the previous similarity between the actinides and the transition metals, the main-group similarity largely ends at thorium before being resumed in the second half of the actinide series, because of the growing contribution of the 5f orbitals to covalent bonding. The only other commonly-encountered actinide, uranium, retains some echoes of main-group behaviour. The chemistry of uranium is more complicated than that of thorium, but the two most common oxidation states of uranium are uranium(VI) and uranium(IV); these are two oxidation units apart, with the higher oxidation state corresponding to formal loss of all valence electrons, which is similar to the behaviour of the heavy main-group elements in the p-block.[40]
- ^ An even number of either protons or neutrons generally increases nuclear stability of isotopes, compared to isotopes with odd numbers. Elements with odd atomic numbers have no more than two stable isotopes; even-numbered elements have multiple stable isotopes, with tin (element 50) having ten.[10]
- ^ Other isotopes may occur alongside 232Th, but only in trace quantities. If the source contains no uranium, the only other thorium isotope present would be 228Th, which occurs in the decay chain of 232Th (the thorium series): the ratio of 228Th to 232Th would be under 10−10.[22] If uranium is present, tiny traces of several other isotopes will also be present: 231Th and 227Th from the decay chain of 235U (the actinium series), and slightly larger but still tiny traces of 234Th and 230Th from the decay chain of 238U (the uranium series).[22] 229Th is also been produced in the decay chain of 237Np (the neptunium series): all primordial 237Np is extinct, but it is still produced as a result of nuclear reactions in uranium ores.[82] 229Th is mostly produced as a daughter of artificial 233U made by neutron irradiation of 232Th, and is extremely rare in nature.[22]
- ^ Thorianite refers to minerals with 75–100 mol% ThO
2; uranothorianite, 25–75 mol% ThO
2; thorian uraninite, 15–25 mol% ThO
2; uraninite, 0–15 mol% ThO
2.[83] - ^ At the time, the rare-earth elements, among which thorium was found and with which it is closely associated in nature, were thought to be divalent; the rare earths were given atomic weight values two-thirds of their actual ones, and thorium and uranium are given values half of the actual ones.
- ^ The main difficulty in isolating thorium lies not in its chemical electropositivity, but in the close association of thorium in nature with the rare-earth elements and uranium, which collectively are difficult to separate from each other. Swedish chemist Lars Fredrik Nilson, the discoverer of scandium, had previously made an attempt to isolate thorium metal in 1882, but was unsuccessful at achieving a high degree of purity.[101] Lely and Hamburger obtained 99% pure thorium metal by reducing thorium chloride with sodium metal.[102] A simpler method leading to even higher purity was discovered in 1927 by American engineers John Marden and Harvey Rentschler, involving the reduction of thorium oxide with calcium in presence of calcium chloride.[102]
- ^ Thorium also appears in the 1864 table by British chemist John Newlands as the last and heaviest element, as it was initially thought that uranium was a trivalent element with an atomic weight of around 120: this is half of its actual value, since uranium is predominantly hexavalent. It also appears as the heaviest element in the 1864 table by British chemist William Odling under titanium, zirconium, and tantalum. It does not appear in the periodic systems published by French geologist Alexandre-Émile Béguyer de Chancourtois in 1862, German-American musician Gustav Hinrichs in 1867, or German chemist Julius Lothar Meyer in 1870, all of which exclude the rare earths and thorium.[103]
- ^ The filling of the 5f subshell from the beginning of the actinide series was confirmed when the 6d elements were reached in the 1960s, proving that the 4f and 5f series are of equal length. Lawrencium has only +3 as an oxidation state, breaking from the trend of the late actinides towards the +2 state; it thus fits as a heavier congener of lutetium. Even more importantly, the next element, rutherfordium, was found to behave like hafnium and show only a +4 state.[116][117] Today, thorium's similarities to hafnium are still sometimes acknowledged by calling it a "pseudo group 4 element".[118]
- ^ The thirteen fissile actinide isotopes with half-lives over a year are 229Th, 233U, 235U, 236Np, 239Pu, 241Pu, 242mAm, 243Cm, 245Cm, 247Cm, 249Cf, 251Cf, and 252Es. Of these, only 235U have significant amounts in nature, and only 233U and 239Pu can be bred from naturally occurring nuclei with a single neutron capture.[158]
المراجع
- الموسوعة العربية
- معمل لوس الاموس القومي- الثوريوم
- المجمع النووي الأوربي- سلاسل الإضمحلال الطبيعي
- تحضير التيتانيوم, والزركونيوم, والهافيوم, والثوريم van Arkel, A.E., and de Boer, J.H., 1925 : Zeitschrift für Anorganische und Allgemeine Chemie, v. 148, p. 345–350
وصلات خارجية
- الطاقة من الثوريوم
- صفحة المعلومات حول الثوريوم
- شركة طاقة الثوريوم- تطوير وقود الثوريوم
- العناصر على الشبكة- الثوريوم
- أسئلة متكررة- الثوريوم
- الفحص الجيولوجي الأمريكي- الثوريوم
- مركز معلومات اليورانيوم يقدم بعض المواد الأصلية في تركيبه.
- المبرد اللانهائي - مزيل رائحة المجمد, منتج تجاري يفترض أنه يزيل الروائح للأبد مصنوع من Th-232.
- الطاقة من الثوريوم
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (86th ed.). CRC Press. pp. 4–135. ISBN 978-0-8493-0486-6.
- ^ Weast, R. (1984). CRC, Handbook of Chemistry and Physics. Chemical Rubber Company Publishing. p. E110. ISBN 978-0-8493-0464-4.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةArblaster 2018 - ^ Negre, César et al. “Reversed flow of Atlantic deep water during the Last Glacial Maximum.” Nature, vol. 468,7320 (2010): 84-8. doi:10.1038/nature09508
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط Wickleder, Fourest & Dorhout 2006, pp. 61–63.
- ^ Gale, W. F.; Totemeier, T. C. (2003). Smithells Metals Reference Book (in الإنجليزية). Butterworth-Heinemann. pp. 15-2–15-3. ISBN 978-0-08-048096-1.
- ^ أ ب ت ث ج Tretyakov, Yu. D., ed. (2007). Non-organic chemistry in three volumes. Chemistry of transition elements. Vol. 3. Academy. ISBN 978-5-7695-2533-9.
- ^ أ ب ت Johansson, B.; Abuja, R.; Eriksson, O.; et al. (1995). "Anomalous fcc crystal structure of thorium metal". Physical Review Letters. 75 (2): 280–283. Bibcode:1995PhRvL..75..280J. doi:10.1103/PhysRevLett.75.280. PMID 10059654. Archived from the original on 8 March 2023. Retrieved 24 August 2019.
- ^ Fricke, Burkhard (1975). "Superheavy elements: a prediction of their chemical and physical properties". Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. 21: 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9. Retrieved 4 October 2013.
- ^ أ ب ت ث ج ح Audi, G.; Bersillon, O.; Blachot, J.; Wapstra, A.H. (December 2003). "The Nubase evaluation of nuclear and decay properties" (PDF). Nuclear Physics A. 729 (1): 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ de Laeter, John Robert; Böhlke, John Karl; De Bièvre, Paul; Hidaka, Hiroshi; Peiser, H. Steffen; Rosman, Kevin J. R.; Taylor, Philip D. P. (2003). "Atomic weights of the elements. Review 2000 (IUPAC Technical Report)". Pure and Applied Chemistry. 75 (6): 683–800. doi:10.1351/pac200375060683.
- ^ Wieser, M. E. (1 January 2006). "Atomic weights of the elements 2005 (IUPAC Technical Report)". Pure and Applied Chemistry. 78 (11): 2051–2066. doi:10.1351/pac200678112051. S2CID 94552853.
- ^ Nagy, S. (2009). Radiochemistry and Nuclear Chemistry. Vol. 2. EOLSS Publications. p. 374. ISBN 978-1-84826-127-3.
- ^ Griffin, H. C. (2010). "Natural Radioactive Decay Chains". In Vértes, A.; Nagy, S.; Klencsár, Z.; et al. (eds.). Handbook of Nuclear Chemistry. Springer Science+Business Media. p. 668. ISBN 978-1-4419-0719-6.
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (2022-05-04). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry (in الإنجليزية). doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- ^ Beiser, A. (2003). "Nuclear Transformations" (PDF). Concepts of Modern Physics (6 ed.). McGraw-Hill Education. pp. 432–434. ISBN 978-0-07-244848-1. Archived from the original (PDF) on 4 October 2016. Retrieved 4 July 2016.
- ^ "AREVA Med launches production of lead-212 at new facility" (Press release). Areva. 2013. Retrieved 1 January 2017.
- ^ "Mineral Yearbook 2012" (PDF). United States Geological Survey. Retrieved 30 September 2017.
- ^ Ramdahl, Thomas; Bonge-Hansen, Hanne T.; Ryan, Olav B.; Larsen, Åsmund; Herstad, Gunnar; Sandberg, Marcel; Bjerke, Roger M.; Grant, Derek; Brevik, Ellen M.; Cuthbertson, Alan S. (September 2016). "An efficient chelator for complexation of thorium-227". Bioorganic & Medicinal Chemistry Letters. 26 (17): 4318–4321. doi:10.1016/j.bmcl.2016.07.034. PMID 27476138.
- ^ Deblonde, Gauthier J.-P.; Lohrey, Trevor D.; Booth, Corwin H.; Carter, Korey P.; Parker, Bernard F.; Larsen, Åsmund; Smeets, Roger; Ryan, Olav B.; Cuthbertson, Alan S.; Abergel, Rebecca J. (19 November 2018). "Solution Thermodynamics and Kinetics of Metal Complexation with a Hydroxypyridinone Chelator Designed for Thorium-227 Targeted Alpha Therapy". Inorganic Chemistry. 57 (22): 14337–14346. doi:10.1021/acs.inorgchem.8b02430. OSTI 1510758. PMID 30372069. S2CID 53115264.
- ^ Captain, Ilya; Deblonde, Gauthier J.-P.; Rupert, Peter B.; An, Dahlia D.; Illy, Marie-Claire; Rostan, Emeline; Ralston, Corie Y.; Strong, Roland K.; Abergel, Rebecca J. (21 November 2016). "Engineered Recognition of Tetravalent Zirconium and Thorium by Chelator–Protein Systems: Toward Flexible Radiotherapy and Imaging Platforms". Inorganic Chemistry. 55 (22): 11930–11936. doi:10.1021/acs.inorgchem.6b02041. OSTI 1458481. PMID 27802058.
- ^ أ ب ت ث ج ح خ د Wickleder, Fourest & Dorhout 2006, pp. 53–55.
- ^ Bonetti, R.; Chiesa, C.; Guglielmetti, A.; et al. (1995). "First observation of spontaneous fission and search for cluster decay of 232Th". Physical Review C. 51 (5): 2530–2533. Bibcode:1995PhRvC..51.2530B. doi:10.1103/PhysRevC.51.2530. PMID 9970335.
- ^ Yang, H. B.; et al. (2022). "New isotope 207Th and odd-even staggering in α-decay energies for nuclei with Z > 82 and N < 126". Physical Review C. 105 (L051302). Bibcode:2022PhRvC.105e1302Y. doi:10.1103/PhysRevC.105.L051302. S2CID 248935764.
- ^ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ "Standard Atomic Weights: Thorium". CIAAW. 2013.
- ^ Ruchowska, E.; Płóciennik, W. A.; Żylicz, J.; et al. (2006). "Nuclear structure of 229Th". Physical Review C. 73 (4): 044326. Bibcode:2006PhRvC..73d4326R. doi:10.1103/PhysRevC.73.044326. hdl:10261/12130.
- ^ Beck, B. R.; Becker, J. A.; Beiersdorfer, P.; et al. (2007). "Energy splitting in the ground state doublet in the nucleus 229Th". Physical Review Letters. 98 (14): 142501. Bibcode:2007PhRvL..98n2501B. doi:10.1103/PhysRevLett.98.142501. PMID 17501268.
- ^ أ ب von der Wense, L.; Seiferle, B.; Laatiaoui, M.; et al. (2016). "Direct detection of the 229Th nuclear clock transition". Nature. 533 (7601): 47–51. arXiv:1710.11398. Bibcode:2016Natur.533...47V. doi:10.1038/nature17669. PMID 27147026. S2CID 205248786.
- ^ Feynman, R.; Leighton, R.; Sands, M. (1963). The Feynman Lectures on Physics. Vol. 1. Addison-Wesley. pp. 2–5. ISBN 978-0-201-02116-5. Retrieved 13 January 2018.
- ^ أ ب ت "Evaluation of nuclear criticality safety data and limits for actinides in transport" (PDF). Institut de radioprotection et de sûreté nucléaire. p. 15. Archived from the original (PDF) on 10 July 2007. Retrieved 20 December 2010.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش Wickleder, Fourest & Dorhout 2006, pp. 52–53.
- ^ أ ب "3–6: Uranium Thorium Dating" (PDF). Institute for Structure and Nuclear Astrophysics, University of Notre Dame. Archived from the original (PDF) on 21 April 2021. Retrieved 7 October 2017.
- ^ Davis, O. "Uranium-Thorium Dating". Department of Geosciences, University of Arizona. Archived from the original on 28 March 2017. Retrieved 7 October 2017.
- ^ أ ب Rafferty, J. P. (2010), Geochronology, Dating, and Precambrian Time: The Beginning of the World As We Know It, The Geologic History of Earth, Rosen Publishing, p. 150, ISBN 978-1-61530-125-6
- ^ أ ب Vértes, A. (2010), Nagy, S.; Klencsár, Z.; Lovas, R. G. et al., eds., Handbook of Nuclear Chemistry, 5 (2nd ed.), Springer Science+Business Media, p. 800, ISBN 978-1-4419-0719-6
- ^ Wickleder, Fourest & Dorhout 2006, pp. 59–60.
- ^ أ ب ت ث Cotton, S. (2006). Lanthanide and Actinide Chemistry. John Wiley & Sons.
- ^ Martin, W. C.; Hagan, Lucy; Reader, Joseph; Sugar, Jack (July 1974). "Ground Levels and Ionization Potentials for Lanthanide and Actinide Atoms and Ions". Journal of Physical and Chemical Reference Data. 3 (3): 771–780. Bibcode:1974JPCRD...3..771M. doi:10.1063/1.3253147.
- ^ أ ب King, R. Bruce (1995). Inorganic Chemistry of Main Group Elements. Wiley-VCH. ISBN 978-0-471-18602-1.
- ^ Greenwood & Earnshaw 1997, p. 1262.
- ^ أ ب Stoll 2005, p. 6.
- ^ أ ب Hammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics (81st ed.). CRC Press. ISBN 978-0-8493-0485-9.
- ^ أ ب Hyde, E. K. (1960). The radiochemistry of thorium (PDF). National Academy of Sciences. Retrieved 29 September 2017.
- ^ Greenwood & Earnshaw 1997, p. 1264.
- ^ Moore, Robert Lee; Goodall, C. A.; Hepworth, J. L.; Watts, R. A. (May 1957). "Nitric Acid Dissolution of Thorium. Kinetics of Fluoride-Catalyzed Reaction". Industrial & Engineering Chemistry. 49 (5): 885–887. doi:10.1021/ie50569a035.
- ^ أ ب Greenwood & Earnshaw 1997, p. 1267.
- ^ Yamashita, Toshiyuki; Nitani, Noriko; Tsuji, Toshihide; Inagaki, Hironitsu (1997). "Thermal expansions of NpO2 and some other actinide dioxides". J. Nucl. Mater. 245 (1): 72–78. Bibcode:1997JNuM..245...72Y. doi:10.1016/S0022-3115(96)00750-7.
- ^ أ ب ت ث ج ح خ Emsley, J. (2011). Nature's building blocks: an A–Z guide to the elements. Oxford University Press. pp. 544–548. ISBN 978-0-19-960563-7.
- ^ أ ب Wickleder, Fourest & Dorhout 2006, pp. 70–77.
- ^ Greenwood & Earnshaw 1997, p. 1269.
- ^ أ ب ت Ivey, H.F. (1974). "Candoluminescence and radical-excited luminescence". Journal of Luminescence. 8 (4): 271–307. Bibcode:1974JLum....8..271I. doi:10.1016/0022-2313(74)90001-5.
- ^ Wickleder, Fourest & Dorhout 2006, pp. 95–97.
- ^ أ ب ت ث ج Wickleder, Fourest & Dorhout 2006, pp. 78–94.
- ^ أ ب Greenwood & Earnshaw 1997, p. 1271.
- ^ Wickleder, Fourest & Dorhout 2006, pp. 97–101.
- ^ Wickleder, Fourest & Dorhout 2006, pp. 64–66.
- ^ Greenwood & Earnshaw 1997, p. 127.
- ^ أ ب ت ث Wickleder, Fourest & Dorhout 2006, pp. 117–134.
- ^ Persson, I. (2010). "Hydrated metal ions in aqueous solution: How regular are their structures?". Pure and Applied Chemistry. 82 (10): 1901–1917. doi:10.1351/PAC-CON-09-10-22.
- ^ أ ب Greenwood & Earnshaw 1997, pp. 1275–1277.
- ^ أ ب ت Wickleder, Fourest & Dorhout 2006, pp. 101–115.
- ^ Krämer2021-01-04T14:40:00+00:00, Katrina. "Heavy-metal cluster sets size record for metal aromaticity". Chemistry World (in الإنجليزية). Retrieved 2022-07-02.
{{cite web}}: CS1 maint: numeric names: authors list (link) - ^ أ ب ت ث Wickleder, Fourest & Dorhout 2006, pp. 116–117.
- ^ أ ب Greenwood & Earnshaw 1997, pp. 1278–1280.
- ^ Langeslay, Ryan R.; Fieser, Megan E.; Ziller, Joseph W.; Furche, Philip; Evans, William J. (2015). "Synthesis, structure, and reactivity of crystalline molecular complexes of the {[C5H3(SiMe3)2]3Th}1− anion containing thorium in the formal +2 oxidation state". Chemical Science. 6 (6): 517–521. doi:10.1039/C4SC03033H. PMC 5811171. PMID 29560172.
- ^ أ ب ت ث Cameron, A.G.W. (September 1973). "Abundances of the elements in the solar system". Space Science Reviews. 15 (1): 121. Bibcode:1973SSRv...15..121C. doi:10.1007/BF00172440. S2CID 120201972.
- ^ Frebel, Anna; Beers, Timothy C. (January 2018). "The formation of the heaviest elements". Physics Today. 71 (1): 30–37. arXiv:1801.01190. Bibcode:2018PhT....71a..30F. doi:10.1063/pt.3.3815. S2CID 4295865.
- ^ أ ب Roederer, I. U.; Kratz, K.-L.; Frebel, A.; et al. (2009). "The End of Nucleosynthesis: Production of Lead and Thorium in the Early Galaxy". The Astrophysical Journal. 698 (2): 1963–1980. arXiv:0904.3105. Bibcode:2009ApJ...698.1963R. doi:10.1088/0004-637X/698/2/1963. S2CID 14814446.
- ^ Burbidge, E. Margaret; Burbidge, G. R.; Fowler, William A.; Hoyle, F. (1 October 1957). "Synthesis of the Elements in Stars". Reviews of Modern Physics. 29 (4): 547–650. Bibcode:1957RvMP...29..547B. doi:10.1103/RevModPhys.29.547.
- ^ Clayton, D. D. (1968). Principles of Stellar Evolution and Nucleosynthesis. McGraw-Hill Education. pp. 577–591. ISBN 978-0-226-10953-4.
- ^ Helmenstine, Anne (28 June 2022). "Composition of the Universe – Element Abundance". Science Notes and Projects (in الإنجليزية الأمريكية). Archived from the original on 24 May 2024. Retrieved 13 June 2024.
- ^ Stoll 2005, p. 2.
- ^ Greenwood & Earnshaw 1997, p. 1294.
- ^ Albarède, F. (2003). Geochemistry: an introduction. Cambridge University Press. p. 17. ISBN 978-0-521-89148-6.
- ^ Trenn, T. J. (1978). "Thoruranium (U-236) as the extinct natural parent of thorium: The premature falsification of an essentially correct theory". Annals of Science. 35 (6): 581–597. doi:10.1080/00033797800200441.
- ^ Diamond, H.; Friedman, A. M.; Gindler, J. E.; et al. (1956). "Possible Existence of Cm247 or Its Daughters in Nature". Physical Review. 105 (2): 679–680. Bibcode:1957PhRv..105..679D. doi:10.1103/PhysRev.105.679.
- ^ Rao, M. N.; Gopalan, K. (1973). "Curium-248 in the Early Solar System". Nature. 245 (5424): 304–307. Bibcode:1973Natur.245..304R. doi:10.1038/245304a0. S2CID 4226393.
- ^ Rosenblatt, D. B. (1953). "Effects of a Primeval Endowment of U236". Physical Review. 91 (6): 1474–1475. Bibcode:1953PhRv...91.1474R. doi:10.1103/PhysRev.91.1474.
- ^ Gando, A.; Gando, Y.; Ichimura, K.; Ikeda, H.; Inoue, K.; Kibe, Y.; Kishimoto, Y.; Koga, M.; Minekawa, Y.; Mitsui, T.; Morikawa, T.; Nagai, N.; Nakajima, K.; Nakamura, K.; Narita, K.; Shimizu, I.; Shimizu, Y.; Shirai, J.; Suekane, F.; Suzuki, A.; Takahashi, H.; Takahashi, N.; Takemoto, Y.; Tamae, K.; Watanabe, H.; Xu, B. D.; Yabumoto, H.; Yoshida, H.; Yoshida, S.; Enomoto, S.; Kozlov, A.; Murayama, H.; Grant, C.; Keefer, G.; Piepke, A.; Banks, T. I.; Bloxham, T.; Detwiler, J. A.; Freedman, S. J.; Fujikawa, B. K.; Han, K.; Kadel, R.; O'Donnell, T.; Steiner, H. M.; Dwyer, D. A.; McKeown, R. D.; Zhang, C.; Berger, B. E.; Lane, C. E.; Maricic, J.; Miletic, T.; Batygov, M.; Learned, J. G.; Matsuno, S.; Sakai, M.; Horton-Smith, G. A.; Downum, K. E.; Gratta, G.; Tolich, K.; Efremenko, Y.; Perevozchikov, O.; Karwowski, H. J.; Markoff, D. M.; Tornow, W.; Heeger, K. M.; Decowski, M. P. (September 2011). "Partial radiogenic heat model for Earth revealed by geoneutrino measurements". Nature Geoscience. 4 (9): 647–651. Bibcode:2011NatGe...4..647K. doi:10.1038/ngeo1205. Archived from the original on 17 April 2023. Retrieved 3 February 2019.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةCIAAWthorium - ^ Peppard, D. F.; Mason, G. W.; Gray, P. R.; et al. (1952). "Occurrence of the (4n + 1) Series in Nature". Journal of the American Chemical Society. 74 (23): 6081–6084. Bibcode:1952JAChS..74.6081P. doi:10.1021/ja01143a074. Archived from the original on 28 July 2019. Retrieved 3 February 2019.
- ^ أ ب ت ث ج ح خ د ذ Wickleder, Fourest & Dorhout 2006, pp. 55–56.
- ^ Agency for Toxic Substances and Disease Registry (2016). Thorium. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://www.atsdr.cdc.gov/tfacts147.pdf. Retrieved on 30 September 2017. - ^ Emsley, John (25 August 2011). Nature's Building Blocks: An A-Z Guide to the Elements (in الإنجليزية). Oxford University Press. ISBN 978-0-19-257046-8.
- ^ Woodhead, James A.; Rossman, George R.; Silver, Leon T. (1 February 1991). "The metamictization of zircon: Radiation dose-dependent structural characteristics". American Mineralogist. 76 (1–2): 74–82. Archived from the original on 13 April 2023. Retrieved 10 October 2021.
- ^ Szymanski, J. T.; Owens, D. R.; Roberts, A. C.; Ansell, H. G.; Chao, George Y. (1 February 1982). "A mineralogical study and crystal-structure determination of nonmetamict ekanite, ThCa2Si8O20". The Canadian Mineralogist. 20 (1): 65–75. Archived from the original on 24 October 2021. Retrieved 10 October 2021.
- ^ Greenwood & Earnshaw 1997, p. 1255.
- ^ "Tor's Fight with the Giants" (in الإنجليزية). Google Arts & Culture. Retrieved 26 June 2016.
- ^ أ ب Fontani, M.; Costa, M.; Orna, V. (2014). The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. p. 73. ISBN 978-0-19-938334-4.
- ^ Ryabchikov, D. I.; Gol'braikh, E. K. (2013). The Analytical Chemistry of Thorium: International Series of Monographs on Analytical Chemistry. Elsevier. p. 1. ISBN 978-1-4831-5659-0.
- ^ Thomson, T. (1831). A System of Chemistry of Inorganic Bodies. Vol. 1. Baldwin & Cradock and William Blackwood. p. 475.
- ^ Berzelius, J. J. (1824). "Undersökning af några Mineralier. 1. Phosphorsyrad Ytterjord" [Examining some minerals. 1st phosphoric yttria.]. Kungliga Svenska Vetenskapsakademiens Handlingar (in السويدية). 2: 334–338.
- ^ "Xenotime-(Y)". Mindat database. Archived from the original on 16 March 2017. Retrieved 7 October 2017.
- ^ Selbekk, R. S. (2007). "Morten Thrane Esmark". Store norske leksikon (in النرويجية). Kunnskapsforlaget. Archived from the original on 28 April 2021. Retrieved 16 May 2009.
- ^ أ ب Weeks, M. E. (1932). "The discovery of the elements. XI. Some elements isolated with the aid of potassium and sodium: Zirconium, titanium, cerium, and thorium". Journal of Chemical Education. 9 (7): 1231. Bibcode:1932JChEd...9.1231W. doi:10.1021/ed009p1231.
- ^ Berzelius, J. J. (1829). "Untersuchung eines neues Minerals und einer darin erhalten zuvor unbekannten Erde" [Investigation of a new mineral and of a previously unknown earth contained therein]. Annalen der Physik und Chemie (in الألمانية). 16 (7): 385–415. Bibcode:1829AnP....92..385B. doi:10.1002/andp.18290920702. Archived from the original on 27 April 2021. Retrieved 20 July 2009. (modern citation: Annalen der Physik, vol. 92, no. 7, pp. 385–415).
- ^ Berzelius, J. J. (1829). "Undersökning af ett nytt mineral (Thorit), som innehåller en förut obekant jord" [Investigation of a new mineral (thorite), as contained in a previously unknown earth]. Kungliga Svenska Vetenskaps Akademiens Handlingar (in السويدية): 1–30.
- ^ Schilling, J. (1902). "Die eigentlichen Thorit-Mineralien (Thorit und Orangit)" [The actual thoritic minerals (thorite and orangite)]. Zeitschrift für Angewandte Chemie (in الألمانية). 15 (37): 921–929. Bibcode:1902AngCh..15..921S. doi:10.1002/ange.19020153703. Archived from the original on 13 April 2023. Retrieved 24 August 2019.
- ^ Leach, M. R. "The Internet Database of Periodic Tables: Berzelius' Electronegativity Table". Archived from the original on 28 April 2021. Retrieved 16 July 2016.
- ^ Nilson, L. F. (1882). "Über metallisches Thorium" [About metallic thorium]. Berichte der Deutschen Chemischen Gesellschaft (in الألمانية). 15 (2): 2537–2547. doi:10.1002/cber.188201502213. Archived from the original on 13 April 2023. Retrieved 24 August 2019.
- ^ أ ب Meister, G. (1948). Production of Rarer Metals. United States Atomic Energy Commission. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://www.lm.doe.gov/Considered_Sites/F/Foote_Mineral_Co_-_PA_27/PA_27-3.pdf. Retrieved on 22 September 2017. - ^ أ ب ت ث Leach, M. R. "The Internet Database of Periodic Tables". Archived from the original on 24 March 2016. Retrieved 14 May 2012.
- ^ Jensen, William B. (August 2003). "The Place of Zinc, Cadmium, and Mercury in the Periodic Table". Journal of Chemical Education. 80 (8): 952. Bibcode:2003JChEd..80..952J. doi:10.1021/ed080p952.
- ^ أ ب Masterton, W. L.; Hurley, C. N.; Neth, E. J. (2011). Chemistry: Principles and reactions (7th ed.). Cengage Learning. p. 173. ISBN 978-1-111-42710-8.
- ^ Wickleder, Fourest & Dorhout 2006, p. 52.
- ^ Curie, M. (1898). "Rayons émis par les composés de l'uranium et du thorium" [Rays emitted by compounds of uranium and thorium]. Comptes Rendus (in الفرنسية). 126: 1101–1103. OL 24166254M.
- ^ Schmidt, G. C. (1898). "Über die vom Thorium und den Thoriumverbindungen ausgehende Strahlung" [On the radiation emitted by thorium and thorium compounds]. Verhandlungen der Physikalischen Gesellschaft zu Berlin (in الألمانية). 17: 14–16.
- ^ Schmidt, G. C. (1898). "Über die von den Thorverbindungen und einigen anderen Substanzen ausgehende Strahlung" [On the radiation emitted by thorium compounds and some other substances]. Annalen der Physik und Chemie (in الألمانية). 65 (5): 141–151. Bibcode:1898AnP...301..141S. doi:10.1002/andp.18983010512. Archived from the original on 28 April 2021. Retrieved 19 July 2009. (modern citation: Annalen der Physik, vol. 301, pp. 141–151 (1898)).
- ^ Rutherford, E.; Owens, R. B. (1899). "Thorium and uranium radiation". Trans. R. Soc. Can. 2: 9–12.: "The radiation from thorium oxide was not constant, but varied in a most capricious manner", whereas "All the compounds of Uranium give out a radiation which is remarkably constant."
- ^ Simmons, J. G. (1996). The Scientific 100: A Ranking of the Most Influential Scientists, Past and Present. Carol. p. 19. ISBN 978-0-8065-2139-8.
- ^ Fröman, N. (1996). "Marie and Pierre Curie and the Discovery of Polonium and Radium". nobelprize.org. Nobel Media AB. Archived from the original on 7 August 2018. Retrieved 11 May 2017.
- ^ أ ب Burns, M. (1987). Low-Level Radioactive Waste Regulation-Science, Politics and Fear. CRC Press. pp. 24–25. ISBN 978-0-87371-026-8.
- ^ van Spronsen, J. W. (1969). The periodic system of chemical elements. Elsevier. pp. 315–316. ISBN 978-0-444-40776-4..
- ^ Rhodes, R. (2012). The Making of the Atomic Bomb (25th Anniversary ed.). Simon & Schuster. pp. 221–222, 349. ISBN 978-1-4516-7761-4.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةjohnson - ^ Türler, A.; Buklanov, G. V.; Eichler, B.; et al. (1998). "Evidence for relativistic effects in the chemistry of element 104". Journal of Alloys and Compounds. 271–273: 287–291. doi:10.1016/S0925-8388(98)00072-3.
- ^ Kratz, J. V.; Nagame, Y. (2014). "Liquid-Phase Chemistry of Superheavy Elements". In Schädel, M.; Shaughnessy, D. (eds.). The Chemistry of Superheavy Elements (2nd ed.). Springer-Verlag. p. 335. doi:10.1007/978-3-642-37466-1. ISBN 978-3-642-37465-4. S2CID 122675117. Archived from the original on 17 April 2021. Retrieved 21 June 2023.
- ^ أ ب ت ث Furuta, E.; Yoshizawa, Y.; Aburai, T. (2000). "Comparisons between radioactive and non-radioactive gas lantern mantles". J. Radiol. Prot. 20 (4): 423–431. Bibcode:2000JRP....20..423F. doi:10.1088/0952-4746/20/4/305. PMID 11140713. S2CID 7368077.
- ^ New Jersey Department of Health (1996). "Health and hazardous waste" (PDF). A Practitioner's Guide to Patients' Environmental Exposures. 1 (3): 1–8. Archived from the original (PDF) on 15 April 2016.
- ^ Toepker, Terrence P. (1996). "Thorium and yttrium in gas lantern mantles". American Journal of Physics. 64 (2): 109. Bibcode:1996AmJPh..64..109T. doi:10.1119/1.18463.
- ^ أ ب Poljanc, K.; Steinhauser, G.; Sterba, J. H.; et al. (2007). "Beyond low-level activity: on a "non-radioactive" gas mantle". Science of the Total Environment. 374 (1): 36–42. Bibcode:2007ScTEn.374...36P. doi:10.1016/j.scitotenv.2006.11.024. PMID 17270253.
- ^ Kazimi, M. (2003). "Thorium Fuel for Nuclear Energy". American Scientist. Archived from the original on 1 January 2017. Retrieved 29 September 2017.
- ^ Mallapaty, Smriti (9 September 2021). "China prepares to test thorium-fuelled nuclear reactor". Nature. 597 (7876): 311–312. Bibcode:2021Natur.597..311M. doi:10.1038/d41586-021-02459-w. PMID 34504330. S2CID 237471852.
- ^ Majumdar, S.; Purushotham, D. S. C. (1999). Thorium fuel utilization: Options and trends. International Atomic Energy Agency. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://large.stanford.edu/courses/2012/ph241/bordia2/docs/te_1319_web.pdf. Retrieved on 7 October 2017. - ^ "Nuclear Power in India". World Nuclear Association. 2017. Archived from the original on 2024-04-25. Retrieved 29 September 2017.
- ^ "IAEA-TECDOC-1450 Thorium Fuel Cycle – Potential Benefits and Challenges" (PDF). International Atomic Energy Agency. 2005. Archived (PDF) from the original on 4 August 2016. Retrieved 23 March 2009.
- ^ Shippingport Atomic Power Station. "Historic Achievement Recognized: Shippingport Atomic Power Station, A National Engineering Historical Landmark" (PDF). p. 4. Archived from the original (PDF) on 17 July 2015. Retrieved 24 June 2006.
- ^ Friedman, John S. (September 1997). "More power to thorium?". Bulletin of the Atomic Scientists. 53 (5): 19–20. Bibcode:1997BuAtS..53e..19F. doi:10.1080/00963402.1997.11456765.
- ^ "IAEA-TECDOC-1349 Potential of thorium-based fuel cycles to constrain plutonium and to reduce the long-lived waste toxicity" (PDF). International Atomic Energy Agency. 2002. Archived (PDF) from the original on 28 April 2021. Retrieved 24 March 2009.
- ^ Evans, B. (2006). "Scientist urges switch to thorium". ABC News. Archived from the original on 28 March 2010. Retrieved 17 September 2011.
- ^ Martin, R. (2009). "Uranium is So Last Century – Enter Thorium, the New Green Nuke". Wired. Archived from the original on 26 June 2010. Retrieved 19 June 2010.
- ^ Dr. Alfredo Carpineti (16 June 2023) Experimental Molten Salt Nuclear Reactor Gets Go-Ahead In China Archived 2 يوليو 2023 at the Wayback Machine
- ^ "China gives green light to its first thorium-powered nuclear reactor". South China Morning Post. 15 June 2023.
- ^ Weinberg, Alvin (1994). The First Nuclear Era: The life and times of a technological fixer. New York: AIP Press. pp. 36–38. ISBN 978-1-56396-358-2.
- ^ Groves, Leslie R. (1983) [1962]. Now It Can Be Told: The Story of the Manhattan Project. New York: Harper and Co. pp. 180–184. ISBN 0-306-80189-2. Retrieved 18 December 2025.
- ^ أ ب ت "Thorium". World Nuclear Association. 2017. Archived from the original on 8 May 2017. Retrieved 21 June 2017.
- ^ Woods, W.K. (1966) (in en). LRL Interest in U-233. Battelle Memorial Institute. doi:. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://digital.library.unt.edu/ark:/67531/metadc720752/m2/1/high_res_d/79078.pdf. Retrieved on 24 August 2019. - ^ "Classification Bulletin WNP-118" (PDF). U.S. Department of Energy. 12 March 2008. Archived (PDF) from the original on 3 February 2017. Retrieved 13 September 2019.
- ^ Stoll 2005, p. 7.
- ^ United States Geological Survey (2012). "Thorium" (PDF). Archived (PDF) from the original on 29 April 2017. Retrieved 12 May 2017.
- ^ Jayaram, K. M. V. (1987). An Overview of World Thorium Resources, Incentives for Further Exploration and Forecast for Thorium Requirements in the Near Future. Department of Atomic Energy. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://www.iaea.org/inisnkm/nkm/aws/fnss/fulltext/0412_1.pdf. - ^ (in en)Thorium. Statistics and Information. United States Geological Survey. 2017. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://minerals.usgs.gov/minerals/pubs/commodity/thorium/index.html#mcs. Retrieved on 6 January 2018. - ^ أ ب ت ث ج ح خ د Stoll 2005, p. 8.
- ^ أ ب ت ث ج Stoll 2005, p. 32.
- ^ أ ب Stoll 2005, p. 31.
- ^ Matson, Tim (2011). The Book of Non-electric Lighting: The classic guide to the safe use of candles, fuel lamps, lanterns, gaslights, & fire-view stoves. Countryman Press. p. 60. ISBN 978-1-58157-829-4.
- ^ Shaw, J.; Dunderdale, J.; Paynter, R.A. (9 June 2005). "A review of consumer products containing radioactive substances in the European Union" (PDF). NRPB Occupational Services Department. Archived (PDF) from the original on 10 March 2021. Retrieved 21 July 2017.
- ^ ""Negative Ion" Technology—What You Should Know". U.S. Nuclear Regulatory Commission. 28 July 2014. Archived from the original on 8 December 2014. Retrieved 16 June 2021.
- ^ Pridham, G.J. (2016). Electronic Devices and Circuits. The Commonwealth and International Library: Electrical Engineering Division (in الإنجليزية). Elsevier. p. 105. ISBN 978-1-4831-3979-1.
- ^ Stokes, John W. (1982). 70 years of radio tubes and valves: a guide for electronic engineers, historians, and collectors. Vestal, N.Y: Vestal Press. ISBN 978-0-911572-27-8.
- ^ Uttrachi, J. (2015). Weld Like a Pro: Beginning to advanced techniques. CarTech Inc. p. 42. ISBN 978-1-61325-221-5.
- ^ Jeffus, L. (2016). Welding: Principles and Applications. Cengage Learning. p. 393. ISBN 978-1-305-49469-5.
- ^ "Thoriated Camera Lens (ca. 1970s)". Oak Ridge Associated Universities. 2021. Archived from the original on 24 June 2021. Retrieved 11 October 2021.
- ^ Rancourt, J.D. (1996). Optical Thin Films. User Handbook. SPIE Press. p. 196. ISBN 978-0-8194-2285-9.
- ^ Kaiser, N.; Pulker, H. K. (2013). Optical Interference Coatings (in الإنجليزية). Springer. p. 111. ISBN 978-3-540-36386-6.
- ^ Ronen, Yigal (March 2006). "A Rule for Determining Fissile Isotopes". Nuclear Science and Engineering. 152 (3): 334–335. Bibcode:2006NSE...152..334R. doi:10.13182/nse06-a2588. S2CID 116039197.
- ^ أ ب Ronen, Y. (2010). "Some remarks on the fissile isotopes". Annals of Nuclear Energy. 37 (12): 1783–1784. Bibcode:2010AnNuE..37.1783R. doi:10.1016/j.anucene.2010.07.006.
- ^ "Plutonium". World Nuclear Association. 2017. Archived from the original on 5 October 2017. Retrieved 29 September 2017.
- ^ "Uranium 233 Fission". Nuclear Power. 2023. Retrieved 28 April 2023.
- ^ أ ب ت Greenwood & Earnshaw 1997, p. 1259.
- ^ "Interactive Chart of Nuclides". Brookhaven National Laboratory. Archived from the original on 24 January 2017. Retrieved 12 August 2013.
- ^ "Thorium test begins". World Nuclear News. 2013. Archived from the original on 19 July 2013. Retrieved 21 July 2013.
- ^ "IAEA-TECDOC-1450 Thorium Fuel Cycle – Potential Benefits and Challenges" (PDF). International Atomic Energy Agency. 2005. Archived (PDF) from the original on 4 August 2016. Retrieved 23 March 2009.
- ^ أ ب Langford, R. E. (2004). Introduction to Weapons of Mass Destruction: Radiological, Chemical, and Biological. John Wiley & Sons. p. 85. ISBN 978-0-471-46560-7.
- ^ أ ب Nakajima, Ts.; Groult, H. (2005). Fluorinated Materials for Energy Conversion. Elsevier. pp. 562–565. ISBN 978-0-08-044472-7.
- ^ Rees, E. (2011). "Don't believe the spin on thorium being a greener nuclear option". The Guardian. Archived from the original on 27 September 2017. Retrieved 29 September 2017.
- ^ Sovacool, B. K.; Valentine, S. V. (2012). The National Politics of Nuclear Power: Economics, Security, and Governance. Routledge. p. 226. ISBN 978-1-136-29437-2.
- ^ "Nuclear Energy FAQs" (PDF). Argonne National Laboratory. 2014. Archived (PDF) from the original on 7 October 2014. Retrieved 13 January 2018.
- ^ Findlay, T. (2011). Nuclear Energy and Global Governance: Ensuring Safety, Security and Non-proliferation. Routledge. p. 9. ISBN 978-1-136-84993-0.
- ^ أ ب ت "Thorium: Radiation Protection". United States Environmental Protection Agency. August 2000. Archived from the original on 1 October 2006. Retrieved 27 February 2016.
- ^ أ ب "Radioactivity in Lantern Mantles". Australian Radiation Protection and Nuclear Safety Agency. Archived from the original on 14 October 2007. Retrieved 29 September 2017.
- ^ "Natural Decay Series: Uranium, Radium, and Thorium" (PDF). Argonne National Laboratory. 2005. Archived from the original (PDF) on 17 August 2016. Retrieved 30 September 2017.
- ^ أ ب ت ث Stoll 2005, p. 35.
- ^ Luetzelschwab, J. W.; Googins, S. W. (1984). "Radioactivity released from burning gas lantern mantles". Health Phys. 46 (4): 873–881. Bibcode:1984HeaPh..46..873L. doi:10.1097/00004032-198404000-00013. PMID 6706595.
- ^ Huyskens, C. J.; Hemelaar, J. T.; Kicken, P. J. (1985). "Dose estimates for exposure to radioactivity in gas mantles". Sci. Total Environ. 45: 157–164. Bibcode:1985ScTEn..45..157H. doi:10.1016/0048-9697(85)90216-5. PMID 4081711. S2CID 39901914.
- ^ "Toxicological Profile for Thorium" (PDF). Agency for Toxic Substances and Disease Registry U.S. Public Health Service. 1990. p. 4. Archived (PDF) from the original on 21 October 2004. Retrieved 5 September 2016.
- ^ Merkel, B.; Dudel, G. (1988) (in de). Untersuchungen zur radiologischen Emission des Uran-Tailings Schneckenstein. Sächsisches Staatsministerium für Umwelt und Landesentwicklung. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://www.geo.tu-freiberg.de/~merkel/schneckenstein.PDF. - ^ أ ب Stoll 2005, p. 34.
- ^ Jacobson, M.; Cooper, A. R.; Nagy, J. (1964). Explosibility of metal powders. United States Department of the Interior. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. http://apps.dtic.mil/dtic/tr/fulltext/u2/b270510.pdf. Retrieved on 29 September 2017. - ^ "Nine Injured in Atomic Lab Blasts". Pittsburgh Post-Gazette. Associated Press. 1956. p. 2. Archived from the original on 16 March 2020. Retrieved 29 September 2017.
- ^ "No Radiation Threat Seen in A-laboratory Blast". The St. Petersburg Times. Associated Press. 1956. p. 2. Archived from the original on 16 March 2020. Retrieved 29 September 2017.
- ^ Harrington, M. (2003). "Sad Memories of '56 Sylvania Explosion". New York Newsday. Archived from the original on 4 February 2012. Retrieved 29 September 2017.
- ^ "Thorium ToxFAQs" (PDF). Agency for Toxic Substances and Disease Registry. Archived (PDF) from the original on 5 June 2012. Retrieved 29 September 2017.
- ^ "Compendium of Policy And Statutory Provisions Relating To Exploitation of Beach Sand Minerals". Department of Atomic Energy. Archived from the original on 4 December 2008. Retrieved 19 December 2008.
- ^ Pfeiffer, W. C.; Penna-Franca, E.; Ribeiro, C. C.; Nogueira, A. R.; Londres, H.; Oliveira, A. E. (1981). "Measurements of environmental radiation exposure dose rates at selected sites in Brazil". An. Acad. Bras. Ciênc. 53 (4): 683–691. PMID 7345962.
- ^ Alberici, Emma (29 January 2019). "Italian military officials' trial ignites suspicions of links between weapon testing and birth defects in Sardinia". ABC News. Australian Broadcasting Corporation. Archived from the original on 29 January 2019. Retrieved 29 January 2019.
- Short description is different from Wikidata
- WikiProject Elements pages using ENGVAR
- Pages using infobox element with unknown parameters
- Articles with hatnote templates targeting a nonexistent page
- Articles with unsourced statements from March 2023
- All articles with specifically marked weasel-worded phrases
- Articles with specifically marked weasel-worded phrases from November 2022
- عوامل مسرطنة
- Chemical elements with face-centered cubic structure
- وقود نووي
- أكتينيدات
- عناصر كيميائية
- مواد نووية
- CS1 maint: numeric names: authors list
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- CS1 السويدية-language sources (sv)
- CS1 النرويجية-language sources (no)
- CS1 الألمانية-language sources (de)
- CS1 الفرنسية-language sources (fr)

