نقطة الانصهار

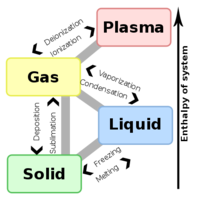
درجة الإنصهار أو درجة الذوبان، وتسمى أيضا بحرارة الانصهار أو الذوبان هي درجة الحرارة التي تتغير فيها حالة مادة ما من الصلابة إلى السيولة.
وفي التغير الحراري في اتجاه النقصان تسمى بدرجة التجمد . وبعض المواد تتصلب دون ان تتبلور اي انها عمليا تظل سائلة ولكن بلزوجة عالية جداً، مثال على ذلك الزجاج. وعند النظر إلى العملية العكسية يرجع إليها على أنها درجة التجمد. فمثلا درجة حرارة الانصهار الزئبق هي 234.32 كلفن (-38.83 °C أو -37.89 °F). وبعض المواد مثل الزجاج يمكن أن تتصلب بدون تبللر, وهذا ما يسمى مادة صلبة لا بلورية.
والمواد المتبلورة تثبت درجة حرارتها عند الانصهار بالرغم من استمرار تدفق الطاقة الحرارية اليها ، ويستمر هذا الثبات إلى حين التحول الكامل إلى الحالة الجديدة ، ويعود ذلك إلى ان فرق الطاقة بين الحالة السائلة والحالة البلورية الصلبة حيث ان ترتيب الذرات في البلورات يتم باقل مستوى ممكن للطاقة ، فيتم امتصاص الطاقة الحرارية من قبل اجزاء المادة التي لم تنصهر بعد، وتظل الحرارة ثابتة حتى الانصهار الكامل ، وتسمى كمية الطاقة اللازمة لتحويل غرام واحد من المادة الصلبة (البلورية) بدرجة حرارة الانصهار (التي يثبت عندها) إلى الحالة السائلة عند نفس درجة الحرارة بالطاقة الكامنة للانصهار.
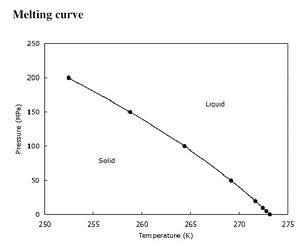
وبخلاف درجة الغليان ، فان تغير الضغط لا يؤثر كثيرا على درجة الانصهار.
والمادة التي تتمتع باعلى درجة انصهار في الضغط الجوي العادي هي الجرافيت بدرجة انصهار 3948 درجة كلفن تقريبا.
الجرافيت هو أكثر المواد المعروفة في درجة الانصهار في الضغط الجوي إذ تبلغ درجة حرارة انصهاره 3948 كيلفن.
درجة حرارة الانصهار يتم استخدامها غالبا لتأكيد نقاء المواد العضوية. وغالبا ما تكون نقطة انصهار المادة النقية أعلى من المادة غير النقية. عند خلط مادتان تكون درجة حرارة الانصهار أقل من درجة انصهار كليهما. ونسبة الخلط التي تحقق أقل درجة حرارة انصهار تسمى نقطة تصلد.
أمثلة
| List of common chemicals | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Chemical[I] | Density (g/cm3) | Melt (K) [1] | Boil (K) | |||||||||
| Water @STP | 1 | 273 | 373 | |||||||||
| Solder (Pb60Sn40) | 456 | |||||||||||
| Cocoa butter | 307.2 | - | ||||||||||
| Paraffin wax | 0.9 | 310 | 643 | |||||||||
| Hydrogen | 0.00008988 | 14.01 | 20.28 | |||||||||
| Helium | 0.0001785 | —[II] | 4.22 | |||||||||
| Beryllium | 1.85 | 1560 | 2742 | |||||||||
| Carbon | 2.267 | —[III][2] | 4000[III][2] | |||||||||
| Nitrogen | 0.0012506 | 63.15 | 77.36 | |||||||||
| Oxygen | 0.001429 | 54.36 | 90.20 | |||||||||
| Sodium | 0.971 | 370.87 | 1156 | |||||||||
| Magnesium | 1.738 | 923 | 1363 | |||||||||
| Aluminium | 2.698 | 933.47 | 2792 | |||||||||
| Sulfur | 2.067 | 388.36 | 717.87 | |||||||||
| Chlorine | 0.003214 | 171.6 | 239.11 | |||||||||
| Potassium | 0.862 | 336.53 | 1032 | |||||||||
| Titanium | 4.54 | 1941 | 3560 | |||||||||
| Iron | 7.874 | 1811 | 3134 | |||||||||
| Nickel | 8.912 | 1728 | 3186 | |||||||||
| Copper | 8.96 | 1357.77 | 2835 | |||||||||
| Zinc | 7.134 | 692.88 | 1180 | |||||||||
| Gallium | 5.907 | 302.9146 | 2673 | |||||||||
| Silver | 10.501 | 1234.93 | 2435 | |||||||||
| Cadmium | 8.69 | 594.22 | 1040 | |||||||||
| Indium | 7.31 | 429.75 | 2345 | |||||||||
| Iodine | 4.93 | 386.85 | 457.4 | |||||||||
| Tantalum | 16.654 | 3290 | 5731 | |||||||||
| Tungsten | 19.25 | 3695 | 5828 | |||||||||
| Platinum | 21.46 | 2041.4 | 4098 | |||||||||
| Gold | 19.282 | 1337.33 | 3129 | |||||||||
| Mercury | 13.5336 | 234.43 | 629.88 | |||||||||
| Lead | 11.342 | 600.61 | 2022 | |||||||||
| Bismuth | 9.807 | 544.7 | 1837 | |||||||||
Notes
| ||||||||||||
قياس نقاط الانصهار
 مقالة مفصلة: Melting point apparatus
مقالة مفصلة: Melting point apparatus
الثرموديناميكا
تحليل DNA
عند الرجوع إلى DNA تكون درجة حرارة الانصهار Tm هي الحرارة التى يكون عندها 50 % من DNA في شكل ثنائي. وبوصف آخر, 50 % من DNA سيكون في شكل شرائط فردية.
انظر أيضاً
- قائمة العناصر حسب نقطة الانصهار
- Phases of matter
- نقطة ثلاثية
- Liquidus temperature
- Slip melting point
- Solidus temperature
الهامش
وصلات خارجية
- Melting and boiling point tables vol. 1 by Thomas Carnelley (Harrison, London, 1885–1887)
- Melting and boiling point tables vol. 2 by Thomas Carnelley (Harrison, London, 1885–1887)