كوريوم
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| صفات عامة | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| الإسم, الرقم, الرمز | كوريوم, Cm, 96 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سلاسل كيميائية | أكتينيدات | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المجموعة, الدورة, المستوى الفرعي | ؟ , 7 , f | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المظهر | فضي | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| كتلة ذرية | (247) g/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| شكل إلكتروني | Rn] 5f7 6d1 7s2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| عدد الإلكترونات لكل مستوى | 2, 8, 18, 32, 25, 9, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| خواص فيزيائية | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الحالة | صلب | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| كثافة عندح.غ. | 13.51 ج/سم³ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الإنصهار | 1613 ك 1340 م ° 2444 ف ° | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الغليان | 3383 ك 3110 م ° 5630 ف ° | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة الإنصهار | kJ/mol ? 15 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخواص الذرية | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| البنية البللورية | سداسي متلاحم | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حالة التأكسد | 3 (أكسيد متردد الخواص) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سالبية كهربية | 1.3 (مقياس باولنج) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| طاقة التأين | الأولي: 581 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| متفرقة | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الترتيب المغناطيسي | no data | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رقم التسجيل | 7440-51-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| النظائر المهمة | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المراجع | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
الكوريوم هو أحد العناصر الاصطناعية الموجودة في الجدول الدوري وله الرمز Cm ورقم ذري 96. وهو عنصر فلزي بعد اليورانيوم ونشيط إشعاعيا من سلسلة الأكتينيدات,يتم إنتاجه بقذف البلوتونيوم بجسيمات ألفا (أيونات الهيليوم) وقد تم تسميته على اسم ماريا سكلودوفسكا كوري وزوجها بيير كوري.
خصائص الكوريوم المميزة
تم تصنيع النظير كوريوم-248 لكميات ضئيلة للغاية لا تتعدى الملي جرامات, ولكن الكوريوم-242 والكوريوم-244 تم تصنيعهم بكميات تصل إلى عدة جرامات, مما أتاح الفرصة للتعرف على بعض خواص العنصر. ويمكن الحصول على كميات معقولة من الكوريوم-244 بتعريض البلوتونيوم لقذائف من النيوترون. ويمكن أن تتواجد كميات قليلة من الكوريوم في اليورانيوم كمنتج ثانوي لاضمحلاله الطبيعي. ولا توجد كثير من التطبيقات التجارية التي يستخدم فيها الكوريوم, ولكن من الممكن مستقبلا أن يستخدم في النظائر المشعة للمولدات الكهروحرارية. يتراكم الكوريوم في خلايا العظام ويدمر إشعاعه لب العظام وهذا يؤدى لتوقف إنتاج خلايا الدم الحمراء.
ومثل العناصر الأرضية النادرة فإن الكوريوم يشبه الجادولينيوم كيميائيا, ولكن له بناء بلوري أكثر تعقيدا. كما أنه نشيط كيميائيا, وهو فلز له لون أبيض فضي وموجب كهربي أكثرمن الألومنيوم (معظم مركبات الكوريوم ثلاثية التكافؤ تميل للاصفرار). الكوريوم-242 يستخدم كمصدر طاقة متنقل وهذا لأنه يمكن أن يولد تقريبا 2 وات من الطاقة الحرارية لكل جرام. كما يستخدم أيضا في منظمات ضربات القلب, ومهمات الفضاء الخارجي.
وقد تم إنتاج عديد من مركبات الكوريوم. ومنها: ثاني أكسيد الكوريوم CmO2, ثالث أكسيد الكوريوم Cm2O3, بروميد الكوريوم CmBr3, كلوريد الكوريوم CmCl3, رباعي فلوريد الكوريوم CmF4, يوديد الكوريوم CmI3.
تاريخ الكوريوم
تم اكتشاف الكوريوم فيجامعة بيركلي بواسطة جيلن تي. سيبورج, رالف إيه. جيمس, ألبرت غيورسو في عام 1944. وقد تم تسميته على اسم ماريا سكلودوفسكا كوري وزوجها بيير كوري, نظرا لأنهم قاما باكتشاف الراديوم ولعملهما المتميز في النشاط الإشعاعي. وقد تم التعرف على العنصر كيميائيا أيضا في معمل أرجون القومي في جامعة شيكاغو. وقد كان العنصر الثالث في سلسلة بعد اليورانيوم الذي يتم اكتشافه رغم أن ترتيبه الثاني في السلسلة. وقد تم الحصول على كوريوم-242 (بفترة عمر نصف تبلغ 163 يوم) ونيترون حر واحد, بقذف جسيمات ألفا على بلوتينيوم-239 في معجل دوراني يبلغ 60 بوصة في بيركلي. وتم الحصول على عينة مرئية من هيدروكسيد الكوريوم-242 بواسطة لويس ويرنر, إيسادور بيرمان في جامعة كاليفورنيا عام 1947 بقذف الأمريكيوم-241 بالنيترونات. وتم الحصول على الكوريوم في شكله العنصري عام 1951.
نظائر الكوريوم
تم التعرف على 19 من النظائر المشعة للكوريوم, وأكثر هذه النظائر استقرارا كوريوم-247 وله فترة عمر نصف تبلغ 1.56 x 107 عام, الكوريوم-248 وله فترة عمر نصف 1.4 x 107 سنة, كوريوم-250 وله فترة عمر نصف تبلغ 9000 سنة, كوريوم-245 وفترة عمر النصف له 8500 سنة. وباقي النظائر لها فترة عمر نصف أقل من 30 سنة, ومعظمها له فترة عمر نصف أقل من 33 يوم. وللكوريوم 4نظائر نووية, وأكثرها استقرارا كوريوم-244 m (t½ 34 ms). وتترواح الكتل الذرية لنظائر الكوريوم من 233.051 وحدة كتل ذرية كوريوم-233 إلى 252.085 وحدة كتل ذرية كوريوم-252.
التخليق
تحضير النظائر
Curium is made in small amounts in nuclear reactors, and by now only kilograms of 242Cm and 244Cm have been accumulated, and grams or even milligrams for heavier isotopes. Hence the high price of curium, which has been quoted at 160–185 USD per milligram,[1] with a more recent estimate at US$2,000/g for 242Cm and US$170/g for 244Cm.[2] In nuclear reactors, curium is formed from 238U in a series of nuclear reactions. In the first chain, 238U captures a neutron and converts into 239U, which via β− decay transforms into 239Np and 239Pu.
-
(the times are half-lives).
(1)
Further neutron capture followed by β−-decay gives americium (241Am) which further becomes 242Cm:
-
.
(2)
For research purposes, curium is obtained by irradiating not uranium but plutonium, which is available in large amounts from spent nuclear fuel. A much higher neutron flux is used for the irradiation that results in a different reaction chain and formation of 244Cm:[3]
-
(3)
Curium-244 alpha decays to 240Pu, but it also absorbs neutrons, hence a small amount of heavier curium isotopes. Of those, 247Cm and 248Cm are popular in scientific research due to their long half-lives. But the production rate of 247Cm in thermal neutron reactors is low because it is prone to fission due to thermal neutrons.[4] Synthesis of 250Cm by neutron capture is unlikely due to the short half-life of the intermediate 249Cm (64 min), which β− decays to the berkelium isotope 249Bk.[4]
-
(4)
The above cascade of (n,γ) reactions gives a mix of different curium isotopes. Their post-synthesis separation is cumbersome, so a selective synthesis is desired. Curium-248 is favored for research purposes due to its long half-life. The most efficient way to prepare this isotope is by α-decay of the californium isotope 252Cf, which is available in relatively large amounts due to its long half-life (2.65 years). About 35–50 mg of 248Cm is produced thus, per year. The associated reaction produces 248Cm with isotopic purity of 97%.[4]
-
(5)
Another isotope, 245Cm, can be obtained for research, from α-decay of 249Cf; the latter isotope is produced in small amounts from β−-decay of 249Bk.
-
(6)
تحضير الفلز
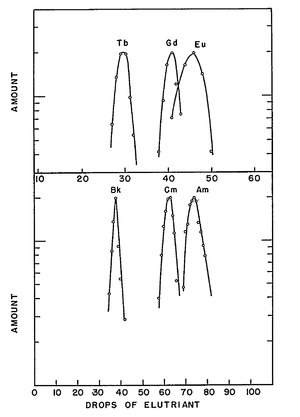
Most synthesis routines yield a mix of actinide isotopes as oxides, from which a given isotope of curium needs to be separated. An example procedure could be to dissolve spent reactor fuel (e.g. MOX fuel) in nitric acid, and remove the bulk of the uranium and plutonium using a PUREX (Plutonium – URanium EXtraction) type extraction with tributyl phosphate in a hydrocarbon. The lanthanides and the remaining actinides are then separated from the aqueous residue (raffinate) by a diamide-based extraction to give, after stripping, a mixture of trivalent actinides and lanthanides. A curium compound is then selectively extracted using multi-step chromatographic and centrifugation techniques with an appropriate reagent.[5] Bis-triazinyl bipyridine complex has been recently proposed as such reagent which is highly selective to curium.[6] Separation of curium from the very chemically similar americium can also be done by treating a slurry of their hydroxides in aqueous sodium bicarbonate with ozone at elevated temperature. Both americium and curium are present in solutions mostly in the +3 valence state; americium oxidizes to soluble Am(IV) complexes, but curium stays unchanged and so can be isolated by repeated centrifugation.[7]
Metallic curium is obtained by reduction of its compounds. Initially, curium(III) fluoride was used for this purpose. The reaction was done in an environment free of water and oxygen, in an apparatus made of tantalum and tungsten, using elemental barium or lithium as reducing agents.[3][8][9][10][11]
Another possibility is reduction of curium(IV) oxide using a magnesium-zinc alloy in a melt of magnesium chloride and magnesium fluoride.[12]
المراجع
- دليل العناصر- الطبعة المنقحة , ألبرت ستيورتا, (طبع جاجمعة أكسفورد; 1998) ISBN 0-19-508083-1
وصلات خارجية
المصادر
- تم ترجمة الصفحة من صفحة ويكيبيديا الإنجليزية .
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةCRC - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةlect - ^ أ ب Morss, L. R.; Edelstein, N. M. and Fugere, J. (eds): The Chemistry of the Actinide Elements and transactinides, volume 3, Springer-Verlag, Dordrecht 2006, ISBN 1-4020-3555-1.
- ^ أ ب ت Lumetta, Gregg J.; Thompson, Major C.; Penneman, Robert A.; Eller, P. Gary (2006). "Curium" (PDF). In Morss; Edelstein, Norman M.; Fuger, Jean (eds.). The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Dordrecht, The Netherlands: Springer Science+Business Media. p. 1401. ISBN 978-1-4020-3555-5. Archived from the original (PDF) on 2010-07-17.
- ^ Penneman, pp. 34–48
- ^ Magnusson D; Christiansen B; Foreman MRS; Geist A; Glatz JP; Malmbeck R; Modolo G; Serrano-Purroy D & Sorel C (2009). "Demonstration of a SANEX Process in Centrifugal Contactors using the CyMe4-BTBP Molecule on a Genuine Fuel Solution". Solvent Extraction and Ion Exchange. 27 (2): 97. doi:10.1080/07366290802672204. S2CID 94720457.
- ^ Penneman, p. 25
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةCM_METALL - ^ Cunningham, B. B.; Wallmann, J. C. (1964). "Crystal structure and melting point of curium metal". Journal of Inorganic and Nuclear Chemistry. 26 (2): 271. doi:10.1016/0022-1902(64)80069-5. OSTI 4667421.
- ^ Stevenson, J.; Peterson, J. (1979). "Preparation and structural studies of elemental curium-248 and the nitrides of curium-248 and berkelium-249". Journal of the Less Common Metals. 66 (2): 201. doi:10.1016/0022-5088(79)90229-7.
- ^ Gmelin Handbook of Inorganic Chemistry, System No. 71, Volume 7 a, transuranics, Part B 1, pp. 67–68.
- ^ Eubanks, I.; Thompson, M. C. (1969). "Preparation of curium metal". Inorganic and Nuclear Chemistry Letters. 5 (3): 187. doi:10.1016/0020-1650(69)80221-7.
