معدن (مغذي)
| جزء من سلسلة عن |
| التمعدن الحيوي |
|---|
 |
عناصر القِلّة أو العناصر الزهيدة Dietary mineral ،هي عناصر تتطلبها الكائنات الحية بكميات قليلة جداً لتأمين حسن سير العمليات الاستقلابية métaboliques، وتتمثل هذه المواد من العناصر معدنية عدة، كالحديد والمنغنيز والبور واليود والكوبالت والموليبدنم وغيرها.[1]
العناصر الكيميائية الأساسية للثدييات
اكتشفت عناصر قلة عدة موجودة على هيئة أثر trace في نسج الكائنات الحية، غير أن بعضها لايمكن الاستغناء عنه بتراكيز محدودة جداً (1 ميلي غرام في كل لتر من الوسط المغذي). ولم يكن من السهل وضع قائمة متكاملة لمعرفة عناصر القلة، لصعوبة تخليص النسج منها كلياً، لمعرفة أثر غيابها في النمو وفي الأفعال الحيوية المختلفة. لكن عمليات الإفقار الحيوي للأوساط المغذية، من خلال تكرار الزراعة في ذات الوسط المغذي، قد نجحت موازنة بالنباتات الدنيا كالفطريات، أما النباتات الراقية فقد يتطلب الأمر تكرار الزراعة ثلاثة أجيال قبل التخلص من هذا العنصر أو ذاك من عناصر القلة، ولهذا يُلجأ إلى زراعة النسج culture des tissues واستخدام المحاليل المغذية ذات التركيب الكيميائي المحدد لمعرفة أهمية عناصر القلة. وقد بينت تلك الدراسات النتائج الآتية:
- وجود ستة عناصر أساسية يتطلبها نمو الكائنات الحية، نباتية كانت أو حيوانية، وهي: الحديد والمنغنيز والتوتياء والنحاس والموليبدن والبور.
- وجود عشرة عناصر في النسج النباتية، على هيئة أثر، ولها أهمية خاصة لدى الحيوان والإنسان، وهي: اليود والكوبالت والسيلينيوم والكروم والنيكل والقصدير والفلور والفاناديوم.
- وجود مجموعة من العناصر الأخرى، في الماء والتربة، تمتصها النباتات بكميات محدودة وتوصلها إلى الكائنات الحية الحيوانية عن طريق السلاسل الغذائية chaines alimentaires، مثل الليثيوم والتيتانيوم والروبيديوم والسيزيوم والسترونسيوم. وتجدر الإشارة هنا إلى احتواء النباتات التي تنمو في مواقع مناجم بعض المعادن، على نسب مرتفعة من عناصر القلة، كما في حال نبات الـميشوفيا كبيرة الزهر Mechovia grandiflora من الفصيلة القطيفية Amaranthacée الذي يركم المنغنيز بنسبة تصل إلى 0.7% في كاتنغا Katanga، كما يركم بعضها الآخر النحاس أو الكوبالت أو اليورانيوم.
| H | He | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Li | Be | B | C | N | O | F | Ne | ||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||
| Cs | Ba | * | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| Fr | Ra | ** | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo | |
| * | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
| ** | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| The four organic basic elements | Quantity elements | Essential trace elements | Suggested function from biochemistry and handling but no identified biological function in humans |
| عنصر القلة | RDA/AI (mg) | الوصف | التصنيف | مغذيات عالية الكثافة المصادر الغذائية |
القصور | الفائض |
|---|---|---|---|---|---|---|
| Potassium | 4700 mg | Quantity | is a systemic electrolyte and is essential in coregulating ATP with sodium. | Legumes, potato skin, tomatoes, bananas, papayas, lentils, dry beans, whole grains, yams, soybeans, spinach, chard, sweet potato, turmeric.[2][3] | hypokalemia | hyperkalemia |
| كلور | 2300 mg | Quantity | is needed for production of hydrochloric acid in the stomach and in cellular pump functions. | Table salt (sodium chloride) is the main dietary source. | hypochloremia | hyperchloremia |
| Sodium | 1500 mg | Quantity | is a systemic electrolyte and is essential in coregulating ATP with potassium. | Table salt (sodium chloride, the main source), sea vegetables, milk, and spinach. | hyponatremia | hypernatremia |
| Calcium | 1300 mg | Quantity | is needed for muscle, heart and digestive system health, builds bone, supports synthesis and function of blood cells. | Dairy products, eggs, canned fish with bones (salmon, sardines), green leafy vegetables, nuts, seeds, tofu, thyme, oregano, dill, cinnamon.[2] | hypocalcaemia | hypercalcaemia |
| Phosphorus | 700 mg | Quantity | is a component of bones (see apatite), cells, in energy processing and many other functions. | Red meat, dairy foods, fish, poultry, bread, rice, oats. [4] [5] In biological contexts, usually seen as phosphate.[6] | hypophosphatemia | hyperphosphatemia |
| Magnesium | 420 mg | Quantity | is required for processing ATP and for bones. | Raw nuts, soy beans, cocoa mass, spinach, chard, sea vegetables, tomatoes, halibut, beans, ginger, cumin, cloves.[7] | hypomagnesemia, magnesium deficiency |
hypermagnesemia |
| Zinc | 11 mg | Trace | is pervasive and required for several enzymes such as carboxypeptidase, liver alcohol dehydrogenase, and carbonic anhydrase. | Calf liver, eggs, dry beans, mushrooms, spinach, asparagus, scallops, red meat, green peas, yoghurt, oats, seeds, miso[2][8] | zinc deficiency | zinc toxicity |
| Iron | 18 mg | Trace | is required for many proteins and enzymes, notably hemoglobin to prevent anemia. Dietary sources include red meat, leafy green vegetables, fish (tuna, salmon), eggs, dried fruits, beans, whole grains, and enriched grains. | Grains, dry beans, eggs, spinach, chard, turmeric, cumin, parsley, lentils, tofu, asparagus, salad greens, soybeans, shrimp, beans, tomatoes, olives[2][9] | anaemia | iron overload disorder |
| Manganese | 2.3 mg | Trace | is a cofactor in enzyme functions. | Spelt grain, brown rice, beans, spinach, pineapple, tempeh, rye, soybeans, thyme, raspberries, strawberries, garlic, squash, eggplant, cloves, cinnamon, turmeric[10] | manganese deficiency | manganism |
| نحاس | 0.900 mg | Trace | is required component of many redox enzymes, including cytochrome c oxidase. | Mushrooms, spinach, greens, seeds, raw cashews, raw walnuts, tempeh, barley[11] | copper deficiency | copper toxicity |
| يود | 0.150 mg | Trace | is required not only for the synthesis of thyroid hormones, thyroxine and triiodothyronine and to prevent goiter, but also, probably as an antioxidant, for extrathyroidal organs as mammary and salivary glands and for gastric mucosa and immune system (thymus): | Sea vegetables, iodized salt, eggs. Alternate but inconsistent sources of iodine: strawberries, mozzarella cheese, yogurt, milk, fish, shellfish.[12] | iodine deficiency | iodism |
| سيلينيوم | 0.055 mg | Trace | a cofactor essential to activity of antioxidant enzymes like glutathione peroxidase. | Brazil nuts, cold water wild fish (cod, halibut, salmon), tuna, lamb, turkey, calf liver, mustard, mushrooms, barley, cheese, garlic, tofu, seeds[13] | selenium deficiency | selenosis |
| Molybdenum | 0.045 mg | Trace | the oxidases xanthine oxidase, aldehyde oxidase, and sulfite oxidase[14] | Tomatoes, onions, carrots[15] | molybdenum deficiency |
تركيزات الدم للمعادن الغذائية
| In the figure, dietary minerals are color highlighted in | purple. |
عناصر أخرى
| العنصر | الوصف | الفائض |
|---|---|---|
| Sulfur | Relatively large quantities of sulfur are required, but there is no RDA,[16] as the sulphur is obtained from and used for amino acids, and therefore should be adequate in any diet containing enough protein. | (primarily associated with compounds) |
| Cobalt | Cobalt is required in the synthesis of vitamin B12, but because bacteria are required to synthesize the vitamin, it is usually considered part of vitamin B12 deficiency rather than its own dietary element deficiency. | Cobalt poisoning |
| Nickel | There have been occasional studies asserting the essentiality of nickel,[17] but it currently has no RDA. | Nickel toxicity |
| Chromium | Chromium has been described as nonessential to mammals.[18][19] Some role in sugar metabolism in humans has been invoked, but evidence is lacking,[20][21] despite a market for the supplement chromium picolinate. | Chromium toxicity |
| Fluorine | Fluorine (as Fluoride) is not generally considered an essential mineral element because humans do not require it for growth or to sustain life. However, if one considers the prevention of dental cavities an important criterion in determining essentiality, then fluoride might well be considered an essential trace element. However, recent research indicates that the primary action of fluoride occurs topically (at the surface).[22][23] | Fluoride poisoning |
| Boron | Boron has been found to be essential for the utilization of vitamin D and calcium in the body.[24] | |
| سترونشيوم | Strontium has been found to be involved in the utilization of calcium in the body. It has promoting action on calcium uptake into bone at moderate dietary strontium levels, but a rachitogenic (rickets-producing) action at higher dietary levels.[25] | Rachitogenic |
| Other | Arsenic, silicon, and vanadium have established, albeit specialized, biochemical roles as structural or functional cofactors in other organisms, and are possibly, even probably, used by mammals (including humans). By contrast, tungsten, bromine, and cadmium have specialized biochemical uses in certain lower organisms, but these elements appear not to be utilized by humans.[26] | Multiple |
الأثر الفيزيولوجي لعناصر القلة في العالمين النباتي والحيواني
لعناصر القلة أثر فيزيولوجي بارز في الوظائف الحيوية النباتية والحيوانية على حد سواء، فالنبات يمد الحيوانات العاشبة herbivores التي تتغذى بالأعشاب بحاجاتها من عناصر القلة بطريقة مباشرة، ويمدّ الحيوانات اللاحمة carnivores، بطريقة غير مباشرة، ويمدّ الكائنات القارتة omnivores؛ التي تتغذى بالنبات والحيوان، وفي طليعتها الإنسان وعدد من الكائنات الأخرى بالطريقتين معاً. ويُعرض فيما يأتي الأثر الفيزيولوجي لأشهر عناصر القلة في عالمي النبات والحيوان.
الأثر الفيزيولوجي لعناصر القلة لدى النبات
تؤكد المعلومات المتوافرة في هذا المجال وجود إجماع على أهمية ستة عناصر، على الأقل، من عناصر القلة لجميع النباتات؛ وهي: الحديد والنحاس والموليبدن والمنغنيز والتوتياء والبور، علماً أن اليود الموجود بكميات وافرة في الطحالب البحرية، لايقوم بأي أثر فيزيولوجي معروف في النباتات، كما أن عنصر السيلينيوم الضروري للحيوانات عامة والمواشي منها خاصة (كالغنم والأبقار والماعز) غير ذي فائدة للنباتات، وإنما تقوم هذه الأخيرة بإيصال هذا العنصر إلى الحيوانات عن طريق العلف. وكذلك الأمر لعنصر الكوبالت الذي لاتحتاجه جميع النباتات غير أنه ضروري جداً لصنع الفيتامين B12 المهم جداً للحيوانات. وتجدر الإشارة إلى أن بعض عناصر الوفرة macro-éléments يمكن أن تقوم ـ في بعض الحالات ـ بأثر مماثل لعناصر القلة من حيث قوة التأثير، كما في حال المغنزيوم والفسفور، على سبيل المثال.
الأثر الفيزيولوجي للحديد
إن حاجة النباتات لعنصر الحديد كبيرة إلى حدٍ ما (10 مغ/ لتر من المحلول المغذي) الأمر الذي يقربه، من حيث التركيز، من عناصر الوفرة، ويرجع ذلك إلى صعوبة إبقاء الحديد على هيئة محلول (إذ يترسب في الأوساط القلوية على هيئة هدروكسيد الحديد Fe (OH)3 وفي مثل هذه الحال لابد من تقديمه على هيئة عوامل كلابيه أو شيلات chelates ويؤدي الحديد أثره الدينامي كأحد أهم عناصر القله لمقدرته على تبديل تكافئه من ثنائي إلى ثلاثي مع تحرير إلكترون أو اقتناصه وفق التفاعل:
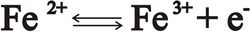
ويتوافر الحديد في مركبات الوساطة catalyseurs الكيميائية الحيوية لتحقيق عمليات الأكسدة والإرجاع oxydoréductions، كما في البروتينات اليحمورية hémoproteines وفي هيموغلوبين الدم، وفي البروتينات الحديدية الكبريتية proteines fer - soufre كالفرودوكسين ferrodoxine وبروتينات عدة التي تتدخل في عملية نقل الإلكترونات خلال عملية التركيب الضوئي photosynthése والتنفس respiration نظراً لتوقف تركيب اليخضور chlorophylle. علماً أن الحديد لا يدخل في تركيب جزيء اليخضور إلا أنه ضروري جداً من أجل صنع اليخضور.
الأثر الفيزيولوجي للنحاس
يتمتع النحاس، كالحديد بقدرة تبديل التكافؤ من أحادي إلى ثنائي وبالعكس، وفق المعادلة:

فيتدخل في عمليات الأكسدة والإرجاع وخاصة في أنزيمات الأكسدة oxydases، التي تتحقق بوجود الأكسجين الجزيء d O2 كما في حال السيتوكروم أكسيداز الضرورية في نهاية السلسلة التنفسية، وكذلك في أنزيمة الفينول أكسيداز المسؤولة عن دوام شرائح البطاطا المتروكة عرضة للهواء الجوي. كما تبين مؤخراً أن النحاس أحد مكونات السوبر أكسيد ديسموتاز superoxyde dismutase (SOD) يسمح بتحطيم شاردة الـ superoxyde (وهي نوع سام من الأكسجين).
الأثر الفيزيولوجي للموليبدن
يوجد الموليبدن على هيئة موليبدات (MoO4-2) وتحتاجه النباتات بتركيز لايتجاوز 0101غ/ لتر، غير أنه لايمكن للنباتات الاستغناء عنه لأثره في عملية إرجاع النترات بوساطة أنزيمه النتراتريدوكتاز nitratreductase التي تعتمد على إمكان الموليبدن تغيير تكافئه من خماسي إلى سداسي التكافؤ وفق المعادلة:
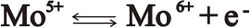
كما يؤثر الموليبدن في عمل أنزيمة النتروجيناز التي تنشط عملية إرجاع الآزوت الجوي.
الأثر الفيزيولوجي للمنغنيز
يقوم المنغنيز بأثر أساسي في عمليات أكسدة وإرجاع عدة؛ وذلك بفضل مقدرته على تغيير تكافئه وفق المعادلة:
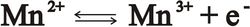
وقد تأكد للباحثين أهمية المنغنيز في عملية إصدار الأكسجين في أثناء التركيب الضوئي، كما تبين وجود 4 ذرات منغنيز في مركز التفاعل للجملة الضوئية الثانية PSII. كما يقوم المنغنيز بأثر في حلمأة hydrolyse الببتيدات، ويؤدي غيابه إلى إصابة النباتات بمرض جرثومي مؤدياً إلى ظهور بقع سوداء مميزة على الأوراق، ولاتظهر هذه البقع في وسط عقيم.
الأثر الفيزيولوجي للتوتياء
تأكدت أهمية التوتياء للفطريات منذ أعمال الفرنسي رولان Raulin عام 1862، ويعد عنصر التوتياء عاملاً مساعداً cofacteur لأنزيمة الالكول ديهيدروجيناز alcool dehydrogenase لأنزيمات أخرى كالـ anhydrase carbonique والفوسفاتاز القلوية phosphatase alcaline والكاربوكسيداز. يؤدي غياب التوتياء في الوسط المغذي إلى اضطرابات في استقلاب هرمون النمو الأكسين auxine، مما يؤدي إلى خلل في النمو، ويبدو ذلك جلياً في الأشجار المثمرة كالتفاح والاجاص والأفوكادو والكاكاو.
الأثر الفيزيولوجي للبور
يتدخل البور على هيئة شاردة البورات (HBO3)-2 التي لابد منها للنباتات (فيما عدا الفطريات)، علماً أن آلية تدخل البورات ليست واضحة تماماً، إلا أن نقص هذا العنصر في الوسط المغذي يُتَرجم باضطرابات في وظيفة النسج القسومة المريستمية وفي تمايز الأعضاء وكذلك في ردود أفعال النباتات تجاه الضوء التي تتحكم فيها الفيتوكرومات، وكذلك في نقل الشوارد المعدنية والسكاكر داخل النبات. ويؤدي غياب الزنك التوتياء إلى نقص في مقاومة النباتات لبعض الأمراض الفطرية، كما في حال مرض لب الشمندر maladie de cueur de la betterave الذي يعد مُشعراًً بنقص البور.
ويضاف إلى العناصر السابقة بعض عناصر القلة الأخرى التي لابد منها لبعض النباتات، كعنصر النيكل Ni الذي تحتاجه الجراثيم في تركيب أنزيمة الـ urease خاصة في الفصيلة القرنية Légumineuses حيث يتدخل في استقلاب نواتج تثبيت الآزوت الجوي. وهناك عنصر الكوبالت Co الذي يدخل في تركيب الكوبالامين cobalaminie أو الفيتامين B12 الضروري جداً لتثبيت الآزوت الجوي بوساطة الجراثيم المتعايشة مع نباتات الفصيلة القرنية، ويؤدي نقص الكوبالت إلى تثبيط تشكل العقد الجذرية . أما الألمنيوم Al فهو العنصر الأكثر انتشاراً في القشرة الأرضية، ويحَسِّن وجوده بتركيز ضعيف نمو بعض النباتات، وكذلك الحال لعنصر السيلينيوم Se الذي يتمتع بخواص قريبة من خواص الكبريت، وهو عنصر ضروري للحيوانات والإنسان كما هو مبين أدناه.
الأثر الفيزيولوجي لعناصر القلة بالنسبة للحيوانات والإنسان
تدخل عناصر القلة في تكوين الأنزيمات التي تسهم في الأعمال الحيوية كافة في النسج الحيوانية وبمقادير قد يصعب قياسها بطرائق التحليل المعتادة، وقد تمكن العلماء من تأكيد أهمية أربعة عشر عنصراً من عناصر القلة للحياة الحيوانية، وهي: الحديد واليود والنحاس والزنك (التوتياء) والمنغنيز والكوبالت والموليبدن والسيلينيوم والكروم والنيكل والقصدير والفلور والفاناديوم والبور.
الأثر الفيزيولوجي للحديد
يدخل الحديد في تركيب خضاب الدم (الهيموغلوبين) hémoglobin الذي يقوم بتثبيت أكسجين الهواء فيتحول إلى أكسي هيموغلوبين oxyhémoglobine حيث ترتبط كل ذرة حديد مع جزيء أكسجين وفق التفاعل:

يعطي هذا المركب الدم اللون الأحمر القاني. غير أن الهيموغلوبين لايثبت الأكسجين إلا عندما يكون ضغط هذا الغاز من رتبة 100 مم زئبق كحد أدنى، علماً أن ضغط الأكسجين في الهواء الجوي يعادل 150مم زئبق، وتتم عملية تثبيت الأكسجين في الرئتين، أما داخل النسج الحيوانية الأخرى حيث تقل نسبة الأكسجين، فإن أكسي هيموغلوبين المؤكسد يتخلى عن أكسجينه ويتحول إلى هيموغلوبين وفق التفاعل:
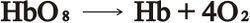
ويصبح لون الدم قاتماً (أحمر بنفسجي)، فالهيموغلوبين مادة غير مستقرة instable تستطيع، عن طريق تفاعل عكوس، أن ترتبط بالأكسجين أو تتخلى عنه داخل النسج وفق التفاعل:

وهذا ما يعطي للحديد دوراً أساسياً عنه في عملية التنفس وأفعال الاستقلاب الأخرى في النسج الحيوانية والإنسانية.
الأثر الفيزيولوجي لليود
يعد اليود من عناصر القله الأساسية لصنع هرمون الدرقين thyroxine الذي تفرزه الغدة الدرقية thyroïde وإن غياب هذا الهرمون أو نقصه يؤدي إلى حفز الغدة النخامية لأن تفرز الهرمون المنشط للدرق، مما يتسبب في تضخمها مؤدياً إلى حال مرضية تعرف بالسلعة البسيطة goitre xérophtalmique، وهي تورم في مقدمة العنق، يترافق بتبلد الذهن وبطء التفكيرـ وقد تؤدي إلى نوع من التخلف العقلي في حال الإصابة به في سن مبكرة. وتلاحظ هذه الظاهرة بكثرة في المناطق الجبلية كما في سويسرا لفقر الماء والنباتات بعنصر اليود وخلو ملح الطعام النقي منه، ولهذا تتم المعالجة بتناول ملح الطعام المشبع باليود وتناول الأسماك البحرية لتأمين الحاجة اليومية والمقدرة بـ 100 ـ 150 ميكروغرام من اليود.
الأثر الفيزيولوجي للزنك
بعد أن كشف النقاب عن أثر الزنك في الخنازير عرفت أهميته؛ إذ لوحظ أن نقص الزنك نتيجة الاستهلاك الضعيف للحوم في بعض مناطق الولايات المتحدة الأمريكية (أقل من 30غ/ يوم) أدى إلى إصابة الأطفال بالهزال ونقص في حاستي الشم والذوق، إضافة إلى تأخر في التئام الجروح، ذلك أن للزنك إسهاماً في تكوّن الحموض النووية والبروتين النوعي في الإنسان، وفي تكوّن المخ في الدماغ، ولهذا لابد من توافره في غذاء المرأة الحامل علماً أن حاجة الإنسان من هذا العنصر لاتتجاوز الثلاثة غرامات طوال حياته. كما تبين أن اضطراب نسبة الزنك إلى النحاس في الغذاء يتسبب في ارتفاع الكولسترول في بلاسما الدم، ومن هنا تأتي أهمية تنوع مصادر الحليب ومشتقاته لاختلاف محتوى نباتات المراعي من هذا العنصر.
الأثر الفيزيولوجي لعناصر القلة الأخرى
يؤدي نقص السيلينيوم Se إلى ضعف النمو والخصب لدى الجنسين، كما يقوم بأثر مهم في الوقاية من مرض نخر الكبد. ويتسبب نقص الكروم في اضطراب استقلاب الأنسولين؛ مما يمهد للإصابة بداء السكري. ويعد عنصر النحاس ضرورة أساسية لإنجاز عمليات الهضم والامتصاص، كما يدخل في تكوين بعض أنزيمات الأكسدة والإرجاع، مما يعزز أثره في العمليات الاستقلابية، كما يسهم في الاستفادة من الحديد لصنع الهيموغلوبين، ويزيد في مناعة الجسم واستقلاب الفيتامينات عدة. ويعد الفلور عنصراً أساسياً لمكافحة تسوس الأسنان. ولابد من توافر الكوبالت لاصطناع الفيتامين B12 الأساسي لتنشيط مختلف الأفعال الحيوية في عالمي الحيوان والإنسان، وخاصة في صنع الهيموغلوبين. ويعد الفاناديوم ضرورياً لأكسدة المركبات الهدروكسيلية مثل الهدروكسي تريبتوفان، وهدروكسي اندول حمض الخل، إضافة إلى تأثيره المضاد لفقر الدم وضرورته لبناء النسج العظمية. وكذلك يدخل الموليبدن في تركيب عدد من الأنزيمات مثل الكزانتين أكسيداز الذي يسهم في أكسدة اليورينات، كما تؤدي زيادته إلى تراكم حمض البول وظهور داء النقرس. وكذلك الحال لبقية عناصر القلة التي توفرها الفواكه والخضار والحبوب الكاملة، كما توفرها الحيوانات التي تتغذى بتلك النباتات من لحوم الغنم والبقر والطيور الداجنة والأسماك وثمار البحر.
ولابد من الإشارة إلى أن بعض عناصر الوفرة الضرورية لبناء النسج الحيوانية كالكالسيوم والفسفور الضرورية لبناء عظام الحيوانات يمكنها أن تقوم بأثر عناصر القلة في بعض الحالات وبتركيز ضعيف جداً كما هي الحال بالنسبة للكالسيوم والمغنزيوم والكبريت والفسفور التي تتدخل في تنظيم عمليات الاستقلاب واستجابة العضلات والأعصاب ومحاربة التشنجات وغيرها من الأفعال الفيزيولوجية الأساسية للحياة.
المصادر
- ^ "عناصر القِلّة". الموسوعة العربية. Retrieved 2012-09-01.
- ^ أ ب ت ث Adam Drewnowski (2010). "The Nutrient Rich Foods Index helps to identify healthy, affordable foods" (PDF). The American Journal of Clinical Nutrition. 91(suppl): 1095S-1101S.
- ^ "Human Nutrition: Potassium". George Mateljan Foundation. 2009.
- ^ "NHS Choices:Vitamins and minerals - Others". Retrieved November 08, 2011.
{{cite web}}: Check date values in:|accessdate=(help) - ^ Corbridge, D. E. C. (1995-02-01). Phosphorus: An Outline of Its Chemistry, Biochemistry, and Technology (5th ed.). Amsterdam: Elsevier Science Pub Co. p. 1220. ISBN 0-444-89307-5.
- ^ "Linus Pauling Institute at Oregon State University". Retrieved 2008-11-29.
- ^ "Human Nutrition: Magnesium". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Zinc". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Iron". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Manganese". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Copper". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Iodine". George Mateljan Foundation. 2009.
- ^ "Human Nutrition: Selenium". George Mateljan Foundation. 2009.
- ^ Sardesai VM (1993). "Molybdenum: an essential trace element". Nutr Clin Pract. 8 (6): 277–81. doi:10.1177/0115426593008006277. PMID 8302261.
{{cite journal}}: Unknown parameter|month=ignored (help) - ^ "Human Nutrition: Selenium". George Mateljan Foundation. 2009.
- ^ "NSC 101 Chapter 8 Content". Retrieved 2008-12-02. [dead link]
- ^ Anke M, Groppel B, Kronemann H, Grün M (1984). "Nickel--an essential element". IARC Sci. Publ. (53): 339–65. PMID 6398286.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ K. R. Di Bona, S. Love, N. R. Rhodes, D. McAdory, S. H. Sinha, N. Kern, J. Kent, J. Strickland, A. Wilson, J. Beaird, J. Ramage, J. F. Rasco, J. B. Vincent "Chromium is not an essential trace element for mammals: effects of a "low-chromium" diet." Journal Biological Inorganic Chemistry, 2011, volume 16, p. 381-90. doi:10.1007/s00775-010-0734-y
- ^ Eastmond DA, Macgregor JT, Slesinski RS (2008). "Trivalent chromium: assessing the genotoxic risk of an essential trace element and widely used human and animal nutritional supplement". Crit. Rev. Toxicol. 38 (3): 173–90. doi:10.1080/10408440701845401. PMID 18324515.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ John B. Vincent "Chromium: celebrating 50 years as an essential element?" Dalton Transactions, 2010, pp. 3787-3794. doi:10.1039/B920480F
- ^ Stearns DM (2000). "Is chromium a trace essential metal?". BioFactors. 11 (3): 149–62. doi:10.1002/biof.5520110301. PMID 10875302.
- ^ Cerklewski FL (1998). "Fluoride--essential or just beneficial". Nutrition. 14 (5): 475–6. doi:10.1016/S0899-9007(98)00023-9. PMID 9614319.
{{cite journal}}: Unknown parameter|month=ignored (help) - ^ "Linus Pauling Institute at Oregon State University". Retrieved 2008-11-29.
- ^ "Boron in human and animal nutrition". Retrieved 2010-10-06.
- ^ "The biological role of strontium". Retrieved 2010-10-06.
- ^ Ultratrace minerals. Authors: Nielsen, Forrest H. USDA, ARS Source: Modern nutrition in health and disease / editors, Maurice E. Shils ... et al.. Baltimore : Williams & Wilkins, c1999., p. 283-303. Issue Date: 1999 URI: [1]
