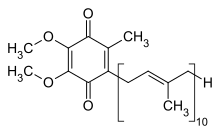
مساعد الإنزيم Q10
| |
| الأسماء | |
|---|---|
| اسم أيوپاك المفضل
2-[(2E,6E,10E,14E,18E,22E,26E,30E,34E)-3,7,11,15,19,23,27,31,35,39-Decamethyltetraconta-2,6,10,14,18,22,26,30,34,38-decaen-1-yl]-5,6-dimethoxy-3-methylcyclohexa-2,5-diene-1,4-dione | |
| أسماء أخرى
أوبيكينون، أوبيدكارنون، مساعد الإنزيم Q، CoQ10، /ˌkoʊˌkjuːˈtɛn/, CoQ، Q10، فيتامين Q
| |
| المُعرِّفات | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.005.590 |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C59H90O4 |
| كتلة مولية | 863.32 g mol-1 |
| المظهر | مادة صلبة صفراء أو برتقالية |
| نقطة الانصهار | |
| قابلية الذوبان في الماء | غير قابل للذوبان |
| علم الأدوية | |
| C01EB09 (WHO) | |
| مركبات ذا علاقة | |
الكينونات ذات العلاقة
|
1,4-بنزوكينون بلاستوكينون Ubiquinol |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
مساعد الإنزيم Q (Coenzyme Q)، يُعرف أيضاً باسم أوبيكينون (ubiquinone)، يُسوق باسم CoQ10)، هي فئة من مساعدات الإنزيم واسعة الانتشار في الحيوانات ومعظم الجراثيم (ومن ثم سُميت أوبيكينون). في البشر، الشكل الأكثر شيوعاً منها هو مساعد الإنزيم Q10 أو أوبيكينون-10.
وهي عبارة عن 1,4-بنزوكينون (1,4-benzoquinone)، حيث يشير Q إلى مجموعة الكينون الكيميائية، ويشير الرقم 10 إلى عدد الوحدات الفرعية الكيميائية الإيزوبرينية في ذيلها. في الأوبيكينونات الطبيعية، يمكن أن يكون العدد في أي مكان من 6 إلى 10. هذه الفئة من المواد القابلة للذوبان في الدهون، والتي تشبه الفيتامينات، موجودة في جميع الخلايا التنفسية لحقيقيات النوى، وبشكل أساسي في خلايا الميتوكوندريا. وهي إحدى مكونات سلسلة نقل الإلكترون وتشارك في التنفس الخلوي الهوائي، والذي يولد الطاقة على شكل أدينوزين ثلاثي الفوسفات. خمسة وتسعين في المائة من طاقة جسم الإنسان تُولد بهذه الطريقة.[1][2] الأعضاء التي تتطلب أعلى مستوى من الطاقة - مثل القلب والكبد والكلى - تمتلك أعلى تركيزات CoQ10.[3][4][5]
هناك ثلاثة حالات لتفاعلات الأكسدة-الاختزال لمركب CoQ: الأكسدة الكاملة (أوبيكينون)، سميكينون (أوبيسميكينون)، والاختزال الكامل (أوبيكوينول). تعد قدرة هذا الجزيء على العمل كناقل ثنائي الإلكترون (يتحرك بين شكل الكينون والكينول) وحامل إلكترون واحد (يتحرك بين السيميكينون وأحد هذه الأشكال الأخرى) أمرًا أساسيًا لدوره في سلسلة نقل الإلكترون بسبب كتلة الحديد-الكبريت التي لا تقبل إلا إلكترونًا واحدًا في كل مرة، وباعتبارها مضادات أكسدة-كاسحة حرة الجذور.
النقص والسمية
هناك مساران رئيسيان لنقص CoQ10 في البشر: تقليل التخليق الحيوي، وزيادة استخدام الجسم له. التخليق الحيوي هو المصدر الرئيسي لمساعد الإنزيم CoQ10. يتطلب التخليق الحيوي ما لا يقل عن 12 جين، والطفرات في العديد منها تسبب نقص CoQ. قد تتأثر مستويات CoQ10 أيضًا بعيوب جينية أخرى (مثل طفرات دنا المتقدرة، ETFDH، APTX، FXN، وBRAF، جينات لا ترتبط ارتباطًا مباشرًا بعملية التخليق الحيوي لمساعد الإنزيم CoQ10. بعض هذه الطفرات، مثل الطفرات في "COQ6"، يمكن أن تؤدي إلى أمراض خطيرة مثل المتلازمة الكلوية المقاومة للسترويد مع الصمم الحسي العصبي.
أبلغ عن بعض الآثار الجانبية، معظمها في الجهاز الهضمي، مع تناول كميات كبيرة جدًا من CoQ10. أشارت طريقة تقييم المخاطر ذات المستوى الآمن (OSL) إلى أن دليل السلامة قوي عند تناول ما يصل إلى 1200 ملجم/يومياً، ويتم تحديد هذا المستوى على أنه مستوى المخاطر الآمن.[6]
التقييم
على الرغم من إمكانية قياس CoQ10 في بلازما الدم، إلى أن هذه القياسات تعكس الامتصاص الغذائي وليس حالة الأنسجة. حالياً، تقيس معظم المراكز السريرية مستويات CoQ10 في الخلايا الليفية اليافعة الجلدية المستزرعة، خزعة العضلات، وخلايا الدم وحيدة النواة.[7] يمكن أيضًا استخدام الخلايا الليفية المستزرعة لتقييم معدل التخليق الحيوي الداخلي لمساعد الإنزيم Q10، عن طريق قياس امتصاص 14C-labelled p-hydroxybenzoate.[8]
الستاتينات
أقترح أن سمية العضلة الهيكلية من الستاتينات ترجع إلى ضعف في التخليق الحيوي لمساعد الإنزيم CoQ، لكن الأدلة الداعمة لذلك اعتبرت مثيرة للجدل عام 2011.[7]
بينما تقوم الستاتينات باختزال مساعد الإنزيم Q10 في الدم، فليس واضحاً ما إذا كانت تختزل مساعد الإنزيم Q10 في العضلات.[9] لا تدعم الأدلة أن المكملات تحسن الآثار الجانبية للستاتينات.[9] ومع ذلك، خلص التحليل الشمولي الأحدث الذي أُجري في الصين، وهي أحد أكبر منتجي هذا المكمل في العالم، إلى أن "مكملات CoQ10 قد حسنت SAMS، مما يعني أن مكملات CoQ10 قد تكون نهجًا تكميليًا لتحسين الاعتلال العضلي الناجم عن الستاتينات."[10]
المكملات الغذائية
التنظيم والتركيب
لم يُعتمد CoQ10 من قبل إدارة الغذاء والدواء الأمريكية لعلاج أي حالة طبية.[11][12] ومع ذلك، يباع كمكمل غذائي باسم UbiQ 300 وUbiQ 100، ولا يخضع لنفس لوائح الأدوية الطبية، كما يدخل لمكون في بعض مستحضرات التجميل.[13][14] تصنيع CoQ10 غير منظم، وقد تختلف التوليفات والعلامات التجارية بشكل كبير::[11] خلص تحليل معملي عام 2004 أجراه ConsumerLab.com إلى أن مكملاتCoQ10 التي تباع في الولايات المتحدة لا تحتوي على الكميات المدرجة على الملصق. تترواح من كميات لا تذكر من CoQ10، حتى أقل 75% من الجرعة المذكورة، وصولاً إلى 75% منها.[15][16]
بشكل عام، يمكن تحمل CoQ10 بشكل جيد. ومن أبرز الآثار الجانبية له أعراض الجهاز الهضمي (الغثيان، القيء، فقدان الشهية، والمغص)، الطفح الجلدي، والصداع.[17]
بينما لا توجد جرعة مثالية ثابتة من CoQ10، فإن الجرعة اليومية النموذجية هي 100-200 مليجرام. تحتوي التركيبات المختلفة على كميات معلنة متفاوتة من CoQ10 ومكونات أخرى.
أمراض القلب
وجدت مراجعة كوكرين لعام 2014 أدلة غير كافية للتوصل إلى استنتاج حول استخدام مساعد الإنزيم Q10 للوقاية من أمراض القلب.[18] وخلصت مراجعة كوكرين لعام 2016 إلى أن CoQ10 ليس لديه أي تأثير على ضغط الدم.[19] وفي مراجعة كوكرين لعام 2021، اتضح أنه "ليس هناك دليل مقنع يدعم أو ينفي" استخدام CoQ10 لعلاج قصور القلب.[20]
في تحليل شمولي لعام 2017 وُجد، شمل عينة لأشخاص مصابين بقصور القلب، تم إعطائهم جرعات 30-100 ملج/يومياً من CoQ10، مما أدى إلى انخفاض معدل الوفيات بينهم إلى 31. كما ارتفعت قدرتهم على ممارسة الرياضة. لم يُعثر على فرق كبير في نقاط نهاية الجزء المقذوف للقلب الأيسر وتصنيف جمعية القلب في نيويورك.[21]
الصداع النصفي
بحسب إرشادات الجمعية الملكية للصداع، بناء على أدلة منخفضة الجودة، أنه من أجل الوقاية من الصداع النصفي، يوصى بتناول جرعة 300 مجم CoQ10 كخيار وقائي.[22]
الاعتلال العضلي الستاتيني
استخدم CoQ10 بشكل روتيني لعلاج انهيار العضلات كأثر جانبي لاستخدام الستاتينات. عام 2015، وجد تحليل شمولي من تجربة منضبطة معشاة أن CoQ CoQ10 ليس له أي تأثير على الاعتلال العضلي المرتبط بالستاتينات.[23] خلص تحليل شمولي عام 2018 إلى أن هناك دليل أولي عن أن تناول جرعات فموية من CoQ10 تحد من أعراض الاعتلال العضلي المرتبط بالستاتينات، بما في ذلك آلام العضلات، ضعف العضلات، التشنج العضلي والإرهاق العضلي.[10]
السرطان
اعتبارًا من 2014 لم تُجرى تجارب سريرية كبيرة على CoQ10 في علاج السرطان.[11] حدد المعهد الوطني للسرطان في الولايات المتحدة مشكلات في الدراسات الصغيرة القليلة التي أجريت، مشيرًا إلى أن "الطريقة التي أجريت بها الدراسات وكمية المعلومات التي أبلغ عنها جعلت من غير الواضح ما إذا كانت الفوائد ناتجة عن CoQ10 أو شيء آخر".[11] وخلصت الجمعية الأمريكية للسرطان إلى أن "CoQ10 قد يقلل من فاعلية العلاج الكيميائي والإشعاعي، لذا يوصي معظم أطباء الأورام بتجنبه أثناء علاج السرطان".[24]
أمراض الأسنان
وجدت دراسة مراجعة أجريت عام 1995 أنه لا توجد فائدة سريرية لاستخدام CoQ10 في علاج أمراض اللثة.[25] كانت معظم الدراسات التي تشير إلى خلاف ذلك قديمة، وركزت على الاختبارات المعملية،[26][27][28] والتي كان لديها عدد قليل جدًا من موضوعات الاختبار و/أو المنهجية الإحصائية الخاطئة وإعداد التجربة،[29][30] أو كانت تحت رعاية مصنعي المنتج.[31]
أمراض الكلى المزمنة
عام 2019 اقترحت إحدى المراجعات دراسة تأثيرات CoQ10 على المصابين بأمراض الكلى المزمنة.[32]
الاستخدامات الإضافية
استخم الإنزيم المساعد Q10 أيضًا كمكون نشط في مستحضرات التجميل وكمكون غير نشط في تركيبات الواقي الشمسي. عند استخدامه موضعيًا في منتجات العناية بالبشرة، فإنه يظهر بعض القدرة على تقليل الإجهاد التأكسدي في الجلد،[33] ويؤخر علامات شيخوخة الجلد الجوهرية، وعكس علامات شيخوخة الجلد الخارجية،[34][35] ويساعد في الاشي خلل التصبغ،[36][37] وزيادة استقرار بعض المواد الفعالة الواقية من الشمس،[38] وزيادة عامل الحماية للواقيات الشمسية،[39] ويوفر بعض الحماية من الأشعة تحت الحمراء للواقيات الشمسية.[40][41] تظهر الكثير من الأبحاث حول فوائد اليوبيكينون للبشرة أنه يعمل بشكل تآزري مع مضادات الأكسدة الموضعية الأخرى لتحسين البشرة ومستحضرات التجميل.
التداخلات الدوائية
لمساعد الإنزيم Q10 تأثيرات محتملة في تثبيت تأثير التيوفيلين وكذلك الوارفارين المضاد للتخثر؛ قد يتداخل مساعد الإنزيم Q10 مع آلية عمل الوارفارين من خلال التفاعل مع إنزيمات سيتوكروم p450 وبالتالي تقليل زمن البروثرومبين INR، وهو مقياس لتخثر الدم.[42] بُنية مساعد الإنزيم Q10 تشبه إلى حد كبير بُنية فيتامين ك التي تتنافس مع تأثيرات الوارفارين المضادة لتخثر الدم وتتصدى لها. يجب تجنب مساعد الإنزيم Q10 للمرضى الذين يتناولون الوارفارين بسبب زيادة خطر التخثر.[17]
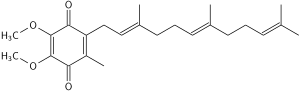
الخصائص الكيميائية
البنية المؤكسدة لمساعد إنزيم CoQ10 موضحة أعلان. يمكن تمييز الأنواع المختلفة من الإنزيم المساعد Q بعدد الوحدات الفرعية الإيزوبرينية في السلاسل الجانبية. الإنزيم المساعد Q الأكثر شيوعًا في الميتوكوندريا البشرية هو CoQ10. يشير حرف Q إلى رأس الكينون ويشير الرقم 10 إلى عدد مرات تكرار الإيزوبرين في الذيل. يحتوي الجزيء أدناه على ثلاث وحدات متساوية الشكل ويسمى Q3.
في حالته النقية، يكون CoQ10 على شكل مسحوق دهني برتقالي اللون، وليس له طعم ولا رائحة.[43]
التخليق الحيوي
يحدث التخليق الحيوي في معظم الأنسجة البشرية. هناك ثلاث خطوات رئيسية:
- إنشاء بنية بنزوكينون (باستخدام الفنايلألانين أو التايروسين، عبر 4-هيدروكسي بنزوات)
- تخليق السلسلة الجانبية للإيزوبرين (باستخدام acetyl-CoA)
- ضم أو تكثيف البنيتين المذكورتين أعلاه
يحدث التفاعلان الأوليان في الميتوكوندريا، والشبكة الإندوبلازمية، والبيروكسيومات، مما يشير إلى مواقع متعددة للتخليق في الخلايا الحيوانية..[44]
هناك إنزيم هام في هذا المسار هو مختزل HMG-CoA، وعادة ما يكون هدفًا للتدخل في مضاعفات القلب والأوعية الدموية. "الستاتينات" المخفضة للكوليسترول تمنع إنزيم HMG-CoA. أحد الآثار الجانبية المحتملة للستاتينات هو انخفاض إنتاج CoQ10، والذي قد يكون مرتبطًا بتطور الاعتلال العضلي وانحلال الربيدات. ومع ذلك، فإن الدور الذي تلعبه الستاتينات في نقص CoQ مثير للجدل. على الرغم من أن هذه الأدوية تقلل مستويات CoQ في الدم، إلا أن الدراسات حول تأثيرات مستويات CoQ في العضلات لم تضح بعد. لا تقلل مكملات CoQ أيضًا من الآثار الجانبية للستاتينات.[7][9]
تتضمن الجينات المسئولة PDSS1، PDSS2، COQ2، وADCK3 (COQ8، CABC1).[45]
تستخدم العضيات بخلاف البشر مواد كيميائية مختلفة نوعًا ما من المصادر لإنتاج بنية البنزوكينون والأيزوبرين. على سبيل المثال، بكتيريا الإشريشيا المعوية تنتج الأول من الكوريسمات والأخير من مصدر غير الميفالونات. على الرغم من ذلك، تُخلق خميرة الجعة الشائعة الأول من الكوريسمات أو التايروسين والأخير من الميفالونات. تشترك معظم العضيات في الوسيط الشائع 4-هيدروكسي بنزوات، لكن مرة أخرى تستخدم خطوات مختلفة للوصول إلى بنية "Q".[46]
الامتصاص والأيض
الامتصاص
CoQ10 هو مسحوق بلوري غير قابل للذوبان في الماء. يتبع في امتصاصه نفس عملية امتصاص الدهون؛ يبدو أن آلية امتصاصه مشابهة لتلك الخاصة بفيتامين هـ، وهو عنصر غذائي آخر قابل للذوبان في الدهون. تتضمن هذه العملية في جسم الإنسان إفرازه في الأمعاء الدقيقة من إنزيم البنكرياس والعصارة الصفراوية، مما يسهل الاستحلاب والمذيلة المطلوبين لامتصاص المواد المحبة للدهون.[47] يحفز تناول الطعام (ووجود الدهون) إفراز القناة الصفراوية في الجسم للأحماض الصفراوية ويعزز بشكل كبير امتصاص CoQ10. يُمتص CoQ10 الخارجي من الأمعاء الدقيقة ويتم امتصاصه بشكل أفضل إذا تم تناوله مع الوجبة. يكون تركيز CoQ10 في مصل الدم في حالة تناول الطعام أعلى منه في حالات الصيام.[48][49]
الأيض
البيانات الخاصة بأيض CoQ10 في الحيوانات والبشر محدودة .[50] أظهرت دراسة أجريت على CoQ10 14C-labeled على الجرذان، أن معظم النشاط الإشعاعي يحدث في الكبد بعد ساعتين من تناوله عن طريق الفم عندما لوحظ ذروة النشاط الإشعاعي للبلازما، لكن CoQ10 (مع 9 وحدات إيزوبرينيل فقط) هو الشكل السائد من مساعد الإنزيم Q في الجرذان.[51] أظهرت الدراسة أن CoQ10 يستقلب في جميع الأنسجة، بينما المسار الرئيسي للتخلص منه هو إخراجه في العصارة الصفراوية والبراز. بعد إيقاف مكملات CoQ10، تعود المستويات إلى وضعها الطبيعي في غضون أيام قليلة، بغض النظر عن نوع التركيبة المستخدمة.[52]
الحركية الدوائية
نُشرت بعض التقارير حول الحرائك الدوائية لمساعد الإنزيم CoQ10. يمكن ملاحظة ذروة البلازما بعد 2-6 ساعات من تناوله عن طريق الفم، اعتمادًا بشكل أساسي على تصميم الدراسة. في بعض الدراسات، لوحظت ذروة البلازما الثانية أيضًا في حوالي 24 ساعة بعد تناوله، وربما يرجع ذلك إلى إعادة التدوير المعوي الكبدي وإعادة التوزيع من الكبد إلى الدورة الدموية.[47] استخدم تومونو وزملائه CoQ10 البلوري المسمى بالديوتيريوم للتحقيق في الحرائك الدوائية لدى البشر وتحديد العمر النصفي للتخلص من الدواء 33 ساعة.[53]
تحسين التوافر الحيوي لمساعد الإنزيم CoQ10
إن أهمية كيفية صياغة الأدوية من أجل التوافر الحيوي معروفة بشكل جيد. من أجل العثور على مبدأ لتعزيز التوافر الحيوي لمساعد الإنزيم CoQ10 بعد تناوله عن طريق الفم، اتبع العديد من الأساليب الجديدة؛ تم تطوير واختبار تركيبات وأشكال مختلفة على الحيوانات والبشر.[50]
تصغير حجم الجسيمات
استكشفت الجسيمات النانوية كنظام إيتاء للأدوية المختلفة، مثل تحسين التوافر الحيوي عن طريق الفم للأدوية ذات خصائص الامتصاص الضعيفة.[54] ومع ذلك ، لم ينجح ذلك مع CoQ10، على الرغم من اختلاف التقارير بشكل كبير.[55][56] كما أن استخدام معلق مائي لمسحوق CoQ10 الناعم في الماء النقي يكشف فقط عن تأثير طفيف.[52]
كبسولات الهلام اللين CoQ10 في معلق الزيت
النهج الناجح هو استخدام نظام مستحلب لتسهيل الامتصاص من الجهاز الهضمي وتحسين التوافر الحيوي. يمكن تثبيت مستحلبات زيت فول الصويا (الكريات الدهنية الدقيقة) بشكل فعال للغاية بواسطة الليسيثين واستخدامها في تحضير كبسولات هلامية. في إحدى المحاولات الأولى، أجرى أوزاوا وآخرون دراسة الحركية الدوائية على كلاب البيجل حيث فُحص مستحلب CoQ10 في زيت فول الصويا؛ وكان مستوى CoQ10 في البلازما يزيد بمقدار الضعف تقريبا عن تحضيره في قرص التحكم، الذي تم تحديده أثناء إيتاء الدواء عن طريق الغلاف المجهري الدهني.[52] على الرغم من أن كومورو وزملائه قد لاحظوا تحسنًا ضئيلًا تقريبًا في التوافر الحيوي مع كبسولات الكبسولات الهلامية القائمة على الزيت في دراسة لاحقة على الكلاب،[57] إلا أن التوافر الحيوي المتزايد بشكل ملحوظ لمساعد الإنزيم CoQ10 قد تأكد للعديد من التركيبات القائمة على الزيت في معظم الدراسات الأخرى.[58]
الأشكال الجديدة من CoQ10 الأكبر قدرة على الذوبان في الماء
يعد تسهيل امتصاص الدواء عن طريق زيادة قابليته للذوبان في الماء استراتيجية دوائية شائعة وقد ثبت أيضًا نجاحه مع CoQ10. تم تطوير طرق مختلفة لتحقيق هذا الهدف، حيث ينتج الكثير منها نتائج أفضل بشكل ملحوظ على الكبسولات الهلامية القائمة على الزيت على الرغم من المحاولات العديدة لتحسين تركيبها.[50] ومن أمثلة هذه الأساليب استخدام المشتت المائي لمساعد الإنزيم الصلب CoQ10 مع البوليمر تايلوكسابول،[59] تركيبات تعتمد على عوامل مختلفة للذوبان، مثل الليسيثين المهدرج،[60] والتركيب مع السيكلودكسترين؛ من الأخير، عُثر على المركب مع β-cyclodextrin لزيادة التوافر الحيوي بشكل كبير[61][62] ويستخدم أيضًا في الصناعات الدوائية والغذائية من أجل تعزيز CoQ10.[50]
التاريخ
عام 1950، كان ج. ن. فستنشتاين أول من عزل كمية صغيرة من CoQ10 من بطانة أمعاء حصان في ليفربول، إنجلترا. في الدراسات اللاحقة، سُمي المركب لفترة وجيزة "مادة SA"، واعتبر أنه كينون ولوحظ أنه يمكن العثور عليه من العديد من أنسجة الحيوانات.[63]
عام 1957، عزل فريدريك كرين وزملاؤه في جامعة وسكنسن-ماديسون نفس المركب من أغشية الميتوكوندريا لقلب بقرة ولاحظوا أنه ينقل الإلكترونات داخل الميتوكوندريا. أطلقوا عليه اسم "Q-275" اختصاراً لأنه كان كينون.[64][63] سرعان ما لاحظوا أن Q-275 والمادة SA المدروسة في إنجلترا قد يكونان نفس المركب. تأكد ذلك في وقت لاحق من ذلك العام وتم تغيير اسم Q-275/مادة SA إلى "أوبيكينون" لأنه كان كينون في كل مكان يمكن العثور عليه من جميع الأنسجة الحيوانية.[63][43]
عام 1958 توصل د. إ. وولف وزملائه تحت إشراف كارل فولكرز بشركة مرك في راهواي إلى البنية الكيميائية الكاملة للإنزيم المساعد.[65][63][43] في وقت لاحق من ذلك العام، اقترح د. إ. جرين وزملاؤه المنتمون إلى مجموعة أبحاث وسكنسن أن الأوبيكينون يجب أن يسمى إما "ميتوكينون" أو "إنزيم Q" نظرًا لمشاركته في سلسلة نقل الإلكترون في الميتاكوندريا.[63][43]
عام 1966، كان أ. ملورز وأ. ل. تابل من جامعة كاليفورنيا أول من أظهر أن انخفاض CoQ6 كان مضاد أكسدة فعال في الخلايا.[66][43]
في الستينيات ، توسع بيتر ميتشل بناءً على فهم وظيفة الميتوكوندريا من خلال نظريته عن التدرج الكهروكيميائي، والتي تتضمن CoQ10، وفي أواخر السبعينيات قام لارس إرنستر بدراسات موسعة بناءً على أهمية CoQ10 كمضاد للأكسدة. شهدت الثمانينيات ارتفاعًا حادًا في عدد التجارب السريرية التي تتضمنت CoQ10.[43]
التركيزات الغذائية
نُشرت المراجعات التفصيلية حول تواجد CoQ10 والمدخول الغذائي عام 2010.[67] إلى جانب التخليق الداخلي داخل العضيات، تستمد العضياتCoQ10 أيضاً عن طريق الأغذية المختلفة. على الرغم من اهتمام المجتمع العلمي الكبير بهذا المركب، إلا أنه لم يًُجرى سوى عدد محدود جدًا من الدراسات لتحديد محتويات CoQ10 في المكونات الغذائية. نُشرت التقارير الأولى عن هذا الجانب عام 1959، لكن حساسية وانتقائية الطرق التحليلية في ذلك الوقت لم تسمح بتحليلات موثوقة، خاصة بالنسبة للمنتجات ذات التركيزات المنخفضة.[67] منذ ذلك الحين، أتاحت التطورات في الكيمياء التحليلية تحديدًا أكثر موثوقية لتركيزات CoQ10 في الأغذية المختلفة:
| الغذاء | تركيز CoQ10 (ملج/كج) | |
|---|---|---|
| الزيوت | زيت فول الصويا | 54–280 |
| الزيتون | 40–160 | |
| بذور العنب | 64–73 | |
| عباد الشمس | 4–15 | |
| الكانولا | 64–73 | |
| اللحم البقري | القلب | 113 |
| الكبد | 39–50 | |
| العضلات | 26–40 | |
| لحم الخنزير | القلب | 12–128 |
| الكبد | 23–54 | |
| العضلات | 14–45 | |
| الدجاج | الصدر | 8–17 |
| الأفخاذ | 24–25 | |
| الأجنحة | 11 | |
| الأسماك | السردين | 5–64 |
| الماكرل: | ||
| – الأسماك الحمراء | 43–67 | |
| – الأسماك البيضاء | 11–16 | |
| السلمون | 4–8 | |
| التونة | 5 | |
| المكسرات | الفول السوداني | 27 |
| عين الجمل | 19 | |
| زيت السمسم | 18–23 | |
| الفستق | 20 | |
| البندق | 17 | |
| اللوز | 5–14 | |
| الخضروات | البقدونس | 8–26 |
| البروكلي | 6–9 | |
| القرنبيط | 2–7 | |
| السبانخ | حتى 10 | |
| الملفوف الصيني | 2–5 | |
| الفواكه | الأفوكادو | 10 |
| الكشمش الأسود | 3 | |
| العنب | 6–7 | |
| الفراولة | 1 | |
| البرتقال | 1–2 | |
| الجريب فروت | 1 | |
| التفاح | 1 | |
| الموز | 1 | |
الزيوت النباتية هي أغنى المصادر الغذائية بمساعد الإنزيم CoQ10؛ تعتبر اللحوم والأسماك أيضًا غنية جدًا بمستوياتCoQ10 التي تزيد عن 50 ملجم؛ كما يتواجد بمستويات مرتفعة في لحوم الأبقار والخنازير وقلب وكبد الدجاج.
تحتوي منتجات الألبان على مستويات CoQ10 أقل بكثير من الأنسجة الحيوانية. ضمن الخضروات، يعد البقدونس والبريلا من أغنى المصادر بمساعد الإنزيم CoQ10، لكن يمكن العثور على اختلافات كبيرة في مستويات CoQ10 في الدراسات. تحتوي البروكلي والعنب والقرنبيط على كميات متواضعة من CoQ10. تمثل معظم الفاكهة والتوت مصدرًا سيئًا إلى فقير جدًا من CoQ10، باستثناء الأفوكادو، الذي يحتوي على محتوى CoQ10 مرتفع نسبيًا.[67]
الجرعة
في العالم المتقدم، تم تحديد المقدار اليومي من CoQ10 بمعدل 3-6 ملجم يوميًا، مشتق بشكل أساسي من اللحوم.[67]
المتوسط المقدر من CoQ في كوريا الجنوبية هو (Q9 + Q10) بمقدار 11.6 ملجم/يومياً، مشتقة بشكل أساسي من الكيمتشي.[68]
تأثير التسخين والمعالجة
يقلل القلي محتوى CoQ10 بنسبة 14-32٪.[69]
انظر أيضاً
- الإيدبينون – مناظر اصطناعي بخصائص توليد الأكسدة منخفضة.
- ميسيلات الميتوكينون – مناظر اصطناعي بنفاذية ميتوكوندريا محسنة.
المصادر
- ^ Ernster L, Dallner G (May 1995). "Biochemical, physiological and medical aspects of ubiquinone function". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1271 (1): 195–204. doi:10.1016/0925-4439(95)00028-3. PMID 7599208.
- ^ Dutton, P. L.; Ohnishi, T.; Darrouzet, E.; Leonard, M. A.; Sharp, R. E.; Cibney, B. R.; Daldal, F.; Moser, C. C. (2000). "4 Coenzyme Q oxidation reduction reactions in mitochondrial electron transport". In Kagan, V. E.; Quinn, P. J. (eds.). Coenzyme Q: Molecular mechanisms in health and disease. Boca Raton: CRC Press. pp. 65–82.
- ^ Okamoto T, Matsuya T, Fukunaga Y, Kishi T, Yamagami T (1989). "Human serum ubiquinol-10 levels and relationship to serum lipids". International Journal for Vitamin and Nutrition Research. Internationale Zeitschrift für Vitamin- und Ernahrungsforschung. Journal International de Vitaminologie et de Nutrition. 59 (3): 288–92. PMID 2599795.
- ^ Aberg F, Appelkvist EL, Dallner G, Ernster L (June 1992). "Distribution and redox state of ubiquinones in rat and human tissues". Archives of Biochemistry and Biophysics. 295 (2): 230–4. doi:10.1016/0003-9861(92)90511-T. PMID 1586151.
- ^ Shindo Y, Witt E, Han D, Epstein W, Packer L (January 1994). "Enzymic and non-enzymic antioxidants in epidermis and dermis of human skin". The Journal of Investigative Dermatology. 102 (1): 122–4. doi:10.1111/1523-1747.ep12371744. PMID 8288904.
- ^ Hathcock JN, Shao A (August 2006). "Risk assessment for coenzyme Q10 (Ubiquinone)". Regulatory Toxicology and Pharmacology. 45 (3): 282–8. doi:10.1016/j.yrtph.2006.05.006. PMID 16814438.
- ^ أ ب ت Trevisson E, DiMauro S, Navas P, Salviati L (October 2011). "Coenzyme Q deficiency in muscle". Current Opinion in Neurology. 24 (5): 449–56. doi:10.1097/WCO.0b013e32834ab528. hdl:10261/129020. PMID 21844807.
- ^ Montero R, Sánchez-Alcázar JA, Briones P, Hernández AR, Cordero MD, Trevisson E, et al. (June 2008). "Analysis of coenzyme Q10 in muscle and fibroblasts for the diagnosis of CoQ10 deficiency syndromes". Clinical Biochemistry. 41 (9): 697–700. doi:10.1016/j.clinbiochem.2008.03.007. hdl:11577/2447079. PMID 18387363.
- ^ أ ب ت Tan JT, Barry AR (June 2017). "Coenzyme Q10 supplementation in the management of statin-associated myalgia". American Journal of Health-System Pharmacy. 74 (11): 786–793. doi:10.2146/ajhp160714. PMID 28546301. S2CID 3825396.
- ^ أ ب Qu H, Guo M, Chai H, Wang WT, Gao ZY, Shi DZ (October 2018). "Effects of Coenzyme Q10 on Statin-Induced Myopathy: An Updated Meta-Analysis of Randomized Controlled Trials". Journal of the American Heart Association. 7 (19): e009835. doi:10.1161/JAHA.118.009835. PMC 6404871. PMID 30371340.
- ^ أ ب ت ث White, J. (14 May 2014). "PDQ® Coenzyme Q10". National Cancer Institute, National Institutes of Health, U.S. Dept. of Health and Human Services. Retrieved 29 June 2014.
- ^ "Mitochondrial disorders in children: Co-enzyme Q10". UK: National Institute for Health and Care Excellence. 28 March 2017.
- ^ Hojerová, J (May 2000). "[Coenzyme Q10--its importance, properties and use in nutrition and cosmetics]". Ceska a Slovenska Farmacie: Casopis Ceske Farmaceuticke Spolecnosti a Slovenske Farmaceuticke Spolecnosti. 49 (3): 119–23. PMID 10953455.
- ^ "What is coenzyme Q10 (CoQ10) and why is it in skin care products?". WebMD (in الإنجليزية).
- ^ "ConsumerLab.com finds discrepancies in strength of CoQ10 supplements". Townsend Letter for Doctors and Patients. Aug–Sep 2004. p. 19.
- ^ "ConsumerLab.com finds discrepancies in strength of CoQ10 supplements". ConsumerLab.com. Jan 2004.
- ^ أ ب Wyman M, Leonard M, Morledge T (July 2010). "Coenzyme Q10: a therapy for hypertension and statin-induced myalgia?". Cleveland Clinic Journal of Medicine. 77 (7): 435–42. doi:10.3949/ccjm.77a.09078. PMID 20601617. S2CID 26572524.
- ^ Flowers N, Hartley L, Todkill D, Stranges S, Rees K (4 December 2014). "Co-enzyme Q10 supplementation for the primary prevention of cardiovascular disease". The Cochrane Database of Systematic Reviews. 2014 (12): CD010405. doi:10.1002/14651858.CD010405.pub2. PMC 9759150. PMID 25474484.
- ^ Ho MJ, Li EC, Wright JM (March 2016). "Blood pressure lowering efficacy of coenzyme Q10 for primary hypertension". The Cochrane Database of Systematic Reviews. 2016 (3): CD007435. doi:10.1002/14651858.CD007435.pub3. PMC 6486033. PMID 26935713.
- ^ Al Saadi, Tareq; Assaf, Yazan; Farwati, Medhat; Turkmani, Khaled; Al-Mouakeh, Ahmad; Shebli, Baraa; Khoja, Mohammed; Essali, Adib; Madmani, Mohammed E (2021-02-03). Cochrane Heart Group (ed.). "Coenzyme Q10 for heart failure". Cochrane Database of Systematic Reviews (in الإنجليزية). 2021 (2): CD008684. doi:10.1002/14651858.CD008684.pub3. PMC 8092430. PMID 35608922.
- ^ Lei L, Liu Y (July 2017). "Efficacy of coenzyme Q10 in patients with cardiac failure: a meta-analysis of clinical trials". BMC Cardiovascular Disorders. 17 (1): 196. doi:10.1186/s12872-017-0628-9. PMC 5525208. PMID 28738783.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Pringsheim T, Davenport W, Mackie G, Worthington I, Aubé M, Christie SN, et al. (March 2012). "Canadian Headache Society guideline for migraine prophylaxis". The Canadian Journal of Neurological Sciences. 39 (2 Suppl 2): S1-59. PMID 22683887.
- ^ Banach M, Serban C, Sahebkar A, Ursoniu S, Rysz J, Muntner P, et al. (January 2015). "Effects of coenzyme Q10 on statin-induced myopathy: a meta-analysis of randomized controlled trials". Mayo Clinic Proceedings (Systematic Review and Meta-Analysis). Lipid and Blood Pressure Meta-analysis Collaboration Group. 90 (1): 24–34. doi:10.1016/j.mayocp.2014.08.021. PMID 25440725.
- ^ "Coenzyme Q10". American Cancer Society.
- ^ Watts TL (March 1995). "Coenzyme Q10 and periodontal treatment: is there any beneficial effect?". British Dental Journal. 178 (6): 209–13. doi:10.1038/sj.bdj.4808715. PMID 7718355. S2CID 7207070.
- ^ Folkers K, Hanioka T, Xia LJ, McRee JT, Langsjoen P (April 1991). "Coenzyme Q10 increases T4/T8 ratios of lymphocytes in ordinary subjects and relevance to patients having the AIDS related complex". Biochemical and Biophysical Research Communications. 176 (2): 786–91. doi:10.1016/S0006-291X(05)80254-2. PMID 1673841.
- ^ Littarru GP, Nakamura R, Ho L, Folkers K, Kuzell WC (October 1971). "Deficiency of coenzyme Q 10 in gingival tissue from patients with periodontal disease". Proceedings of the National Academy of Sciences of the United States of America. 68 (10): 2332–5. Bibcode:1971PNAS...68.2332L. doi:10.1073/pnas.68.10.2332. PMC 389415. PMID 5289867.
- ^ Nakamura R, Littarru GP, Folkers K, Wilkinson EG (April 1974). "Study of CoQ10-enzymes in gingiva from patients with periodontal disease and evidence for a deficiency of coenzyme Q10". Proceedings of the National Academy of Sciences of the United States of America. 71 (4): 1456–60. Bibcode:1974PNAS...71.1456N. doi:10.1073/pnas.71.4.1456. PMC 388248. PMID 4151519.
- ^ McRee, J. T.; Hanioka, T.; Shizukuishi, S.; Folkers, K. (1993). "Therapy with coenzyme Q10 for patients with periodontal disease". Journal of Dental Health. 43 (5): 659–666. doi:10.5834/jdh.43.659.
- ^ Hanioka T, Tanaka M, Ojima M, Shizukuishi S, Folkers K (1994). "Effect of topical application of coenzyme Q10 on adult periodontitis". Molecular Aspects of Medicine. 15 Suppl (Suppl): s241-8. doi:10.1016/0098-2997(94)90034-5. PMID 7752836.
- ^ Wilkinson EG, Arnold RM, Folkers K (August 1976). "Bioenergetics in clinical medicine. VI. adjunctive treatment of periodontal disease with coenzyme Q10". Research Communications in Chemical Pathology and Pharmacology. 14 (4): 715–9. PMID 785563.
- ^ Xu, Yongxing; Liu, Juan; Han, Enhong; Wang, Yan; Gao, Jianjun (2019). "Efficacy of coenzyme Q10 in patients with chronic kidney disease: protocol for a systematic review". BMJ Open. 9 (5): e029053. doi:10.1136/bmjopen-2019-029053. ISSN 2044-6055. PMC 6530451. PMID 31092669.
- ^ Knott, Anja; Achterberg, Volker; Smuda, Christoph; Mielke, Heiko; Sperling, Gabi; Dunckelmann, Katja; Vogelsang, Alexandra; Krüger, Andrea; Schwengler, Helge; Behtash, Mojgan; Kristof, Sonja (2015-11-12). "Topical treatment with coenzyme Q10‐containing formulas improves skin's Q10 level and provides antioxidative effects". Biofactors. 41 (6): 383–390. doi:10.1002/biof.1239. ISSN 0951-6433. PMC 4737275. PMID 26648450.
- ^ Addor, Flavia Alvim Sant'anna (2017). "Antioxidants in dermatology". Anais Brasileiros de Dermatologia. 92 (3): 356–362. doi:10.1590/abd1806-4841.20175697. ISSN 0365-0596. PMC 5514576. PMID 29186248.
- ^ Blatt, Thomas; Wittern, Klaus-Peter; Wenck, Horst; Staeb, Franz (2004-03-01). "CoQ10, a topical energizer for aging skin". Journal of the American Academy of Dermatology (in English). 50 (3): P76. doi:10.1016/j.jaad.2003.10.628. ISSN 0190-9622.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Zhang, M.; Dang, L.; Guo, F.; Wang, X.; Zhao, W.; Zhao, R. (June 2012). "Coenzyme Q(10) enhances dermal elastin expression, inhibits IL-1α production and melanin synthesis in vitro". International Journal of Cosmetic Science. 34 (3): 273–279. doi:10.1111/j.1468-2494.2012.00713.x. ISSN 1468-2494. PMID 22339577. S2CID 4664219.
- ^ Hseu, You-Cheng; Ho, Yi-Geng; Mathew, Dony Chacko; Yen, Hung-Rong; Chen, Xuan-Zao; Yang, Hsin-Ling (2019-06-01). "The in vitro and in vivo depigmenting activity of Coenzyme Q10 through the down-regulation of α-MSH signaling pathways and induction of Nrf2/ARE-mediated antioxidant genes in UVA-irradiated skin keratinocytes". Biochemical Pharmacology (in الإنجليزية). 164: 299–310. doi:10.1016/j.bcp.2019.04.015. ISSN 0006-2952. PMID 30991050. S2CID 119556226.
- ^ Afonso, S.; Horita, K.; Sousa e Silva, J. P.; Almeida, I. F.; Amaral, M. H.; Lobão, P. A.; Costa, P. C.; Miranda, Margarida S.; Esteves da Silva, Joaquim C. G.; Sousa Lobo, J. M. (November 2014). "Photodegradation of avobenzone: stabilization effect of antioxidants". Journal of Photochemistry and Photobiology B: Biology. 140: 36–40. doi:10.1016/j.jphotobiol.2014.07.004. ISSN 1873-2682. PMID 25086322.
- ^ Wu, Haiyou; Zhong, Zhangfeng; Lin, Sien; Qiu, Chuqun; Xie, Peitao; Lv, Simin; Cui, Liao; Wu, Tie (2020-08-19). "Coenzyme Q10 Sunscreen Prevents Progression of Ultraviolet-Induced Skin Damage in Mice". BioMed Research International (in الإنجليزية). 2020: 1–8. doi:10.1155/2020/9039843. PMC 7453241. PMID 32923487.
- ^ Grether-Beck, Susanne; Marini, Alessandra; Jaenicke, Thomas; Krutmann, Jean (January 2015). "Effective photoprotection of human skin against infrared A radiation by topically applied antioxidants: results from a vehicle controlled, double-blind, randomized study". Photochemistry and Photobiology. 91 (1): 248–250. doi:10.1111/php.12375. ISSN 1751-1097. PMID 25349107. S2CID 206270691.
- ^ Lim, Henry W.; Arellano-Mendoza, Maria-Ivonne; Stengel, Fernando (March 2017). "Current challenges in photoprotection". Journal of the American Academy of Dermatology. 76 (3S1): S91–S99. doi:10.1016/j.jaad.2016.09.040. ISSN 1097-6787. PMID 28038886.
- ^ Sharma, A; Fonarow, GC; Butler, J; Ezekowitz, JA; Felker, GM (April 2016). "Coenzyme Q10 and Heart Failure: A State-of-the-Art Review". Circulation: Heart Failure. 9 (4): e002639. doi:10.1161/CIRCHEARTFAILURE.115.002639. PMID 27012265. S2CID 2034503.
- ^ أ ب ت ث ج ح Boreková M, et al. (2008). "Nourishing and health benefits of coenzyme Q10". Czech Journal of Food Sciences. 26 (4): 229–241. doi:10.17221/1122-cjfs.
- ^ Bentinger M, Tekle M, Dallner G (May 2010). "Coenzyme Q--biosynthesis and functions". Biochemical and Biophysical Research Communications. 396 (1): 74–9. doi:10.1016/j.bbrc.2010.02.147. PMID 20494114.
- ^ Espinós, Carmen; Felipo, Vicente; Palau, Francesc (2009). Inherited Neuromuscular Diseases: Translation from Pathomechanisms to Therapies. Springer. pp. 122ff. ISBN 978-90-481-2812-9. Retrieved 4 January 2011.
- ^ Meganathan R (September 2001). "Ubiquinone biosynthesis in microorganisms". FEMS Microbiology Letters. 203 (2): 131–9. doi:10.1111/j.1574-6968.2001.tb10831.x. PMID 11583838.
- ^ أ ب Bhagavan HN, Chopra RK (May 2006). "Coenzyme Q10: absorption, tissue uptake, metabolism and pharmacokinetics". Free Radical Research. 40 (5): 445–53. doi:10.1080/10715760600617843. PMID 16551570. S2CID 39001523.
- ^ Bogentoft 1991[التحقق مطلوب]
- ^ Ochiai A, Itagaki S, Kurokawa T, Kobayashi M, Hirano T, Iseki K (August 2007). "Improvement in intestinal coenzyme q10 absorption by food intake". Yakugaku Zasshi. 127 (8): 1251–4. doi:10.1248/yakushi.127.1251. PMID 17666877.[التحقق مطلوب]
- ^ أ ب ت ث Žmitek; et al. (2008). "Improving the bioavailability of CoQ10". Agro Food Industry Hi Tech. 19 (4): 9. Archived from the original on 5 October 2011. Retrieved 21 October 2008.
- ^ Kishi, H.; Kanamori, N.; Nisii, S.; Hiraoka, E.; Okamoto, T.; Kishi, T. (1964). "Metabolism and Exogenous Coenzyme Q10 in vivo and Bioavailability of Coenzyme Q10 Preparations in Japan". Biomedical and Clinical Aspects of Coenzyme Q. Amsterdam: Elsevier. pp. 131–142.
- ^ أ ب ت Ozawa Y, Mizushima Y, Koyama I, Akimoto M, Yamagata Y, Hayashi H, Murayama H (April 1986). "Intestinal absorption enhancement of coenzyme Q10 with a lipid microsphere". Arzneimittel-Forschung. 36 (4): 689–90. PMID 3718593.
- ^ Tomono Y, Hasegawa J, Seki T, Motegi K, Morishita N (October 1986). "Pharmacokinetic study of deuterium-labelled coenzyme Q10 in man". International Journal of Clinical Pharmacology, Therapy, and Toxicology. 24 (10): 536–41. PMID 3781673.
- ^ Mathiowitz E, Jacob JS, Jong YS, Carino GP, Chickering DE, Chaturvedi P, et al. (March 1997). "Biologically erodable microspheres as potential oral drug delivery systems". Nature. 386 (6623): 410–4. Bibcode:1997Natur.386..410M. doi:10.1038/386410a0. PMID 9121559. S2CID 4324209.
- ^ Hsu CH, Cui Z, Mumper RJ, Jay M (2003). "Preparation and characterization of novel coenzyme Q10 nanoparticles engineered from microemulsion precursors". AAPS PharmSciTech. 4 (3): E32. doi:10.1208/pt040332. PMC 2750625. PMID 14621964.[التحقق مطلوب]
- ^ Joshi SS, Sawant SV, Shedge A, Halpner AD (January 2003). "Comparative bioavailability of two novel coenzyme Q10 preparations in humans". International Journal of Clinical Pharmacology and Therapeutics. 41 (1): 42–8. doi:10.5414/CPP41042. PMID 12564745.[التحقق مطلوب]
- ^ Kommuru TR, Ashraf M, Khan MA, Reddy IK (July 1999). "Stability and bioequivalence studies of two marketed formulations of coenzyme Q10 in beagle dogs". Chemical & Pharmaceutical Bulletin. 47 (7): 1024–8. doi:10.1248/cpb.47.1024. PMID 10434405.
- ^ Bhagavan HN, Chopra RK (June 2007). "Plasma coenzyme Q10 response to oral ingestion of coenzyme Q10 formulations". Mitochondrion. 7 Suppl (Suppl): S78-88. doi:10.1016/j.mito.2007.03.003. PMID 17482886.[التحقق مطلوب]
- ^ {{{1}}} patent {{{2}}}
- ^ {{{1}}} patent {{{2}}}
- ^ Zmitek J, Smidovnik A, Fir M, Prosek M, Zmitek K, Walczak J, Pravst I (2008). "Relative bioavailability of two forms of a novel water-soluble coenzyme Q10". Annals of Nutrition & Metabolism. 52 (4): 281–7. doi:10.1159/000129661. PMID 18645245. S2CID 825159.
- ^ Kagan, Daniel; Madhavi, Doddabele (2010). "A Study on the Bioavailability of a Novel Sustained-Release Coenzyme Q10-β-Cyclodextrin Complex". Integrative Medicine. 9 (1).
- ^ أ ب ت ث ج Morton RA (December 1958). "Ubiquinone". Nature. 182 (4652): 1764–7. Bibcode:1958Natur.182.1764M. doi:10.1038/1821764a0. PMID 13622652.
- ^ Crane FL, Hatefi Y, Lester RL, Widmer C (July 1957). "Isolation of a quinone from beef heart mitochondria". Biochimica et Biophysica Acta. 25 (1): 220–1. doi:10.1016/0006-3002(57)90457-2. PMID 13445756.
- ^ Wolf DE, et al. (1958). "Coenzyme Q. I. structure studies on the coenzyme Q group". Journal of the American Chemical Society. 80 (17): 4752. doi:10.1021/ja01550a096. ISSN 0002-7863.
- ^ Mellors A, Tappel AL (July 1966). "Quinones and quinols as inhibitors of lipid peroxidation". Lipids. 1 (4): 282–4. doi:10.1007/BF02531617. PMID 17805631. S2CID 2129339.
- ^ أ ب ت ث ج Pravst I, Zmitek K, Zmitek J (April 2010). "Coenzyme Q10 contents in foods and fortification strategies". Critical Reviews in Food Science and Nutrition. 50 (4): 269–80. doi:10.1080/10408390902773037. PMID 20301015. S2CID 38779392.
- ^ doi:10.1016/j.jfca.2011.03.018
- ^ Weber C, Bysted A, Hłlmer G (1997). "The coenzyme Q10 content of the average Danish diet". International Journal for Vitamin and Nutrition Research. Internationale Zeitschrift für Vitamin- und Ernahrungsforschung. Journal International de Vitaminologie et de Nutrition. 67 (2): 123–9. PMID 9129255.
وصلات خارجية
- "List of USP Verified CoQ10 Ingredients". U.S. Pharmacopeial Convention. Archived from the original on 9 February 2009.
- "Coenzyme Q10". National Cancer Institute. 23 September 2005.
- Bonakdar, Robert Alan; Guarneri, Erminia (15 September 2005). "Coenzyme Q10". American Family Physician. 72 (6): 1065–1070. PMID 16190504.
- CS1 maint: unflagged free DOI
- مقالات بالمعرفة تحتاج تمحيص الحقائق from November 2010
- جميع الصفحات التي تحتاج تمحيص حقائق
- Short description matches Wikidata
- ECHA InfoCard ID from Wikidata
- Articles containing unverified chemical infoboxes
- Short description is different from Wikidata
- مضادات أكسدة
- 1,4-بنزوكونينات
- تنفس خلوي
- مساعدات الإنزيم
- مضادات أكسدة غذائية
- تحلل السكر
- إيثرات الفنول
- بوليينات