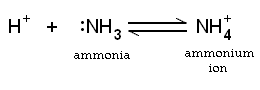أمونيوم
| |||
|
| |||
| الأسماء | |||
|---|---|---|---|
| اسم أيوپاك
Ammonium
| |||
| اسم أيوپاك النظامي
Azanium[1] | |||
| المُعرِّفات | |||
| رقم CAS | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| عناوين مواضيع طبية MeSH | |||
PubChem CID
|
|||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| الخصائص | |||
| الصيغة الجزيئية | H4N | ||
| كتلة مولية | 18.04 g mol-1 | ||
| الحموضة (pKa) | 9.25 | ||
| البنية | |||
| الشكل الجزيئي | Tetrahedral | ||
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |||
| مراجع الجدول | |||
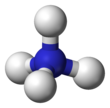
الأمونيوم Ammonium هو شاردة موجبة (كاتيون) للتجمع الذري +NH4 . كتلته المولية مقدارها 18.04 غ/مول، وينتج من عملية إضافة بروتون (برتنة) للأمونياك. يتميز الأمونيوم بأنه قلوي له ثابت تشرد حمضي (pKa) مقداره 9.25 .
كيمياء الأمونيوم - خصائص الحمض-قاعدة
في شاردة الأمونيوم ترتبط ذرة النيتروجين المشحونة إيجاباً بأربع روابط مشتركة مع الهيدروجين. تتصرف شاردة الأمونيوم كحمض برونشتد لوري ضعيف ، أي أن شاردة الأمونيوم قادرة على منح بروتون إلى قاعدة أقوى وذلك بالتخلي عن أي من ذرات الهيدروجين التي لديها ، فتتحول بالتالي إلى الأمونيا. مما يعني أن شاردة الأمونيوم هي حمض مترافق مع القاعدة التي هي الأمونيا.
تعتمد مقدرة الأمونيا في المحلول في تشكيل شاردة الأمونيوم على pH الوسط. أغلب مركبات الأمونيوم تكون في المحاليل، إلا أنه يمكن أن تتكون أيضاً في الحالة الغازية؛ فعلى سبيل المثال عندما يحصل تماس بين بخار الأمونيا مع بخار كلور الهيدروجين تنشأ سحابة بيضاء من كلوريد الأمونيوم، والتي تترسب أخيراً على شكل صلب على سطح المحلول.
الأملاح والتفاعلات المميزة
Ammonium cation is found in a variety of salts such as ammonium carbonate, ammonium chloride, and ammonium nitrate. Most simple ammonium salts are very soluble in water. An exception is ammonium hexachloroplatinate, the formation of which was once used as a test for ammonium. The ammonium salts of nitrate and especially perchlorate are highly explosive, in these cases, ammonium is the reducing agent.
In an unusual process, ammonium ions form an amalgam. Such species are prepared by the addition of sodium amalgam to a solution of ammonium chloride.[2] This amalgam eventually decomposes to release ammonia and hydrogen.[3]
To find whether the ammonium ion is present in the salt, first, the salt is heated in presence of alkali hydroxide releasing a gas with a characteristic smell, which is ammonia.
- [NH
4]+
+ OH−
NH
3 + H
2O
To further confirm ammonia, it is passed through a glass rod dipped in an HCl solution (hydrochloric acid), creating white dense fumes of ammonium chloride.
- NH
3(g) + HCl(aq) → [NH
4]Cl(s)
Ammonia, when passed through CuSO
4 (copper(II) sulfate) solution, changes its color from blue to deep blue, forming Schweizer's reagent.
- CuSO
4(aq) + 4 NH
3(aq) + 4 H
2O → [Cu(NH
3)
4(H
2O)
2](OH)
2(aq) + H
2SO
4(aq)
Ammonia or ammonium ion when added to Nessler's reagent gives a brown color precipitate known as the iodide of Million's base in basic medium.
Ammonium ion when added to chloroplatinic acid gives a yellow precipitate of ammonium hexachloroplatinate(IV).
- H
2[PtCl
6](aq) + [NH
4]+
(aq) → [NH
4]
2[PtCl
6](s) + 2 H+
Ammonium ion when added to sodium cobaltinitrite gives a yellow precipitate of ammonium cobaltinitrite.
- Na
3[Co(NO
2)
6](aq) + 3 [NH
4]+
(aq) → [NH
4]
3[Co(NO
2)
6](s) + 3 Na+
(aq)
Ammonium ion gives a white precipitate of ammonium bitartrate when added to potassium bitartrate.
- KC
4H
5O
6(aq) + [NH
4]+
(aq) → [NH
4]C
4H
5O
6(s) + K+
(aq)
البنية والروابط
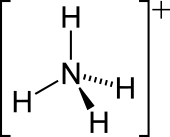
The lone electron pair on the nitrogen atom (N) in ammonia, represented as a line above the N, forms a coordinate bond with a proton (H+
). After that, all four N−H bonds are equivalent, being polar covalent bonds. The ion has a tetrahedral structure and is isoelectronic with methane and the borohydride anion. In terms of size, the ammonium cation (rionic = 175 pm)[citation needed] resembles the caesium cation (rionic = 183 pm).[citation needed]
الأيونات العضوية
The hydrogen atoms in the ammonium ion can be substituted with an alkyl group or some other organic group to form a substituted ammonium ion (IUPAC nomenclature: aminium ion). Depending on the number of organic groups, the ammonium cation is called a primary, secondary, tertiary, or quaternary. Except the quaternary ammonium cations, the organic ammonium cations are weak acids.
An example of a reaction forming an ammonium ion is that between dimethylamine, (CH
3)
2NH, and an acid to give the dimethylammonium cation, [(CH
3)
2NH
2]+
:
Quaternary ammonium cations have four organic groups attached to the nitrogen atom, they lack a hydrogen atom bonded to the nitrogen atom. These cations, such as the tetra-n-butylammonium cation, are sometimes used to replace sodium or potassium ions to increase the solubility of the associated anion in organic solvents. Primary, secondary, and tertiary ammonium salts serve the same function but are less lipophilic. They are also used as phase-transfer catalysts and surfactants.
An unusual class of organic ammonium salts is derivatives of amine radical cations, [•NR
3]+
such as tris(4-bromophenyl)ammoniumyl hexachloroantimonate.
علم الأحياء

Because nitrogen often limits net primary production due to its use in enzymes that mediate the biochemical reactions that are necessary for life, ammonium is utilized by some microbes and plants.[4] For example, energy is released by the oxidation of ammonium in a process known as nitrification, which produces nitrate and nitrite.[5] This process is a form of autotrophy that is common amongst Nitrosomonas, Nitrobacter, Nitrosolobus, and Nitrosospira, amongst others.[5]
The amount of ammonium in soil that is available for nitrification by microbes varies depending on environmental conditions.[6][7] For example, ammonium is deposited as a waste product from some animals, although it is converted into urea in mammals, sharks, and amphibians, and into uric acid in birds, reptiles, and terrestrial snails.[8] Its availability in soils is also influenced by mineralization, which makes more ammonium available from organic nitrogen sources, and immobilization, which sequesters ammonium into organic nitrogen sources, both of which are mitigated by biological factors.[5]
Conversely, nitrate and nitrite can be reduced to ammonium as a way for living organisms to access nitrogen for growth in a process known as assimilatory nitrate reduction.[9] Once assimilated, it can be incorporated into proteins and DNA.[10]
Ammonium can accumulate in soils where nitrification is slow or inhibited, which is common in hypoxic soils.[11] For example, ammonium mobilization is one of the key factors for the symbiotic association between plants and fungi, called mycorrhizae.[12] However, plants that consistently utilize ammonium as a nitrogen source often must invest into more extensive root systems due to ammonium's limited mobility in soils compared to other nitrogen sources.[13][14]
الوقع البشري
Ammonium deposition from the atmosphere has increased in recent years due to volatilization from livestock waste and increased fertilizer use.[15] Because net primary production is often limited by nitrogen, increased ammonium levels could impact the biological communities that rely on it. For example, increasing nitrogen content has been shown to increase plant growth, but aggravate soil phosphorus levels, which can impact microbial communities.[16]
الفلز
The ammonium cation has very similar properties to the heavier alkali metal cations and is often considered a close equivalent.[17][18][19] Ammonium is expected to behave as a metal ([NH
4]+
ions in a sea of electrons) at very high pressures, such as inside giant planets such as Uranus and Neptune.[18][19]
Under normal conditions, ammonium does not exist as a pure metal but does as an amalgam (alloy with mercury).[20]
انظر أيضاً
المراجع
- ^ قالب:RedBookRef
- ^ "Pseudo-binary compounds". Archived from the original on 2020-07-27. Retrieved 2007-10-12.
- ^ "Ammonium Salts". VIAS Encyclopedia.
- ^ Schlesinger, William H.; Bernhardt, Emily S. (2020-01-01), Schlesinger, William H.; Bernhardt, Emily S., eds., Chapter 12 - The Global Cycles of Nitrogen, Phosphorus and Potassium, Academic Press, pp. 483–508, doi:, ISBN 978-0-12-814608-8, https://www.sciencedirect.com/science/article/pii/B9780128146088000128, retrieved on 2024-03-08
- ^ أ ب ت Rosswall, T. (1982). "Microbiological regulation of the biogeochemical nitrogen cycle / Regulación microbiana del ciclo bíogeoquímico del nitrógeno". Plant and Soil. 67 (1/3): 15–34. doi:10.1007/BF02182752. ISSN 0032-079X. JSTOR 42934020.
- ^ Barsdate, Robert J.; Alexander, Vera (January 1975). "The Nitrogen Balance of Arctic Tundra: Pathways, Rates, and Environmental Implications". Journal of Environmental Quality (in الإنجليزية). 4 (1): 111–117. Bibcode:1975JEnvQ...4..111B. doi:10.2134/jeq1975.00472425000400010025x. ISSN 0047-2425.
- ^ Nadelhoffer, Knute J.; Aber, John D.; Melillo, Jerry M. (1984-10-01). "Seasonal patterns of ammonium and nitrate uptake in nine temperate forest ecosystems". Plant and Soil (in الإنجليزية). 80 (3): 321–335. Bibcode:1984PlSoi..80..321N. doi:10.1007/BF02140039. ISSN 1573-5036.
- ^ Campbell, Neil A.; Reece, Jane B. (2002). Biology. Internet Archive. San Francisco : Benjamin Cummings. ISBN 978-0-8053-6624-2.
- ^ Tiedje, J. M.; Sørensen, J.; Chang, Y.-Y. L. (1981). "Assimilatory and Dissimilatory Nitrate Reduction: Perspectives and Methodology for Simultaneous Measurement of Several Nitrogen Cycle Processes". Ecological Bulletins (33): 331–342. ISSN 0346-6868. JSTOR 45128674.
- ^ Llácer, José L; Fita, Ignacio; Rubio, Vicente (2008-12-01). "Arginine and nitrogen storage". Current Opinion in Structural Biology. Catalysis and regulation / Proteins. 18 (6): 673–681. doi:10.1016/j.sbi.2008.11.002. hdl:10261/111022. ISSN 0959-440X. PMID 19013524.
- ^ Wang, Lixin; Macko, Stephen A. (March 2011). "Constrained preferences in nitrogen uptake across plant species and environments". Plant, Cell & Environment (in الإنجليزية). 34 (3): 525–534. doi:10.1111/j.1365-3040.2010.02260.x. ISSN 0140-7791. PMID 21118424.
- ^ Hodge, Angela; Storer, Kate (2015-01-01). "Arbuscular mycorrhiza and nitrogen: implications for individual plants through to ecosystems". Plant and Soil (in الإنجليزية). 386 (1): 1–19. Bibcode:2015PlSoi.386....1H. doi:10.1007/s11104-014-2162-1. ISSN 1573-5036.
- ^ Raven, John A.; Linda, Bernd Wollenweber; Handley, L. (May 1992). "Ammonia and ammonium fluxes between photolithotrophs and the environment in relation to the global nitrogen cycle". New Phytologist (in الإنجليزية). 121 (1): 5–18. doi:10.1111/j.1469-8137.1992.tb01087.x. ISSN 0028-646X.
- ^ Bloom, A. J.; Jackson, L. E.; Smart, D. R. (March 1993). "Root growth as a function of ammonium and nitrate in the root zone". Plant, Cell & Environment (in الإنجليزية). 16 (2): 199–206. doi:10.1111/j.1365-3040.1993.tb00861.x. ISSN 0140-7791.
- ^ Ackerman, Daniel; Millet, Dylan B.; Chen, Xin (January 2019). "Global Estimates of Inorganic Nitrogen Deposition Across Four Decades". Global Biogeochemical Cycles (in الإنجليزية). 33 (1): 100–107. Bibcode:2019GBioC..33..100A. doi:10.1029/2018GB005990. ISSN 0886-6236.
- ^ Dong, Junfu; Cui, Xiaoyong; Niu, Haishan; Zhang, Jing; Zhu, Chuanlu; Li, Linfeng; Pang, Zhe; Wang, Shiping (2022-06-20). "Effects of Nitrogen Addition on Plant Properties and Microbiomes Under High Phosphorus Addition Level in the Alpine Steppe". Frontiers in Plant Science. 13. doi:10.3389/fpls.2022.894365. ISSN 1664-462X. PMC 9251499. PMID 35795351.
- ^ قالب:Holleman&Wiberg
- ^ أ ب Stevenson, D. J. (November 20, 1975). "Does metallic ammonium exist?". Nature. 258 (5532): 222–223. Bibcode:1975Natur.258..222S. doi:10.1038/258222a0. S2CID 4199721.
- ^ أ ب Bernal, M. J. M.; Massey, H. S. W. (February 3, 1954). "Metallic Ammonium". Monthly Notices of the Royal Astronomical Society. 114 (2): 172–179. Bibcode:1954MNRAS.114..172B. doi:10.1093/mnras/114.2.172.
- ^ Reedy, J.H. (October 1, 1929). "Lecture demonstration of ammonium amalgam". Journal of Chemical Education. 6 (10): 1767. Bibcode:1929JChEd...6.1767R. doi:10.1021/ed006p1767.