ورم قحفي بلعومي
| Pituicytoma | |
|---|---|
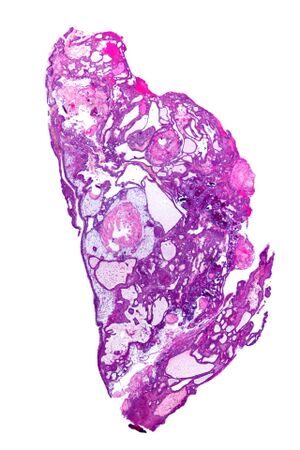 | |
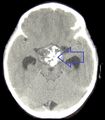
| Very low magnification micrograph of an adamantinomatous craniopharyngioma. HPS stain. | |
| التخصص | علم الأورام |
الورم القحفي البلعومي هو نوع نادر من أورام المخ مشتق من أنسجة الغدة النخامية[1] والتي تحدث بشكل شائع عند الأطفال ، ولكنها تؤثر أيضًا على البالغين. قد يظهر في أي عمر ، حتى في فترة ما قبل الولادة وفترات حديثي الولادة ، ولكن معدلات حدوث الذروة تبدأ في الطفولة عند 5-14 سنة وتبدأ عند البالغين عند 50-74 سنة.[2] قد يصاب الأشخاص بالعمي الرباعي الصدغي السفلي مما يؤدي إلى عمى نصفي صدغي ، حيث قد يضغط الورم على التصالب البصري . تبلغ نسبة انتشاره نقطتين لكل 1،000،000.[3] تختلف الأورام القحفية البلعومية عن أورام جيبة راتكه والتكيسات العنكبوتية داخل الخلايا.[4]
العلامات والاعراض
تكون الأورام القحفية البلعومية حميدة دائمًا ف الاغلب.[5] ومع ذلك ، كما هو الحال مع العديد من أورام الدماغ ، قد يكون علاجها صعبًا ، وترتبط حالات المرض الكبيرة بالورم والعلاج
- صداع (استسقاء المخ الانسدادي)[6]
- فرط النوم[7]
- وذمة مخاطية
- زيادة الوزن بعد الجراحة[8]
- عطاش[9]
- بوال ( مرض السكري الكاذب ) [10]
- فقدان البصر ( عمى نصفي صدغي )[11]
- قيء[12]
- غالبا ما يحدث بعد العلاج
- قصور هرمون النمو (GH) الناجم عن انخفاض إنتاج هرمون النمو - يشمل الأعراض:
- تأخر النمو وتأخر البلوغ (عند الأطفال)
- التعب العام ، وفقدان كتلة العضلات وقوتها (عند البالغين)
- قصور الغدة النخامية
- غالبًا ما يحدث إلى حد ما لأن الورم القحفي البلعومي يتطور في منطقة سويقة الغدة النخامية ، مما قد يؤثر على وظيفة الغدة النخامية والعديد من الهرمونات الأخرى[13]
- انخفاض إنتاج البرولاكتين غير شائع جدًا ويحدث مع قصور حاد في الغدة النخامية.
- يمكن لأورام الغدة النخامية الكبيرة أن ترفع مستويات البرولاكتين في الدم بشكل متناقض بسبب "تأثير السويقة". يحدث هذا الارتفاع نتيجة ضغط سويقة الغدة النخامية ، والذي يتعارض مع تحكم الدماغ في إنتاج البرولاكتين.
- في النساء قبل انقطاع الطمث ، يمكن أن يؤدي ارتفاع مستوى البرولاكتين إلى تقليل أو فقدان فترات الطمث و / أو إنتاج حليب الثدي (ثر اللبن).
- مع تأثير السويقة ، عادةً ما تكون مستويات البرولاكتين مرتفعة قليلاً فقط ، على عكس أورام البرولاكتين التي يكون فيها مستوى البرولاكتين مرتفعًا جدًا.
- يحدث مرض السكري الكاذب[14] بسبب عدم وجود هرمون الغدة النخامية الخلفي يسمى الهرمون المضاد لإدرار البول. تشمل الأعراض:
- العطش الشديد
- التبول المفرط
- يحدث قصور الغدة الكظرية[13] بسبب انخفاض إنتاج الهرمون الموجه لقشر الكظر ، وانخفاض الكورتيزول. في الحالات الشديدة ، يمكن أن تكون قاتلة. تشمل الأعراض::
الآليات
الورم القحفي البلعومي هو ورم نادر ، عادة ما يكون فوق السرج التركي[15] والذي قد يكون كيسيًا ، يتطور من أعشاش ظهارة مشتقة من جيبة راتكه
.[16][17]جيبة راتكه هي طليعة جنينية للغدة النخامية الأمامية.
عادةً ما تكون الأورام القحفية البلعومية أورامًا بطيئة النمو. تنشأ من الخلايا الموجودة على طول سويقة الغدة النخامية ، وتحديداً من أعشاش من ظهارة سنية (مكونة للأسنان) داخل منطقة فوق السرج التركي / الدماغ البيني ، لذلك تحتوي على رواسب الكالسيوم التي تظهر في الأشعة السينية.[18]
التشخيص
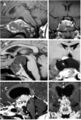
فحوصات التصوير للورم القحفي البلعومي
يمكن للطبيب إجراء بعض الفحوصات والاختبارات لتشخيص الشخص المصاب بالورم القحفي البلعومي.[19] يعد التصوير بالرنين المغناطيسي عالي الدقة (MRI) ذا قيمة لأنه يسمح لأخصائي الأشعة العصبية بمشاهدة الورم من زوايا مختلفة..
في بعض الحالات ، يمكن أن يساعد ماسح التصوير بالرنين المغناطيسي القوي 3T (Tesla) في تحديد موقع هياكل الدماغ الهامة المتأثرة بالورم. يتكون النمط النسيجي من تعشيش ظهارة حرشفية تحدها خلايا مرتبة بشكل اشعاعي. غالبًا ما يكون مصحوبًا بترسب الكالسيوم وقد يكون له بنية حليمية مجهرية. يعد التصوير المقطعي المحوسب (CT) أيضًا أداة تشخيصية جيدة ، حيث يكتشف التكلس في الورم..[20]
يتم التعرف على نوعين متميزين:[21][22]
- الاورام البلعومية القحفية المينائية ، التي تشبه الاورام الأرومية المينائية (أكثر نوع شائع من الأورام سنية المنشأ)، وتتميز من خلال تفعيل الطفرات CTNNB1.
- تتميز الأورام القحفية البلعومية الحليمية بطفرات BRAFv600E.[23]
في النوع المينائي ، تظهر التكلسات في التصوير العصبي وهي مفيدة في التشخيص.
نادرا ما يتكلس النوع الحليمي. الغالبية العظمى من الأورام القحفية البلعومية عند الأطفال تكون شديدة ، في حين أن كلا النوعين الفرعيين شائعان عند البالغين. تحدث الأورام المختلطة أيضًا.[24]
في الفحص العياني ، يكون الورم القحفي البلعومي كيسيًا أو كيسيًا جزئيًا مع مناطق صلبة. في المجهر الضوئي ، يُنظر إلى الأكياس على أنها مبطنة بظهارة حرشفية طبقية. يمكن أيضًا رؤية لآلئ الكيراتين. تمتلئ الأكياس عادة بسائل أصفر لزج غني ببلورات الكوليسترول. من بين قائمة طويلة من الأعراض المحتملة ، تشمل العروض المجيئية الأكثر شيوعًا الصداع ، وفشل النمو ، والعمى نصفي صدغي مزدوج .
يظهر التصوير المقطعي المحوسب ورم قحفي بلعومي
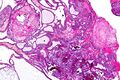
صورة مجهرية توضح السمات المميزة للورم القحفي البلعومي المينائي - الفراغات الكيسية ، والتكلسات ، والكيراتين "الرطب" ، صبغة الهيماتوكسيلين فلوكسين الكركمية اللون
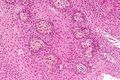
صورة مجهرية تظهر ورم قحفي بلعومي حليمي ، صبغة الهيماتوكسيلين فلوكسين الكركمية اللون
الورم القحفي البلعومي الخبيث
عادةً ما تتم معالجة الأورام القحفية البلعومية بنجاح بمزيج من العلاج الكيميائي المساعد وجراحة الأعصاب. تصف الأبحاث الحديثة الحدوث النادر للتحولات الخبيثة لهذه الأورام الحميدة في العادة. يمكن أن تحدث الأورام القحفية البلعومية الخبيثة في أي عمر ، وهي أكثر شيوعًا قليلاً عند الإناث ، وعادةً ما تكون من النوع المينائي.[25]
يمكن أن تستغرق التحولات الخبيثة سنوات حتى تحدث (على الرغم من أن حالة واحدة من كل خمس حالات تم تشخيصها كانت عبارة عن تحولات جديدة ) ، ومن هنا تأتي الحاجة إلى متابعة أطول للمرضى الذين تم تشخيصهم بأشكال حميدة أكثر شيوعًا.[25]
لم يتم العثور على أي صلة بين الورم الخبيث والعلاج الكيميائي الإشعاعي الأولي,[25] وكان معدل البقاء على قيد الحياة ضعيفًا جدًا مع متوسط البقاء على قيد الحياة بعد 6 أشهر من تشخيص الورم الخبيث.
الوقاية
على الرغم من أن أسباب الورم القحفي البلعومي غير معروفة ، إلا أنه يمكن أن يحدث في كل من الأطفال والبالغين ، ويبلغ معدل الإصابة ذروته في سن 9 إلى 14 عامًا. يتم تشخيص حوالي 120 حالة كل عام في الولايات المتحدة لدى مرضى تقل أعمارهم عن 19 عامًا. أكثر من 50٪ من جميع مرضى الورم القحفي البلعومي تقل أعمارهم عن 18 عامًا. لا يوجد ارتباط واضح بين الورم وجنس أو عرق معين. لا يبدو أن الورم القحفي البلعومي "يسري في العائلات" أو أنه موروث مباشرة من الوالدين[بحاجة لمصدر]
العلاج
يتكون العلاج عمومًا من استئصال تحت الجبهي أو استئصال عظمي. الجراحة بالمنظار من خلال الأنف[26][27] oغالبًا ما يتم إجراؤها بواسطة فريق مشترك من جراحي الأعصاب والأنف والحنجرة ، يتم اعتبارها بشكل متزايد كبديل للجراحة عبر الجمجمة التي يتم إجراؤها عن طريق فتح فتحة في الجمجمة. نظرًا لموقع الورم القحفي البلعومي بالقرب من الدماغ وقاعدة الجمجمة ، يمكن استخدام نظام ملاحة جراحي للتحقق من موضع الأدوات الجراحية أثناء العملية.[28]
يتم استخدام العلاج الإشعاعي الإضافي أيضًا إذا كان الإزالة الكاملة غير ممكنة. نظرًا للنتائج السيئة المرتبطة بتلف الغدة النخامية والوطاء من الإزالة الجراحية والإشعاع ، يتم أحيانًا استخدام العلاجات التجريبية باستخدام الفسفور داخل التجويف 32 أو الإيتريوم أو البليوميسين عبر خزان خارجي ، خاصة في المرضى الصغار. يمكن أن يسبب الورم ، الموجود في الغدة النخامية ، مشاكل صحية ثانوية. يمكن أن يتعرض الجهاز المناعي ومستويات الغدة الدرقية ومستويات هرمون النمو ومستويات هرمون التستوستيرون للخطر من الورم القحفي البلعومي. كل هذه المشاكل الصحية يمكن علاجها بالطب الحديث..[29] لا يوجد دليل عالي الجودة قام بتقييم استخدام البليوميسين في هذه الحالة.[30]
يوفر العلاج بالبروتون انخفاضًا في جرعة الهياكل الحرجة مقارنة بإشعاع الفوتون التقليدي ، بما في ذلك العلاج الاشعاعي ذو الشدة المعدلة ، للمرضى الذين يعانون من ورم قحفي بلعومي..[31]
"حزمة" العلاج الأكثر فاعلية للأورام القحفية البلعومية الخبيثة الموصوفة في المنشورات هي الجمع بين الجراحة "الجزئية الاستئصالية الكلية" مع العلاج الكيميائي الإشعاعي المساعد. أظهرت عقاقير العلاج الكيميائي باكليتاكسيل وكاربوبلاتين أهمية إكلينيكية (ولكن ليست إحصائية) في زيادة معدل البقاء على قيد الحياة لدى المرضى الذين خضعوا لعمليات استئصال كلية لأورامهم الخبيثة.[25]
المآل
[25]تعتبر الأورام القحفية البلعومية حميدة بشكل عام ولكن من المعروف أنها تتكرر بعد الاستئصال. أظهرت الأبحاث الحديثة ميلًا خبيثًا (ولكن نادرًا) للأورام القحفية البلعومية. هذه الأورام القحفية البلعومية الخبيثة نادرة جدًا ولكنها مرتبطة بسوء المآل.
الابحاث الحديثة
أظهرت الأبحاث الحالية طرقًا لعلاج الأورام بطريقة أقل توغلًا بينما أظهر البعض الآخر كيف يمكن تحفيز منطقة الوطاء مع الورم لمنع إصابة الطفل والبالغ بالورم بالسمنة. عادة ما يكون الورم القحفي البلعومي في مرحلة الطفولة كيسيًا بطبيعته.[32] قد تؤدي الجراحة المحدودة التي تقلل من تلف الوطاء إلى الحد من معدل السمنة الشديدة على حساب الحاجة إلى العلاج الإشعاعي لإكمال العلاج.[33]
دور العلاج الاشعاعي
تؤدي المحاولات العدوانية للإزالة الكاملة إلى البقاء على قيد الحياة لفترات طويلة بدون تقدم في معظم المرضى ، ولكن بالنسبة للأورام التي تتضمن بوضوح منطقة تحت المهاد ، فقد دفعت المضاعفات المرتبطة بالجراحة الجذرية إلى اعتماد استراتيجية مشتركة من الجراحة المحافظة والعلاج الإشعاعي للورم المتبقي مع ارتفاع معدل العلاج. يبدو أن هذه الاستراتيجية تقدم أفضل معدلات السيطرة على المدى الطويل مع معدلات اعتلال مقبولة. لكن المعالجة المثلى للأورام القحفية البلعومية لا تزال محل جدل. على الرغم من أنه يوصى عمومًا بإعطاء العلاج الإشعاعي بعد الاستئصال الجزئي للورم القحفي البلعومي ، إلا أنه لا يزال من غير الواضح ما إذا كان يجب على جميع المرضى الذين يعانون من الورم المتبقي تلقي العلاج الإشعاعي الفوري أو المختلف عند الانتكاس.[34] الجراحة والعلاج الإشعاعي هما حجر الزاوية في المعالجة العلاجية للورم القحفي البلعومي. يرتبط الاستئصال الجذري بخطر الوفاة أو الإصابة بالأمراض خاصةً مثل تلف الوطاء ، والتدهور البصري ، ومضاعفات الغدد الصماء بين 45 و 90٪ من الحالات. يشكل القرب من الهياكل البليغة المجاورة تحديًا خاصًا للعلاج الإشعاعي. تقنيات العلاج الحديثة بما في ذلك العلاج الإشعاعي المطابق المجزأ ثلاثي الأبعاد,[35] العلاج الإشعاعي المعدل الشدة ، والعلاج بالبروتونات مؤخرًا قادرة على تغطية الهدف بدقة مع الحفاظ على الأنسجة المحيطة ، ويمكن تحقيق السيطرة على الورم بنسبة تزيد عن 90٪. توفر العلاجات البديلة التي تتكون من الجراحة الإشعاعية والتطبيق داخل التجويفات للنظائر والمعالجة الكثبية أيضًا تحكمًا مقبولًا في الورم ويمكن إعطاؤها في حالات مختارة. هناك حاجة إلى مزيد من البحث لتحديد دور كل طريقة علاج..[36]
مراجع
- ^ "Craniopharyngioma". The Lecturio Medical Concept Library. Retrieved 10 July 2021.
- ^ Hermann L. Müller Endocrine Reviews, Volume 35, Issue 3, 1 June 2014, Pages 513–543, https://doi.org/10.1210/er.2013-1115
- ^ Garnett MR, Puget S, Grill J, Sainte-Rose C (2007). "Craniopharyngioma". Orphanet Journal of Rare Diseases. 2: 18. doi:10.1186/1750-1172-2-18. PMC 1855047. PMID 17425791.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Jennifer L. Shin, Sylvia L. Asa, Linda J. Woodhouse, Harley S. Smyth, Shereen Ezzat, The Journal of Clinical Endocrinology & Metabolism, Volume 84, Issue 11, 1 November 1999, pp3972–3982. https://doi.org/10.1210/jcem.84.11.6114
- ^ Garrè ML, Cama A (2007). "Craniopharyngioma: modern concepts in pathogenesis and treatment". Curr. Opin. Pediatr. 19 (4): 471–9. doi:10.1097/MOP.0b013e3282495a22. PMID 17630614. S2CID 25955091.
- ^ "Hydrocephalus Fact Sheet". NINDS. April 5, 2016. Archived from the original on 27 July 2016. Retrieved 5 September 2016.
- ^ Reynolds, Charles F.; O’Hara, Ruth (2013). "DSM-5 Sleep-Wake Disorders Classification: Overview for Use in Clinical Practice". The American Journal of Psychiatry. 170 (10): 1099–1101. doi:10.1176/appi.ajp.2013.13010058. PMID 24084814.
The aim is simply to acknowledge the bidirectional and interactive effects between sleep disorders and coexisting medical and psychiatric illnesses.
- ^ Ahmet A, Blaser S, Stephens D, Guger S, Rutkas JT, Hamilton J (2006). "Weight gain in craniopharyngioma--a model for hypothalamic obesity". Journal of Pediatric Endocrinology & Metabolism. 19 (2): 121–7. doi:10.1515/jpem.2006.19.2.121. PMID 16562584. S2CID 35451441.
- ^ Porth, C. M (1990). Pathophysiology: Concepts of altered health states. Philadelphia: Philadelphia: J.B. Lippincott Company.
- ^ "Diabetes Insipidus". The Lecturio Medical Concept Library. Retrieved 11 July 2021.
- ^ "Bitemporal hemianopsia". Science Daily.
- ^ "Pediatric Vomiting". The Lecturio Medical Concept Library. Retrieved 19 July 2021.
- ^ أ ب "Craniopharyngioma | UCLA Pituitary Tumor Program". pituitary.ucla.edu. Retrieved 2017-12-09.
- ^ "Diabetes insipidus - Symptoms and causes - Mayo Clinic". www.mayoclinic.org (in الإنجليزية). Retrieved 2017-12-09.
- ^ Rodriguez FJ, Scheithauer BW, Tsunoda S, Kovacs K, Vidal S, Piepgras DG (2007). "The spectrum of malignancy in craniopharyngioma". Am. J. Surg. Pathol. 31 (7): 1020–8. doi:10.1097/PAS.0b013e31802d8a96. PMID 17592268. S2CID 36172034.
- ^ Moore, Kraig D.; Couldwell, William T. (January 15, 2000). "41. Craniopharyngioma". In Bernstein, Mark; Berger, Mitchel S. (eds.). Neuro-oncology: the essentials. Endorsed by the Joint Tumor Section of the American Association of Neurological Surgeons & the Congress of Neurological Surgeons. Thieme. pp. 409–418. ISBN 978-0-86577-880-1. Retrieved August 8, 2011.
- ^ "Endocrine Pathology". Retrieved 2009-05-08.
- ^ "Craniopharyngioma". The Lecturio Medical Concept Library. Retrieved 22 July 2021.
- ^ "Craniopharyngioma - Childhood: Diagnosis | Cancer.Net". Cancer.Net (in الإنجليزية). 2012-06-25. Retrieved 2017-12-09.
- ^ "Craniopharyngioma". UCLA Health.
- ^ Sekine S, Shibata T, Kokubu A, et al. (December 2002). "Craniopharyngiomas of adamantinomatous type harbor beta-catenin gene mutations". Am. J. Pathol. 161 (6): 1997–2001. doi:10.1016/s0002-9440(10)64477-x. PMC 1850925. PMID 12466115.
- ^ Sekine S, Takata T, Shibata T, et al. (December 2004). "Expression of enamel proteins and LEF1 in adamantinomatous craniopharyngioma: evidence for its odontogenic epithelial differentiation". Histopathology. 45 (6): 573–9. doi:10.1111/j.1365-2559.2004.02029.x. PMID 15569047. S2CID 35192721.
- ^ Brastianos, Priscilla K.; Taylor-Weiner, Amaro; Manley, Peter E.; Jones, Robert T.; Dias-Santagata, Dora; Thorner, Aaron R.; Lawrence, Michael S.; Rodriguez, Fausto J.; Bernardo, Lindsay A. (February 2014). "Exome sequencing identifies BRAF mutations in papillary craniopharyngiomas". Nature Genetics. 46 (2): 161–165. doi:10.1038/ng.2868. ISSN 1546-1718. PMC 3982316. PMID 24413733.
- ^ Weiner, HL; Miller, DC; et al. (Dec 1994). "Craniopharyngiomas: a clinicopathological analysis of factors predictive of recurrence and functional outcome". Neurosurgery. 35 (6): 1001–10, discussion 1010–1. doi:10.1227/00006123-199412000-00001. PMID 7885544.
- ^ أ ب ت ث ج Sofela, AA; Hettige, S; Curran, O; Bassi, S (Sep 2014). "Malignant transformation in craniopharyngiomas". Neurosurgery. 75 (3): 306–14, discussion 314. doi:10.1227/NEU.0000000000000380. PMID 24978859.
- ^ Dhandapani, S; et, al. (Feb 2017). "Endonasal endoscopic reoperation for residual or recurrent craniopharyngiomas". J Neurosurg. 126 (2): 418–430. doi:10.3171/2016.1.JNS152238. PMID 27153172.
- ^ "Mayfield".
- ^ "Use of Surgical Navigation for Craniopharyngioma Removal". January 2013.
- ^ Wisoff, JH (Feb 2008). "Craniopharyngioma". Journal of Neurosurgery. Pediatrics. 1 (2): 124–5, discussion 125. doi:10.3171/PED/2008/1/2/124. PMID 18352780.
- ^ Zhang, Si; Fang, Yuan; Cai, Bo Wen; Xu, Jian Guo; You, Chao (2016-07-14). "Intracystic bleomycin for cystic craniopharyngiomas in children". The Cochrane Database of Systematic Reviews. 7: CD008890. doi:10.1002/14651858.CD008890.pub4. ISSN 1469-493X. PMC 6457977. PMID 27416004.
- ^ "Treating Pediatric Tumors With Proton Therapy Current Practice, Opportunities and Challenges". October 2015.
- ^ Roth, C.; Wilken, B.; Hanefeld, F.; Schroter, W.; Leonhardt, U. (1998-01-01). "Hyperphagia in children with craniopharyngioma is associated with hyperleptinaemia and a failure in the downregulation of appetite". European Journal of Endocrinology (in الإنجليزية). 138 (1): 89–91. doi:10.1530/eje.0.1380089. ISSN 0804-4643. PMID 9461323.
- ^ Elowe-Gruau, E.; Beltrand, J.; Brauner, R.; Pinto, G.; Samara-Boustani, D.; Thalassinos, C.; Busiah, K.; Laborde, K.; Boddaert, N. (June 2013). "Childhood craniopharyngioma: hypothalamus-sparing surgery decreases the risk of obesity". The Journal of Clinical Endocrinology and Metabolism. 98 (6): 2376–2382. doi:10.1210/jc.2012-3928. ISSN 1945-7197. PMID 23633208.
- ^ Chargari, Cyrus; Bauduceau, Olivier; Bauduceau, Bernard; Camparo, Philippe; Ceccaldi, Bernard; Fayolle, Maryse; Le Moulec, Sylvestre; Védrine, Lionel (2007-12-01). "Craniopharyngiomas: Role of radiotherapy". Bulletin du Cancer. 94 (11): 987–94. PMID 18055317.
- ^ "Three Dimensional (3D) Conformal Radiation Therapy". hillman.upmc.com (in الإنجليزية). Retrieved 2017-12-09.
- ^ Kortmann, Rolf-Dieter (2011-12-20). "Different Approaches in Radiation Therapy of Craniopharyngioma". Frontiers in Endocrinology. 2: 100. doi:10.3389/fendo.2011.00100. ISSN 1664-2392. PMC 3356005. PMID 22654836.
{{cite journal}}: CS1 maint: unflagged free DOI (link)