تحت كلوريت الكالسيوم
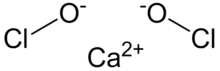
| |
| الأسماء | |
|---|---|
| اسم أيوپاك
هيبوكلوريت الكالسيوم
| |
| أسماء أخرى
مسحوق القصر (التبييض)
| |
| المُعرِّفات | |
| رقم CAS | |
| ECHA InfoCard | 100.029.007 |
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | Ca(OCl)2 |
| كتلة مولية | 142.98 غ/مول |
| المظهر | مسحوق بلوري أبيض |
| الكثافة | 2.35 غ/سم3 |
| نقطة الانصهار | |
| قابلية الذوبان في الماء | 21 غ/100 مل ماء يتفاعل |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
 O O
|
| توصيف المخاطر | R8-R22-R31-R34-R50 |
| تحذيرات وقائية | (S1/2)-S26-S36/37/39-S45-S61 |
| الجرعة أو التركيز القاتل (LD, LC): | |
LD50 (الجرعة الوسطى)
|
850 مغ/كغ (جرذان، فموي) [1] |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
تحت كلوريت كالسيوم (هيبو كلوريت الكالسيوم) مركب كيميائي له الصيغة Ca(OCl)2، ويكون على شكل مسحوق بلوري أبيض مصفر، له رائحة الكلور.
الخواص
- ينحل تحت كلوريت الكالسيوم بشكل جيد في الماء، وتكون محاليله المائية المركزة ذات لون أصفر مخضر.
- يتميز تحت كلوريت الكالسيوم بخواصه المؤكسدة القوية، وهو يحرر غاز الكلور عند التماس مع الحموض. فعلى سبيل المثال عند التفاعل مع حمض هيدروكلوريك يتحرر غاز الكلور ويتشكل كلوريد الكالسيوم حسب المعادلة:
- Ca(ClO)2 + 4 HCl → CaCl2 + 2 H2O + 2 Cl2
كما يتحرر غاز الكلور عند التفاعل مع غاز ثنائي أكسيد الكربون ويتشكل كربونات الكالسيوم:
- 2 Ca(ClO)2 + 2 CO2 → 2 CaCO3 + 2 Cl2 + O2
تتراوح نسبة الكلور الفعال في العينات التجارية من تحت كلوريت الكالسيوم من 35–80 %.
التحضير
يحضر تحت كلوريت الكالسيوم من تنرير غاز الكلور على مستعلق هيدروكسيد الكالسيوم المائي عند درجات حرارة منخفضة (-20°س)، وذلك لأن التفاعل ناشر للحرارة:
2 Ca(OH)2 + 2 Cl2 → Ca(ClO)2.2H2O + CaCl2 + 2 H2O
يكون تحت كلوريت الكالسيوم الناتج من هذه العملية عبارة عن هيدرات ثنائية، ويحوي مزيجاً من كلوريد الكالسيوم القلوي Ca(OH)2, H2O، بالإضافة إلى الكلس غير المتفاعل. [2]
الاستخدامات
- يستخدم كمادة قاصرة (مبيضة) في الصناعات النسيجية، كما يستخدم لقصر عجينة الورق.
- يستخدم تحت كلوريت الكالسيوم في تعقيم مياه المسابح.
المصادر
- موسوعة رومب الكيميائية Römpp Lexikon Chemie, Georg Thieme Verlag
المراجع
- ^ http://www.merck-chemicals.com/documents/sds/emd/eng/en/8417/841799.pdf
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
الكلمات الدالة:
This article may include material from Wikimedia licensed under CC BY-SA 4.0. Please comply with the license terms.
