أتورفاستاتين
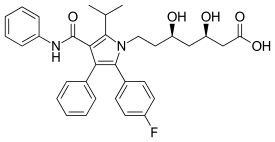 | |
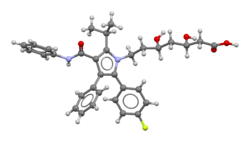 | |
| البيانات السريرية | |
|---|---|
| النُطق | /əˌtɔːrvəˈstætən/ |
| الأسماء التجارية | ليپيتور، وأسماء أخرى |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a600045 |
| License data |
|
| فئة السلامة أثناء الحمل | |
| مسارات الدواء | عن طريق الفم |
| رمز ATC | |
| الحالة القانونية | |
| الحالة القانونية | |
| بيانات الحركية الدوائية | |
| التوافر الحيوي | 12% |
| الأيض | الكبد (CYP3A4) |
| Elimination half-life | 14 ساعة |
| الإخراج | العصارة المرارية |
| المعرفات | |
| |
| رقم CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| PDB ligand | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.125.464 |
| Chemical and physical data | |
| التركيب | C33H35FN2O5 |
| الكتلة المولية | 558٫65 g·mol−1 |
| 3D model (JSmol) | |
| |
| |
| (verify) | |
الأتورڤاستاتين (إنگليزية: Atorvastatin)، يباع تحت الاسم التجاري ليپيتور Lipitor، وأسماء أخرى)، هو أحد أدوية الستاتينات الذي يستخدمه للوقاية من الأمراض القلبية الوعائية لمن يعانون من ارتفاع الكولسترول أو ارتفاع نسبة الدهون في الدم.[3] من أجل الوقاية من الأمراض القلبية الوعائية، تعتبر الستاتينات هي الخط العلاجي الأول.[3] تؤخذ الستاتينات عن طريق الفم.[3]
تشمل الآثار الجانبية الشائعة آلام المفاصل والإسهال والحموضة المعدة والغثيان وآلام العضلات.[3] قد تشمل الآثار الجانبية الخطيرة انحلال الربيدات ومشاكل الكبد ومرض السكري.[3] استخدام الدواء أثناء الحمل قد يضر بالجنين.[3] مثل جميع الستاتينات، يعمل أتورڤاستاتين عن طريق تثبيط HMG-CoA reductase، إنزيم موجود في الكبد يلعب دوراً في إنتاج الكولسترول.[3]
سُجلت براءة اختراع أتورڤاستاتين عام 1986، واعتمد للاستخدام الطبي في الولايات المتحدة عام 1996.[3][4] وهو مدرج على قائمة الأدوية الأساسية بحسب منظمة الصحة العالمية.[5] وهو متوفر على شكل دواء مكافئ.[3][6] عام 2020، كان الليپيتور هو الدواء الأكثر شيوعاً في الولايات المتحدة، بأكثر من 114 مليون وصفة طبية.[7][8]
الاستخدامات الطبية
يستخدم الأتورڤاستاتين بشكل أساسي لعلاج اضطرابات دهون الدم والوقاية من الأمراض القلبية الوعائية:[9]
اضطرابات دهون الدم
- فرط كولسترول الدم[10] (فرط كولسترول الدم العائلي والغير عائلي) واضطرابات دهون الدم المختلطة (نمط فردركسون 2أ و2ب) وخفض الكولسترول الإجمالي، الپروتين الدهني منخفض الكثافة-ج،[11] صميم الپروتين الدهني ب،[12] مستويات الدهون الثلاثية[13] وCRP[14] وكذلك زيادة مستويات الپروتين الدهني مرتفع الكثافة (الكولسترول النافع).
- فرط كولسترول الدم العائلي متغير الزيجوت[10] لدى الأطفال
- فرط كولسترول الدم العائلي متماثل الزيجوت[10][15]
- فرط ثلاثي الگليسريد في الدم (نمط فردركسون الرابع)
- نقص ثلاثي الگليسريد في الدم (نمط فردركسون الثالث)
- فرط دهون الدم المركب[16]
الأمراض القلبية الوعائية
- الوقاية الأولية من النوبات القلبية والسكتة الدماغية والحاجة إلى إجراءات إعادة توعية لدى الأشخاص الذين لديهم عوامل خطر مثل العمر والتدخين وارتفاع ضغط الدم وانخفاض HDL-C وتاريخ عائلي لإصابة بأمراض القلب المبكرة، لكن لم يتطور لديهم دليل على خطر الإصابة بأمراض الشرايين التاجية.[2]
- الوقاية الثانوية من الاحتشاء القلبي، السكتة الدماغية، الذبحة الصدرية غير المستقرة،[17][18] وإعادة تكوين الأوعية الدموية لدى الأشخاص المصابين بمرض الشريان التاجي المستقر.[19][20]
- الوقاية من الاحتشاء القلبي والسكتة الدماغية لدى مرضى سكري النمط 2.[21][22][23]
أظهر تحليل شمولي عام 2014 أن العلاج بجرعة عالية من الستاتين كان أفضل بشكل ملحوظ مقارنة بالعلاج المعتدل أو المنخفض الكثافة في تقليل حجم اللويحة في المرضى الذين يعانون من متلازمة الشريان التاجي الحادة.[24] أكدت تجربة SATURN التي قارنت تأثيرات الجرعات العالية من أتورڤاستاتين وروسوڤاستاتين أيضًا هذه النتائج.[25]
على الرغم من الجرعة العالية، فإن جرعة 40 ملگم من الپراڤاستاتين في تجربة REVERSAL فشلت في وقف تقدم اللويحات، مما يشير إلى عوامل أخرى مثل استخدام الستاتين، ومدة وموقع اللويحة قد تؤثر أيضًا على تقليل حجم اللويحة وبالتالي استقرارها.[26] بشكل عام، يجب اعتبار تقليل اللويحة كنقطة نهاية بديلة ويجب عدم استخدامه مباشرة لتحديد الفائدة السريرية للعلاج.[25][26] يجب أيضًا مراعاة زيادة مخاطر الآثار الجانبية عند التفكير في العلاج بجرعات عالية من الستاتين.[24][25][26]
أمراض الكلى
هناك أدلة من المراجعة المنهجية والتحليلات الشمولية على أن الستاتينات، وخاصة الأتورڤاستاتين، تقلل من انخفاض وظائف الكلى (eGFR) وشدة إفراز الپروتين في البول،[27][28][29] حيث الجرعات الأكبر لها تأثير أكبر.[28][29] تتضارب البيانات حول ما إذا كانت الستاتينات تقلل من خطر الإصابة بالفشل الكلوي.[27] الستاتينات، ومن بينها الأتورڤاستاتين، قبل جراحة القلب لا تقي إصابة الكلى الحادة.[30]
قبل إعطاء وسيط التباين (CM)، يمكن أن تقلل المعالجة المسبقة بالأتورڤاستاتين من خطر إصابة الكلى الحادة الناجمة عن التباين (CI-AKI) بين المرضى الذين يعانون من مرض الكلى المزمن الموجود مسبقًا (CKD) (eGFR أقل من 60 مل/دقيقة/ 1.73 م 2) والذين يخضعون لإجراءات تدخلية مثل قسطرة القلب وتصوير الأوعية التاجية (CAG) أو التدخل التاجي عن طريق الجلد (PCI).[31][32][33]
أكد التحليل الشمولي لـ 21 تجربة معشاة ذات شواهد أن جرعة عالية من الأتورڤاستاتين (80 ملگ) أكثر فعالية من الجرعة العادية أو العلاج بجرعة منخفضة من الستاتين في منع إصابة الكلى الحادة الناجمة عن التباين CI-AKI.[31] يمكن أن يساعد العلاج بالأتورڤاستاتين أيضًا في منع غسيل الكلى في المستشفى بعد إعطاء وسيط التباين، ومع ذلك لا يوجد دليل على أنه يقلل من الوفيات الناجمة عن جميع الأسباب المرتبطة بـ CI-AKI.[31][32][33][34]
العلاج
تمت تجربة الستاتينات (في الغالب السيمڤاستاتين) بالاشتراك مع الفايبريت لعلاج عسر دهون الدم لدى المرضى الذين يعانون أيضًا من سكري النمط 2، وخطر الإصابة بالأمراض القلبية الوعائية، ومع ذلك، هناك فائدة سريرية محدودة ملحوظة لمعظم النتائج القلبية الوعائية [35][36]
في حين أنه يجب إعطاء العديد من الستاتينات قبل النوم للحصول على أفضل تأثير، يمكن تناول الأتورڤاستاتين في أي وقت من اليوم، طالما يتم تناوله باستمرار مرة واحدة يوميًا في نفس الوقت.[37][38]
مجموعات سكانية محددة
- المسنون: تركيزات الأتورڤاستاتين في الپلازما لدى المسنين الأصحاء أعلى من تلك الموجودة لدى الشباب، وتشير البيانات السريرية إلى درجة أكبر من خفض الپروتين الدهني منخفض الكثافة عند أي جرعة للأشخاص مقارنة بالشباب.[2]
- الأطفال: لا تتوفر بيانات لحركة الدواء لهذه الفئة من الأشخاص.[2]
- النوع: تكون تركيزات الپلازما أعلى بشكل عام عند النساء منها عند الرجال، لكن لا يوجد فرق هام سريريًا في مدى انخفاض الپروتين الدهني منخفض الكثافة بين الرجال والنساء.[2]
- اعتلال الكلى: لا يوجد لأمراض الكلى أي تأثير ذي دلالة إحصائية على تركيزات الأتورڤاستاتين في الپلازما ويجب مراعاة اعتبارات تعديل الجرعة فقط في سياق الحالة الصحية العامة للمريض.[39][مصدر طبي غير موثق به][40][مصدر طبي غير موثق به]
- الديال الدموي: كانت هناك أدلة ذات جودة متوسطة إلى عالية لإظهار عدم وجود فوائد سريرية واضحة وهامة للستاتينات، بما في ذلك الأتورڤاستاتين ، في تقليل الاحتشاء القلبي الغير مميت، والسكتة الدماغية، والوفيات القلبية الوعائية لدى المرضى البالغين الذين يخضعون لغسيل الكلى (بما في ذلك مرضى السكري و/أو الأمراض القلبية الوعاية الموجودة مسبقًا) على الرغم من الانخفاض ذي الصلة سريريًا في مستويات الكولسترول الكلي/LDL.[41][مصدر طبي غير موثق به][42] ومع ذلك ، فقد كشف تحليل لاحق على الأتورڤاستاتين أنه قد يكون مفيدًا في تقليل المشكلات القلبية المشتركة والوفيات القلبية وجميع الأسباب لدى أولئك الذين لديهم مستوى مرتفع من كولسترول الپروتين الدهني منخفض الكثافة (LDL)> 3.75 ملي.مول/لتر.[43][مصدر طبي غير موثق به] بينما اقترحت دراسة SHARP أن الأدوية المخفضة لكولسترول الپروتين الدهني منخفض الكثافة (مثل مزيج الستاتين/إزتيميب) فعالة في الحد من مخاطر حالات تصلب الشرايين الرئيسية لدى مرضى الكلى بما في ذلك مرضى الديال الدموي، فإن تحليل المجموعة الفرعية لمرضى الديال الدموي لم يكشف عن أي فوائد هامة.[44][مصدر طبي غير موثق به] لم تتناول الدراسات ما إذا كان للغسيل الكلوي أي تأثير على مستويات الستاتين بشكل خاص في هذه التجارب الرئيسية.
- القصور الكبدي: يمكن ملاحظة زيادة مستويات الدواء لدى مرضى تليف الكبد المتقدم. يجب توخي احتياطات محددة للمرضى الذين يعانون من مرض الكبد الكحولي المزمن.[2] على الرغم من هذه المخاوف، فقد أظهرت مراجعة وتحليلات منهجية أجريت عام 2017 للأدلة المتاحة أن الستاتينات، مثل الأتورڤاستاتين، آمنة نسبيًا للاستخدام في حالة تليف الكبد المستقر بدون أعراض وقد تقلل حتى من خطر تطور أمراض الكبد والوفاة.[45]
موانع الاستخدام
- أمراض الكبد النشطة: الركود الصفراوي، الاعتلال الدماغي الكبدي، التهاب الكبد، واليرقان.
- الارتفاعات الغير مبررة في مستويات AST أو ALT.
- الحمل: قد يتسبب الأتورڤاستاتين في أضرار للجنين من خلال التأثير على مستويات الكولسترول والدهون الثلاثية في الدم، والتي تعتبر ضرورية لنمو الجنين.[2]
- الرضاعة الطبيعية: عُثر على كميات صغيرة من الستاتينات الأخرى تنتقل إلى حليب الأم، على الرغم من عدم دراسة الأتورڤاستاتين على وجه التحديد.[2] نظرًا لخطر تعطيل التمثيل الغذائي للدهون لدى الرضيع أثناء الرضاعة الطبيعية، لا يعتبر الأتورڤاستاتين مناسباً أثناء الرضاعة الطبيعية.[46]
- المستويات المرتفعة بشكل ملحوظ لـ CPK أو في حالة الاشتباه في الاعتلال العضلي أو تشخيصه بعد بدء تناول جرعات الأتورڤاستاتين. في حالات نادرة جداً قد يسبب الأتورڤاستاتين انحلال الربيدات،[47] وقد يكون خطيراً جداً مما يؤدي إلى إصابة الكلى الحادة بسبب البيلة الگلوبيينية. في حالة الاشتباه في انحلال الربيدات أو تشخيصه، يجب إيقاف العلاج بالأتورڤاستاتين فوراً.[48] تزداد احتمالية الإصابة بالاعتلال العضلي عن طريق العلاج المشترك بالسيكلوسپورين، مشتقات حمض الفيبريك، الإريثروميسين، النياسين والأزل المضاد للفطريات.[2]
الآثار الجانبية
الكبرى
- لوحظ سكري النمط الثاني في عدد قليل من الحالات، وهو تأثير غير شائع في جميع الستاتينات.[49][50][51] ومع ذلك، فإن فوائد العلاج بالستاتين في الوقاية من السكتات الدماغية المميتة وغير المميتة، وأمراض القلب التاجية القاتلة، والاحتشاء القلبي غير المميت كبيرة.[17] بالنسبة لمعظم الأشخاص، تفوق فوائد العلاج بالستاتينات خطر الإصابة بالسكري.[52] أظهر تحليل شمولي عام 2010 أن كل 255 شخصًا عولجوا ببالستاتين لأربع سنوات - حدث لديهم انخفاضاً قدره 5.4 من الاضطرابات رئيسية في الشريان التاجي وأدى إلى حدوث حالة واحدة جديدة فقط من مرض السكري.[52]
- هناك أدلة تشير إلى أن الآثار الجانبية مثل الاعتلال العضلي والألم العضلي من المرجح أن تحدث في المرضى الذين يتناولون جرعات أعلى من الأتورڤاستاتين إذا تم تناوله لفترة طويلة.[53][54] هناك أيضًا خطر متزايد محتمل للإصابة بانحلال الربيدات الناجم عن الستاتين عند تناول الستاتينات مع أدوية أخرى مصاحبة لفترة طويلة.[55] كما ذكرنا سابقًا، يجب إيقاف الأتورڤاستاتين فورًا في حالة حدوث ذلك.
- وُثقت شذوذات مستمرة في إنزيمات الكبد (ارتفاعات في الترانساميناسات الكبدية).[56] سُجلت ارتفاعات أكبر بثلاثة أضعاف من المعتاد في 0.5% من الأشخاص الذين عولجوا باستخدام أتورڤاستاتين
10 ملگم-80 ملگم بدلاً من الدواء الوهمي.[57] من المستحسن أن تُقيم وظائف الكبد من خلال الاختبارات المعملية قبل البدء في العلاج بالأتورڤاستاتين وتكرارها كما هو محدد سريريًا لاحقاً. إذا حدث دليل على إصابة الكبد الخطيرة أثناء تناول الأتورڤاستاتين، فيجب إيقافه وعدم إعادة تشغيله حتى تُحدد مسببات ضعف الكبد لدى الشخص. إذا لم يُعثر على سبب آخر، يجب إيقاف الأتورڤاستاتين بشكل دائم.[2]
الشائعة
ثبت أن ما يلي يحدث في 1-10% من الأشخاص الذين يتناولون الأتورڤاستاتين في التجارب السريرية:
- ألم المفاصل[2]
- الإسهال[2]
- سوء الهضم[2]
- ألم العضلات[2]
- الغثيان[2]
- ارتبط فرط سكر الدم بتناول جرعة عالية من الأتورڤاستاتين أيضاً بتدهور السيطرة على سكر الدم.[58][59]
أخرى
الوظائف الإدراكية
هناك تقارير نادرة عن فقدان الذاكرة القابل للعكس والارتباك مع جميع الستاتينات، بما في ذلك الأتورڤاستاتين. ومع ذلك، لم يكن هناك دليل كافٍ لربط استخدام الستاتين بالضعف الإدراكي، ومن المحتمل أن تكون مخاطر الإدراك تفوقها الآثار المفيدة للالتزام بالعلاج الستاتين في الأمراض القلبية الوعائية والوعائية الدماغية.[60][61][62][63]
التهاب الپنكرياس
هناك بعض الأدلة على أن استخدام الأتورڤاستاتين قد يزيد من خطر الإصابة بالتهاب الپنكرياس الحاد لدى الأشخاص المعرضين بالفعل لخطر أكبر.[64][65] ومع ذلك، هناك أيضًا دليل على أن استخدام الأتورڤاستاتين يقلل من خطر الإصابة بالتهاب الپنكرياس الحاد لدى الأشخاص المصابين بفرط دهون الدم الخفيف إلى المتوسط، عن طريق خفض مستويات الدهون الثلاثية.[65]
ضعف الانتصاب
يبدو أن للستاتينات أثراً إيجابياً على ضعف الانتصاب.[66][67]
التداخلات الدوائية
الفايبرات هي فئة من الأدوية يمكن استخدامها لعلاج فرط دهون الدم الحاد أو المختلط المقاوم للحرارة كعلاج مركب مع الستاتينات أو كعلاج أحادي. يمكن أن يؤدي العلاج المتزامن مع الأتورڤاستاتين بأدوية من فئة الفايبرات (مثل الگمفبروزيل، الفينوفيبرات) إلى زيادة خطر الاعتلال العضلي وانحلال الربيدات.[68][69][70][71]
العلاج المشترك بالأتورڤاستاتين وأحد مثبطات CYP3A4 مثل الإيتراكونازول،[72] التليثرومايسين والڤوريكونازول، قد يزيد من تركيزات الأتورڤاستاتين في الدم، مما قد يؤدي إلى تفاعلات خطرة. يقل احتمال حدوث ذلك مع مثبطات CYP3A4 الأخرى مثل الديلتيازيم، الإريثرومايسين، الفلوكونازول، الكيتوكونازول، الكلاريثرومايسين، السيكلوسپورين، مثبطات الإنزيم الپروتيني، أو الڤراپاميل،[73] ونادراً مع مثبطات CYP3A4 الأخرى، مثل الأميودارون والأپريپيتانت.[48] في كثير من الأحيان، يمكن أن يقلل البوسنتان والفوسفنيتوين والفنيتوين، وهي محفزات لإنزيم CYP3A4، من تركيزات الأتورڤاستاتين في الپلازما. نادرًا ما يكون الباربيتورات والكاربامازيپين والإيفاڤيرنز والنڤيراپين والأوكسكاربازپين والريفامپين والريفامايسين،[74] والتي تعتبر من محفزات إنزيم CYP3A4، يمكن أن تقلل من تركيزات الأتورڤاستاتين في الپلازما. موانع الحمل الفموية زادت من قيم AUC للنوريثيستيرون وإيثينيل الإستراديول؛ يجب أخذ هذه الزيادات في الاعتبار عند اختيار موانع الحمل الفموية للنساء اللاتي يعالجن بالأتورڤاستاتين.[2]
نادرًا ما يمكن لمضادات الحموضة أن تقلل من تركيزات الستاتينات في الپلازما، ولكنها لا تؤثر على كولسترول الپروتين الدهني منخفض الكثافة- تخفيض الفعالية.[75]
ثبت أيضًا أن النياسين يزيد من خطر الإصابة بالاعتلال العضلي أو انحلال الربيدات.[48]
قد تغير بعض الستاتينات أيضاً تركيزات الأدوية الأخرى، مثل الوارفارين أو الديجوكسين، مما يؤدي إلى حدوث تغييرات في التأثير أو الحاجة إلى المراقبة السريرية.[48] الزيادة في مستويات الديجوكسين بسبب الأتورڤاستاتين هي ارتفاع بمقدار 1.2 ضعف في المنطقة الواقعة تحت المنحنى (AUC)، مما يؤدي إلى تفاعل دوائي-دوائي ثانوي. تنص جمعية القلب الأمريكية على أن الجمع بين الديجوكسين والأتورڤاستاتين معقول.[76] على عكس بعض الستاتينات الأخرى، لا يتفاعل الأتورڤاستاتين مع تركيزات الوارفارين بطريقة هامة سريريًا (على غرار الپيتاڤاستاتين).[76]
تقلل مكملات ڤيتامين د الأتورڤاستاتين وتركيزات المستقلب النشط، ومع ذلك فهي تقلل الپروتين الدهني منخفض الكثافة وتركيزات الكولسترول الكلية تآزرياً.[77]
من المعروف أن عصير جريب فروت من مثبطات CYP3A4 المعوية. شرب عصير الجريب فروت مع الأتورڤاستاتين قد يسبب زيادة في Cmax والمنطقة الواقعة تحت المنحنى (AUC). أثارت هذه النتيجة في البداية مخاوف من السمية، وفي عام 2000، أوصى الأشخاص الذين يتناولون الأتورڤاستاتين بعدم تناول عصير الجريب فروت "بشكل غير خاضع للرقابة".[78]
أظهرت الدراسات الصغرى (باستخدام المشاركين الشباب في الغالب) التي تدرس آثار تناول عصير الجريب فروت على الجرعات المنخفضة من الستاتينات، بشكل رئيسي الأتورڤاستاتين، أن عصير الجريب فروت يزيد من مستويات الأتورڤاستاتين في الدم، مما قد يزيد من مخاطر الآثار الجانبية.[79][80][81]لم تتضمن أي دراسات تقيم تأثير استهلاك عصير الجريب فروت المشاركين الذين يتناولون أعلى جرعة من الأتورڤاستاتين (80 ملگم/يومياً)،[79][80][81] والتي غالبًا ما توصف للأشخاص الذين لديهم تاريخ من الأمراض القلبية الوعائية (مثل النوبة القلبية أو السكتة الدماغية الإقفارية) أو للأشخاص المعرضين لخطر الإصابة بالأمراض القلبية الوعائية. يجب على الأشخاص الذين يتناولون الأتورڤاستاتين استشارة الطبيب أو الصيدلي قبل تناول عصير الجريب فروت، حيث أن تأثيرات تناول عصير الجريب فروت على الأتورڤاستاتين ستختلف وفقًا لعوامل مثل كمية وتكرار استهلاك العصير بالإضافة إلى الاختلافات في مكونات العصير وجودته وطريقة تناوله وتحضيره بحسب العلامات التجارية المختلفة.[82]
أُفيد عن حالات قليلة من الاعتلال العضلي عند الجمع بين الأتورڤاستاتين والكولشيسين.[2]
آلية العمل
كما هو الحال مع الستاتينات الأخرى، يعتبر الأتورفاستاتين مثبط منافس لــ HMG-CoA reductase. على عكس معظم المثبطات الأرخرى، فهو مركب مخلق بالكامل. يحفز HMG-CoA reductase اختزال 3-hydroxy-3-methylglutaryl-coenzyme A (HMG-CoA) إلى مڤالونات، وهي خطوة تحديد المعدل في تخليق الكولسترول الحيوي بالكبد. تثبيط الإنزيم يقلل من تخليق الكولسترول، مما يزيد من التعبير عن مستقبلات الپروتين الدهني منخفض الكثافة (مستقبلات LDL في الخلايا الكبدية. يزيد هذا من امتصاص الخلايا الكبدية للپروتين الدهني منخفض الكثافة، مما يقلل من كمية الكولسترول الضار في الدم. مثل الستاتينات الأخرى، يقلل الأتورفاستاتين أيضاً من مستويات الدهون الثلاثية في الدم ويزيد بشكل طفيف من مستويات كولسترول الپروتين الدهني مرتفع الكثافة (الكولسترول النافع).
لدى الأشخاص الذين يعانون من متلازمة الشريان التاجي الحادة، قد يلعب العلاج بجرعات عالية من الأتورفاستاتين دوراً في تثبيت الترسبات.[83][84] عند تناول جرعات عالية، يكون للستاتينات تأثيرات مضادة للالتهابات، وتحرض على تقليل الطبقة اللوحية النخرية، وتحسن وظيفة البطانة، مما يؤدي إلى استقرار اللويحة، وأحيانًا تراجعها.[84][83] هناك عملية تفكير مماثلة باستخدام جرعة عالية من الأتورفاستاتين كشكل من أشكال الوقاية من تكرار السكتة الدماغية الثانوية.[85][86][87]
الديناميكية الدوائية
الكبد هو الموقع الرئيسي لعمل الأتورفاستاتين، حيث أن هذا هو الموقع الرئيسي لتخليق الكولسترول وتصفية الپروتين الدهني منخفض الكثافة. جرعة الأتورفاستاتين، بدلاً من تركيز الدواء الجهازي، ترتبط بمدى تتقليل كولسترول الپروتين الدهني منخفض الكثافة.[2] جرعة أتورفاستاتين بمقدار يتراوح من 10-80 ملگ/يومياً، تخفض الكولسترول الكلي بنسبة 27.0% إلى 37.9%، وتخفض كولسترول الپروتين الدهني منخفض الكثافة بنسبة 37.1% إلى 51.7% والدهون الثلاثية بنسبة 18.0% إلى 28.3%.[88]
الحركة الدوائية
الامتصاص
يُمتص الأتورڤاستاتين بشكل سريع عند تناوله عن طريق الفم، ليصل لأقصى تركيز له في الپلازما في غضون 1-2 ساعة تقريباً. يبلغ التوافر الحيوي المطلق للدواء حوالي 14%، لكن التوافر الجهازي لنشاط HMG-CoA reductase يقارب 30%. يخضع الأتورڤاستاتين لإخراج معوي وتمثيل غذائي مرتفع، وهو السبب الرئيسي لضعف التوافر الجهازي. يؤدي تناول الأتورڤاستاتين مع الطعام إلى انخفاض بنسبة 25% في Cmax (معدل الامتصاص) وانخفاض بنسبة 9% في AUC (مدى الامتصاص)، على الرغم من أن الطعام لا يؤثر على كولسترول الپروتين الدهني منخفض الكثافة في الپلازما- خفض فعالية الأتورڤاستاتين. من المعروف أن الجرعة الدوائية المسائية تقلل معدل ومدى الامتصاص بنسبة 30% لكل منهما. إلا أن توقيت تناول الدواء لا يؤثر على كفاءة تخفيض كولسترول الپروتين الدهني منخفض الكثافة في الپلازما للأتورڤاستاتين.
الانتشار
متوسط حجم انتشار الأتورڤاستاتين حوالي 381 لترًا وهو مرتبط بدرجة كبيرة بالپروتين (98%)، وقد أظهرت الدراسات أنه من المحتمل أن يُفرز في لبن الأم.
الاستقلاب
يُستقلب الأتورفاستاتين بشكل أساسي عن طريق هدرلة سيتوكروم پي450 3A4 لتشكيل مستلبات ortho- and parahydroxylated النشطة، بالإضافة إلى مستقبلات أكسدة-بيتا. مستقلبات ortho- and parahydroxylated هي المسئولة عن 70% من نشاط HMG-CoA reductase الجهازي. وكذلك نواتج أكسدة بيتا مختلفة. مستقلبات ortho- وparahydroxylated هي المسؤولة عن 70٪ من النشاط الجهازي اختزال HMG-CoA. تخضع هذه المستقلبات دورها لاستقلاب آخر عن طريق الاقتران الگلوكوروني. كركيزة لإيزوزيم CYP3A4، فقد أظهر قابلية لمثبطات ومحفزات CYP3A4 لإنتاج تركيزات پلازما متزايدة أو منخفضة، على التوالي. خضع هذا التفاعل للاختبار المعملي مع الإعطاء المتزامن للإريثروميسين، وهو أحد مثبطات إنزيم CYP3A4 المعروفة، مما أدى إلى زيادة تركيزات الأتورفاستاتين في الپلازما . وهو أيضًا مثبط لسيتوكروم 3A4.
الإفراز
يتم التخلص من الأتورڤاستاتين بشكل أساسي عن طريق الإفرازات الكبدية المرارية، مع خروج أقل من 2% عن طريق البول. تتبع العصارة المرارية التخلص من الأيض الكبدي و/أو خارج الكبد. لا يبدو أن هناك أي إعادة تدوير معوية كبدية. يبلغ نصف عمر إطراح الأتورڤاستاتين 14 ساعة تقريباً. من الجدير بالذكر، أن النشاط التثبيطي لانزيم HMG-CoA يبدو أن نصف عمره من 20 إلى 30 ساعة، والذي يُعتقد أنه ناتج عن المستقلبات النشطة. الأتورڤاستاتين هو أيضًا ركيزة في ناقل تدفق پ-الپروتين الدهني المعوي، والذي يضخ الدواء مرة أخرى إلى تجويف الأمعاء أثناء امتصاص الدواء.[48]
في حالات القصور الكبدي، تتأثر تركيزات الأتورفاستاتين في الپلازما بشكل كبير بمرض الكبد المتزامن. يُظهر الأشخاص المصابون بمرض الكبد من مرحلة Child-Pugh A زيادة بمقدار أربعة أضعاف في كل من Cmax وAUC. يُظهر الأشخاص المصابون بمرض الكبد في المرحلة B لدى الطفل زيادة بمقدار 16 ضعفًا في Cmax وزيادة بمقدار 11 ضعفًا في AUC.
كبار السن (> 65 عامًا) أظهروا تغيرًا في الحرائك الدوائية للأتورفاستاتين مقارنةً بالشباب، مع متوسط قيم AUC وCmax أعلى بنسبة 40% و30% على التوالي. بالإضافة إلى ذلك، يظهر كبار السن الأصحاء استجابة ديناميكية دوائية أكبر للأتورفاستاتين بأي جرعة؛ لذلك، قد يكون لدى هؤلاء السكان جرعات أقل فعالية.[2]
علم الأدوية الوراثية
قد ترتبط العديد من تعدد الأشكال بزيادة الآثار الجانبية المرتبطة بالستاتينات مع تعدد أشكال النوكليوتيدات المفردة (SNPs) في جين SLCO1B1 مما يُظهر حدوث الاعتلال العضلي المرتبط بالستاتين بمعدل 45 ضعفاً[89] عن الأشخاص الذين ليس لديهم تعدد أشكال وراثي.
هناك العديد من الدراسات التي تظهر المتغيرات الوراثية والاستجابة المتغيرة للأتورفاستاتين.[90][91] كانت الأشكال المتعددة التي أظهرت أهمية كبيرة للجينوم بين سكان القوقاز هي تعدد الأشكال في المنطقة apoE؛ rs445925،[90] rs7412،[90][91] rs429358[91] وrs4420638[90] الذين أظهروا استجابة متغيرة لكولسترول الپروتين الدهني منخفض الكثافة اعتمادًا على التركيب الوراثي عند معالجتهم بالأتورفاستاتين.[90][91] المتغير الوراثي الآخر الذي أظهر أهمية كبيرة للجينوم بين سكان القوقاز هو SNP rs10455872 في جين LPA الذي يؤدي إلى مستويات Lp (a) أعلى والتي تسبب استجابة لكولسترول الپروتين الدهني منخفض الكثافة منخفضة بشكل واضع للأتورفاستاتين.[90] كانت هذه الدراسات على سكان القوقاز، ويجب إجراء المزيد من الأبحاث مع مجموعة كبيرة من العرقيات المختلفة لتحديد المزيد من الأشكال المتعددة التي يمكن أن تؤثر على الحرائك الدوائية للأتورفاستاتين والاستجابة للعلاج.[90]
التخليق الكيميائي

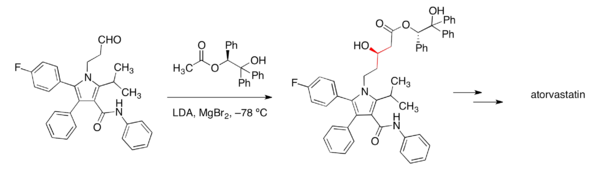
أول تخليق لأتورفاستاتين كان في شركة پارك-ديڤس، والذي حدث أثناء اكتشاف الدواء، كان تخليقاً راسمياً متبوعاً بفصل استشرابي للمتماكبات المتقابلة. استخدم المسار الانتقائي المتماثل المبكر إلى أتورفاستاتين مساعداً كيرالياً من الإستر لإعداد الكيمياء الفراغية للمجموعة الأولى من المجموعتين الوظيفيتين للكحول عن طريق تفاعل ألدول انتقائي التماكب.[92][93]
بمجرد دخول المركب مرحلة التطوير قبل السريري، طوّرت كيمياء العمليات تخليقاً فعالاً من حيث التكلفة وقابلية للتطوير.[92] في حالة الأتورفاستاتين، كان أحد العناصر الأساسية للتخليق الكلي هو ضمان النقاء الكيميائي الفراغي في مادة الدواء النهائية، ولذلك أصبح إنشاء أول مركز فراغي جانباً رئيسياً في التصميم العام. اعتمد الإنتاج التجاري النهائي للأتورفاستاتين على مقاربة المجمع الكيرالي، حيث أُجريت الكيمياء الفراغية لأول مجموعة وظيفية كحولية أثناء التخليق - من خلال اختيار حمض السكوربيك الأحادي، وهو منتج طبيعي غير مكلف مشتق من النباتات.[92][94]
يحتوي مركب "الكالسيوم أتورفاستاتين" على اثنين من أيونات الأتورفاستاتين، وأيون كالسيوم وثلاثة جزيئات ماء.[95]
التاريخ
بروس روث، الذي عينته شركة وارنر-لامبرت ككيميائي عام 1982، قام بتصنيع "مركب تجريبي" يحمل الاسم الرمزي CI 981 - أطلق عليه لاحقًا أتورڤاستاتين.[96][97] صُنع لأول مرة في أغسطس 1985.[92][96][98][99][100] كانت إدارة شركة وارنر-لامبرت قلقة من أن الأتورڤاستاتين كان نسخة شبيهة لدواء شركة مرك اليتيم الذي يحمل اسم لوڤاستاتين (يبتاع تحت الاسم التجاري مڤاكور). كان مڤاكور، الذي تم تسويقه لأول مرة عام 1987، أول ستاتين مُصنع ونسخة سيماڤاستاتين التي ولفتتها مرك- في مراحل متقدمة من التطوير.[97] ومع ذلك، أقنع بروس روث ورؤسائه، روجر نيوتن ورونالد كرسويل، عام 1985، المديرين التنفيذيين للشركة بنقل المركب إلى مرحلة التجارب السريرية باهظة الثمن. أظهرت النتائج المبكرة التي قارنت الأتورڤاستاتين مع السيماڤاستاتين أن الأتورڤاستاتين بدا أكثر فعالية مع آثار جانبية أقل.[97]
عام 1994، نُشرت نتائج دراسة مولتها شركة مرك في مجلة "ذا لانست" خلصت إلى فاعلية الستاتينات في خفض الكولسترول وأثبتت للمرة الأولى أن "الستاتين" يقلل الكوليسترول الضار "LDL" ولكن كما أدى إلى انخفاض حاد في النوبات القلبية القاتلة بين المصابين بأمراض القلب".[97][101]
عام 1996، أبرمت شركة وارنر-لامبرت اتفاقية تسويق مشترك مع شركة فايزر لبيع ليبپتور. وفي عام 2000 استحوذت فايزر على شركة وارنر-لامبرت مقابل 90.2 مليار دولار.[102][92][98][99] بدأ طرح ليپيتور في الأسواق عام 1996.[100][103] بحلول عام 2003، أصبح ليبپتور أكثر الأدوية مبيعًا في الولايات المتحدة.[96] من عام 1996 حتى 2012، تحت الاسم التجاري ليپيتور، أصبح الأتورڤاستاتين الدواء الأكثر مبيعًا في العالم على الإطلاق، حيث بلغت مبيعاته أكثر من 125 مليار دولار أمريكي على مدار 14.5 سنة تقريباً.[104] و13 بليون دولار سنوياً في ذروة مبيعاته،[105] يدر الليپيتور بمفرده "أكثر من ربع الدخل السنوي لفايزر منذ سنوات".[104]
انتهت براءة اختراع فايزر للأتورڤاستاتين في نوفمبر 2011.[106]
المجتمع والثقافة
الاقتصاد
سعر الأتورڤاستاتين رخيص نسبياً.[6] بموجب أحكام قانون حماية المريض والرعاية الميسرة (PPACA) في الولايات المتحدة، قد تغطي خطط الرعاية الصحي تكاليف أتورڤاستاتين 10 ملگم و20 ملگم للبالغين الذين تتراوح أعمارهم بين 40 و75 عامًا بناءً على توصيات فريق عمل الخدمات الوقائية (USPSTF).[107][108][109] هناك بعض الخطط تغطي فقط الستاتينات الأخرى.[110][111]
الأسماء التجارية
تُباع أقراص أتورڤاستاتين كالسيوم تحت الاسم التجاري ليپيتور.[112] كما تُصنع فايزر الدواء في عبوات تحتوي على الأتورڤاستاتين مع أدوية أخرى لعلاجات أخرى، مثل أتورڤاستاتين/أملوديپين.[113]
انتهت براءة اختراع فايزر الولايات المتحدة لليپيتور في 30 نوفمبر.[114] في البداية، كانت واطسون للصناعات الدوائية ومختبرات رانباكسي الهندية تُصنعان فقط أتورڤاستاتين المكافيء. لم تنخفض أسعار النسخة المكافئة إلى مستوى الأدوية المكافئة الأخرى - 10 دولار أو أقل للعلاج مدة شهر- حتى بدأ المصنعون الآخرون في توفير الدواء في مايو 2012.[115]
في بلدان أخر، يُصنع أتورڤاستاتين كالسيوم على شكل أقراص بواسطة صانعي الأدوية المكافئة تحت أسماء تجارية مختلفة بما في ذلك أتوريس، أتورليپ، أتورڤا، أتورڤاستاتين تـِڤا، أتورڤاستاتين پارك-ديڤيز، أڤاس، كارديل، ليپريمار، ليتورڤا، ماكتور، أوربيوس، پرڤنكور، سورتيس، ستاتور، تاهور، توريد، تورڤاكارد، تورڤاست، توتاليپ، توليپ، إكسراتور، وزاراتور.[116][117] كما تُصنع فايزر نسختها المكافئة تحت اسم زاراتور.[118]
سحب الدواء
في 9 نوفمبر 2012، سحبت شركة مختبرات رانباكسي الهندية للأدوية طواعية جرعات 10 و20 و40 ملگ من نسختها المكافئة من أتورڤاستاتين في الولايات المتحدة.[119][120][121] تم سحب كميات كبيرة من الأتورڤاستاتين، المعبأ في زجاجات من 90 و500 قرص، بسبب التلوث المحتمل بجزيئات زجاجية صغيرة للغاية في حجم حبة الرمل (أقل من 1 ملم). لم تتلق إدارة الغذاء والدواء الأمريكية أي تقارير عن الإصابة من التلوث.[119] أصدرت شركة رانباكسي كذلك قراراً بسحب زجاجات أقراص 10 ملگ في أغسطس 2012 ومارس 2014، بسبب مخاوف من أن الزجاجات قد تحتوي على أقراص بتركيز 20 ملگ وبالتالي تسبب خطاً في الجرعة.[122][123]
المصادر
- ^ أ ب "Atorvastatin (Lipitor) Use During Pregnancy". Drugs.com. 3 February 2020. Archived from the original on 4 December 2019. Retrieved 26 February 2020.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ "Lipitor- atorvastatin calcium tablet, film coated". DailyMed. Archived from the original on 26 November 2020. Retrieved 26 February 2020.
- ^ أ ب ت ث ج ح خ د ذ "Atorvastatin Calcium Monograph for Professionals". Drugs.com. AHFS. Archived from the original on 25 October 2010. Retrieved 23 December 2018.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. p. 473. ISBN 9783527607495. Archived from the original on 12 January 2023. Retrieved 10 May 2020.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ أ ب Hitchings A, Lonsdale D, Burrage D, Baker E (2014). The Top 100 Drugs e-book: Clinical Pharmacology and Practical Prescribing. Elsevier Health Sciences. p. 197. ISBN 978-0-7020-5515-7. Archived from the original on 26 February 2023. Retrieved 27 June 2022.
- ^ "The Top 300 of 2020". ClinCalc. Archived from the original on 18 March 2020. Retrieved 7 October 2022.
- ^ "Atorvastatin - Drug Usage Statistics". ClinCalc. Archived from the original on 8 October 2022. Retrieved 7 October 2022.
- ^ "Atorvastatin Calcium". American Society of Health-System Pharmacists. Archived from the original on 25 October 2010. Retrieved 3 April 2011.
- ^ أ ب ت McCrindle BW, Ose L, Marais AD (July 2003). "Efficacy and safety of atorvastatin in children and adolescents with familial hypercholesterolemia or severe hyperlipidemia: a multicenter, randomized, placebo-controlled trial". The Journal of Pediatrics. 143 (1): 74–80. doi:10.1016/S0022-3476(03)00186-0. PMID 12915827.
- ^ Nissen SE, Nicholls SJ, Sipahi I, Libby P, Raichlen JS, Ballantyne CM, et al. (April 2006). "Effect of very high-intensity statin therapy on regression of coronary atherosclerosis: the ASTEROID trial". JAMA. 295 (13): 1556–65. doi:10.1001/jama.295.13.jpc60002. PMID 16533939.
- ^ Nawrocki JW, Weiss SR, Davidson MH, Sprecher DL, Schwartz SL, Lupien PJ, et al. (May 1995). "Reduction of LDL cholesterol by 25% to 60% in patients with primary hypercholesterolemia by atorvastatin, a new HMG-CoA reductase inhibitor". Arteriosclerosis, Thrombosis, and Vascular Biology. 15 (5): 678–82. doi:10.1161/01.ATV.15.5.678. PMID 7749881.
- ^ Bakker-Arkema RG, Davidson MH, Goldstein RJ, Davignon J, Isaacsohn JL, Weiss SR, et al. (January 1996). "Efficacy and safety of a new HMG-CoA reductase inhibitor, atorvastatin, in patients with hypertriglyceridemia". JAMA. 275 (2): 128–33. doi:10.1001/jama.1996.03530260042029. PMID 8531308.
- ^ Ozaki K, Kubo T, Imaki R, Shinagawa H, Fukaya H, Ohtaki K, et al. (August 2006). "The anti-atherosclerotic effects of lipid lowering with atorvastatin in patients with hypercholesterolemia". Journal of Atherosclerosis and Thrombosis. 13 (4): 216–9. doi:10.5551/jat.13.216. PMID 16908955.
- ^ Marais AD, Firth JC, Bateman ME, Byrnes P, Martens C, Mountney J (August 1997). "Atorvastatin: an effective lipid-modifying agent in familial hypercholesterolemia". Arteriosclerosis, Thrombosis, and Vascular Biology. 17 (8): 1527–31. doi:10.1161/01.ATV.17.8.1527. PMID 9301631.
- ^ Rossi S, ed. (2006). Australian medicines handbook 2006. Adelaide, S. Aust: Australian Medicines Handbook Pty Ltd. ISBN 978-0-9757919-2-9.
- ^ أ ب Sever PS, Dahlöf B, Poulter NR, Wedel H, Beevers G, Caulfield M, et al. (April 2003). "Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower-than-average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial—Lipid Lowering Arm (ASCOT-LLA): a multicentre randomised controlled trial". Lancet. 361 (9364): 1149–58. doi:10.1016/S0140-6736(03)12948-0. PMID 12686036. S2CID 9409142.
- ^ Law MR, Wald NJ, Rudnicka AR (June 2003). "Quantifying effect of statins on low density lipoprotein cholesterol, ischaemic heart disease, and stroke: systematic review and meta-analysis". BMJ. 326 (7404): 1423–0. doi:10.1136/bmj.326.7404.1423. PMC 162260. PMID 12829554.
- ^ Wilson PW, D'Agostino RB, Levy D, Belanger AM, Silbershatz H, Kannel WB (May 1998). "Prediction of coronary heart disease using risk factor categories". Circulation. 97 (18): 1837–47. doi:10.1161/01.CIR.97.18.1837. PMID 9603539.
- ^ Jones P, Kafonek S, Laurora I, Hunninghake D (March 1998). "Comparative dose efficacy study of atorvastatin versus simvastatin, pravastatin, lovastatin, and fluvastatin in patients with hypercholesterolemia (the CURVES study)". The American Journal of Cardiology. 81 (5): 582–7. doi:10.1016/S0002-9149(97)00965-X. PMID 9514454.
- ^ Colhoun HM, Betteridge DJ, Durrington PN, Hitman GA, Neil HA, Livingstone SJ, et al. (2004). "Primary prevention of cardiovascular disease with atorvastatin in type 2 diabetes in the Collaborative Atorvastatin Diabetes Study (CARDS): multicentre randomised placebo-controlled trial". Lancet. 364 (9435): 685–96. doi:10.1016/S0140-6736(04)16895-5. PMID 15325833. S2CID 28885209.
- ^ Neil HA, DeMicco DA, Luo D, Betteridge DJ, Colhoun HM, Durrington PN, et al. (November 2006). "Analysis of efficacy and safety in patients aged 65–75 years at randomization: Collaborative Atorvastatin Diabetes Study (CARDS)". Diabetes Care. 29 (11): 2378–84. doi:10.2337/dc06-0872. PMID 17065671.
- ^ Gentile S, Turco S, Guarino G, Sasso CF, Amodio M, Magliano P, et al. (December 2000). "Comparative efficacy study of atorvastatin vs simvastatin, pravastatin, lovastatin and placebo in type 2 diabetic patients with hypercholesterolaemia". Diabetes, Obesity & Metabolism. 2 (6): 355–62. doi:10.1046/j.1463-1326.2000.00106.x. PMID 11225965. S2CID 27148191.
- ^ أ ب Banach M, Serban C, Sahebkar A, Mikhailidis DP, Ursoniu S, Ray KK, et al. (September 2015). "Impact of statin therapy on coronary plaque composition: a systematic review and meta-analysis of virtual histology intravascular ultrasound studies". BMC Medicine. 13 (1): 229. doi:10.1186/s12916-015-0459-4. PMC 4575433. PMID 26385210.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ أ ب ت Nicholls SJ, Ballantyne CM, Barter PJ, Chapman MJ, Erbel RM, Libby P, et al. (December 2011). "Effect of two intensive statin regimens on progression of coronary disease". The New England Journal of Medicine. 365 (22): 2078–87. doi:10.1056/NEJMoa1110874. PMID 22085316.
- ^ أ ب ت Nissen SE, Tuzcu EM, Schoenhagen P, Brown BG, Ganz P, Vogel RA, et al. (March 2004). "Effect of intensive compared with moderate lipid-lowering therapy on progression of coronary atherosclerosis: a randomized controlled trial". JAMA. 291 (9): 1071–80. doi:10.1001/jama.291.9.1071. PMID 14996776.
- ^ أ ب Su X, Zhang L, Lv J, Wang J, Hou W, Xie X, Zhang H (June 2016). "Effect of Statins on Kidney Disease Outcomes: A Systematic Review and Meta-analysis". American Journal of Kidney Diseases. 67 (6): 881–892. doi:10.1053/j.ajkd.2016.01.016. PMID 26905361.
- ^ أ ب Geng Q, Ren J, Song J, Li S, Chen H (August 2014). "Meta-analysis of the effect of statins on renal function". The American Journal of Cardiology. 114 (4): 562–570. doi:10.1016/j.amjcard.2014.05.033. PMID 25001155.
- ^ أ ب Amarenco P, Callahan A, Campese VM, Goldstein LB, Hennerici MG, Messig M, et al. (October 2014). "Effect of high-dose atorvastatin on renal function in subjects with stroke or transient ischemic attack in the SPARCL trial". Stroke. 45 (10): 2974–2982. doi:10.1161/STROKEAHA.114.005832. PMID 25147328. S2CID 6575836.
- ^ Xiong B, Nie D, Cao Y, Zou Y, Yao Y, Qian J, et al. (November 2017). "Preoperative Statin Treatment for the Prevention of Acute Kidney Injury in Patients Undergoing Cardiac Surgery: A Meta-Analysis of Randomised Controlled Trials". Heart, Lung & Circulation. 26 (11): 1200–1207. doi:10.1016/j.hlc.2016.11.024. PMID 28242291.
- ^ أ ب ت Zhou X, Dai J, Xu X, Wang Z, Xu H, Chen J, et al. (April 2019). "Comparative Efficacy of Statins for Prevention of Contrast-Induced Acute Kidney Injury in Patients With Chronic Kidney Disease: A Network Meta-Analysis". Angiology. 70 (4): 305–316. doi:10.1177/0003319718801246. PMID 30261736. S2CID 52875826.
- ^ أ ب Ma WQ, Zhao Y, Wang Y, Han XQ, Zhu Y, Liu NF (June 2018). "Comparative efficacy of pharmacological interventions for contrast-induced nephropathy prevention after coronary angiography: a network meta-analysis from randomized trials" (PDF). International Urology and Nephrology. 50 (6): 1085–1095. doi:10.1007/s11255-018-1814-0. PMID 29404930. S2CID 3295220. Archived (PDF) from the original on 30 November 2020. Retrieved 9 May 2020.
- ^ أ ب Cho A, Lee YK, Sohn SY (March 2020). "Beneficial effect of statin on preventing contrast-induced acute kidney injury in patients with renal insufficiency: A meta-analysis". Medicine. 99 (10): e19473. doi:10.1097/MD.0000000000019473. PMC 7478506. PMID 32150109.
- ^ Zhang J, Guo Y, Jin Q, Bian L, Lin P (October 2018). "Meta-analysis of rosuvastatin efficacy in prevention of contrast-induced acute kidney injury". Drug Design, Development and Therapy. 12: 3685–3690. doi:10.2147/DDDT.S178020. PMC 6216974. PMID 30464400.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Keech A, Simes RJ, Barter P, Best J, Scott R, Taskinen MR, et al. (November 2005). "Effects of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial". Lancet. 366 (9500): 1849–1861. doi:10.1016/S0140-6736(05)67667-2. PMID 16310551. S2CID 40744740.
- ^ Ginsberg HN, Elam MB, Lovato LC, Crouse JR, Leiter LA, Linz P, et al. (April 2010). "Effects of combination lipid therapy in type 2 diabetes mellitus". The New England Journal of Medicine. 362 (17): 1563–1574. doi:10.1056/NEJMoa1001282. PMC 2879499. PMID 20228404.
- ^ Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) (16 May 2001). "Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP]". JAMA. 285 (19): 2486–2497. doi:10.1001/jama.285.19.2486. PMID 11368702.
- ^ Grundy SM, Cleeman JI, Merz CN, Brewer HB, Clark LT, Hunninghake DB, et al. (July 2004). "Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines". Circulation. 110 (2): 227–39. doi:10.1161/01.CIR.0000133317.49796.0E. PMID 15249516.
- ^ Lins RL, Matthys KE, Verpooten GA, Peeters PC, Dratwa M, Stolear JC, Lameire NH (May 2003). "Pharmacokinetics of atorvastatin and its metabolites after single and multiple dosing in hypercholesterolaemic haemodialysis patients". Nephrology, Dialysis, Transplantation. 18 (5): 967–976. doi:10.1093/ndt/gfg048. PMID 12686673.
- ^ Stern RH, Yang BB, Horton M, Moore S, Abel RB, Olson SC (September 1997). "Renal dysfunction does not alter the pharmacokinetics or LDL-cholesterol reduction of atorvastatin". Journal of Clinical Pharmacology. 37 (9): 816–819. doi:10.1002/j.1552-4604.1997.tb05629.x. PMID 9549635. S2CID 752038.
- ^ Wanner C, Krane V, März W, Olschewski M, Mann JF, Ruf G, Ritz E (July 2005). "Atorvastatin in patients with type 2 diabetes mellitus undergoing hemodialysis". The New England Journal of Medicine. 353 (3): 238–48. doi:10.1056/NEJMoa043545. PMID 16034009.
- ^ Fellström BC, Jardine AG, Schmieder RE, Holdaas H, Bannister K, Beutler J, et al. (April 2009). "Rosuvastatin and cardiovascular events in patients undergoing hemodialysis". The New England Journal of Medicine. 360 (14): 1395–407. doi:10.1056/NEJMoa0810177. PMID 19332456.
- ^ März W, Genser B, Drechsler C, Krane V, Grammer TB, Ritz E, et al. (June 2011). "Atorvastatin and low-density lipoprotein cholesterol in type 2 diabetes mellitus patients on hemodialysis". Clinical Journal of the American Society of Nephrology. 6 (6): 1316–25. doi:10.2215/CJN.09121010. PMC 3109927. PMID 21493741.
- ^ Baigent C, Landray MJ, Reith C, Emberson J, Wheeler DC, Tomson C, et al. (June 2011). "The effects of lowering LDL cholesterol with simvastatin plus ezetimibe in patients with chronic kidney disease (Study of Heart and Renal Protection): a randomised placebo-controlled trial". Lancet. 377 (9784): 2181–92. doi:10.1016/S0140-6736(11)60739-3. PMC 3145073. PMID 21663949.
- ^ Kim RG, Loomba R, Prokop LJ, Singh S (October 2017). "Statin Use and Risk of Cirrhosis and Related Complications in Patients With Chronic Liver Diseases: A Systematic Review and Meta-analysis". Clinical Gastroenterology and Hepatology. 15 (10): 1521–1530.e8. doi:10.1016/j.cgh.2017.04.039. PMC 5605397. PMID 28479502.
- ^ "TOXNET". toxnet.nlm.nih.gov. U.S. National Library of Medicine. Archived from the original on 12 June 2018. Retrieved 29 May 2018.
- ^ Hermann M, Bogsrud MP, Molden E, Asberg A, Mohebi BU, Ose L, Retterstøl K (June 2006). "Exposure of atorvastatin is unchanged but lactone and acid metabolites are increased several-fold in patients with atorvastatin-induced myopathy" (PDF). Clinical Pharmacology and Therapeutics. 79 (6): 532–9. doi:10.1016/j.clpt.2006.02.014. PMID 16765141. S2CID 12838555. Archived (PDF) from the original on 26 February 2023. Retrieved 28 December 2020.
- ^ أ ب ت ث ج Williams D, Feely J (2002). "Pharmacokinetic-pharmacodynamic drug interactions with HMG-CoA reductase inhibitors". Clinical Pharmacokinetics. 41 (5): 343–70. doi:10.2165/00003088-200241050-00003. PMID 12036392. S2CID 8759303.
- ^ Thakker D, Nair S, Pagada A, Jamdade V, Malik A (October 2016). "Statin use and the risk of developing diabetes: a network meta-analysis". Pharmacoepidemiology and Drug Safety. Wiley. 25 (10): 1131–1149. doi:10.1002/pds.4020. PMID 27277934. S2CID 22626629.
- ^ Sattar N, Preiss D, Murray HM, Welsh P, Buckley BM, de Craen AJ, et al. (February 2010). "Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials". Lancet. Elsevier BV. 375 (9716): 735–742. doi:10.1016/s0140-6736(09)61965-6. PMID 20167359. S2CID 11544414.
- ^ Shah RV, Goldfine AB (October 2012). "Statins and risk of new-onset diabetes mellitus". Circulation. 126 (18): e282–e284. doi:10.1161/CIRCULATIONAHA.112.122135. PMID 23109518.
- ^ أ ب Baigent C, Blackwell L, Emberson J, Holland LE, Reith C, Bhala N, et al. (November 2010). "Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials". Lancet. 376 (9753): 1670–1681. doi:10.1016/S0140-6736(10)61350-5. PMC 2988224. PMID 21067804.
- ^ Macedo AF, Taylor FC, Casas JP, Adler A, Prieto-Merino D, Ebrahim S (March 2014). "Unintended effects of statins from observational studies in the general population: systematic review and meta-analysis". BMC Medicine. 12 (1): 51. doi:10.1186/1741-7015-12-51. PMC 3998050. PMID 24655568.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Agrawal D, Manchanda SC, Sawhney JP, Kandpal B, Jain R, Mehta A, et al. (December 2018). "To study the effect of high dose Atorvastatin 40mg versus 80mg in patients with dyslipidemia". Indian Heart Journal. 70 (Suppl 3): S8–S12. doi:10.1016/j.ihj.2018.01.034. PMC 6310693. PMID 30595326.
- ^ Mendes P, Robles PG, Mathur S (April 2014). "Statin-induced rhabdomyolysis: a comprehensive review of case reports". Physiotherapy Canada. Physiotherapie Canada. 66 (2): 124–132. doi:10.3138/ptc.2012-65. PMC 4006404. PMID 24799748.
- ^ Kashani A, Phillips CO, Foody JM, Wang Y, Mangalmurti S, Ko DT, Krumholz HM (December 2006). "Risks associated with statin therapy: a systematic overview of randomized clinical trials". Circulation. 114 (25): 2788–97. doi:10.1161/CIRCULATIONAHA.106.624890. PMID 17159064.
- ^ Newman CB, Palmer G, Silbershatz H, Szarek M (September 2003). "Safety of atorvastatin derived from analysis of 44 completed trials in 9,416 patients". American Journal of Cardiology. 92 (6): 670–6. doi:10.1016/S0002-9149(03)00820-8. PMID 12972104.
- ^ "Statin Side Effects: Weigh the Risks and Benefits". The Mayo Clinic. Archived from the original on 31 March 2014. Retrieved 19 April 2014.
- ^ Kostapanos MS, Liamis GL, Milionis HJ, Elisaf MS (September 2010). "Do statins beneficially or adversely affect glucose homeostasis?". Current Vascular Pharmacology. 8 (5): 612–31. doi:10.2174/157016110792006879. PMID 20507274. S2CID 220905587.
- ^ Ott BR, Daiello LA, Dahabreh IJ, Springate BA, Bixby K, Murali M, Trikalinos TA (March 2015). "Do statins impair cognition? A systematic review and meta-analysis of randomized controlled trials". Journal of General Internal Medicine. 30 (3): 348–58. doi:10.1007/s11606-014-3115-3. PMC 4351273. PMID 25575908.
- ^ Chu CS, Tseng PT, Stubbs B, Chen TY, Tang CH, Li DJ, et al. (April 2018). "Use of statins and the risk of dementia and mild cognitive impairment: A systematic review and meta-analysis". Scientific Reports. 8 (1): 5804. Bibcode:2018NatSR...8.5804C. doi:10.1038/s41598-018-24248-8. PMC 5895617. PMID 29643479.
- ^ Samaras K, Makkar SR, Crawford JD, Kochan NA, Slavin MJ, Wen W, et al. (November 2019). "Effects of Statins on Memory, Cognition, and Brain Volume in the Elderly". Journal of the American College of Cardiology. 74 (21): 2554–2568. doi:10.1016/j.jacc.2019.09.041. PMID 31753200.
- ^ "Atorvastatin: A medicine used to lower cholesterol". 3 January 2019. Archived from the original on 7 November 2021. Retrieved 7 November 2021.
- ^ Lai SW, Lin CL, Liao KF (February 2016). "Atorvastatin Use Associated With Acute Pancreatitis: A Case-Control Study in Taiwan". Medicine (in الإنجليزية الأمريكية). 95 (7): e2545. doi:10.1097/MD.0000000000002545. PMC 4998597. PMID 26886597.
- ^ أ ب Preiss D, Tikkanen MJ, Welsh P, Ford I, Lovato LC, Elam MB, et al. (August 2012). "Lipid-modifying therapies and risk of pancreatitis: a meta-analysis" (PDF). JAMA. 308 (8): 804–811. doi:10.1001/jama.2012.8439. PMID 22910758. Archived (PDF) from the original on 23 January 2022. Retrieved 23 January 2023.
- ^ Kostis JB, Dobrzynski JM (July 2014). "The effect of statins on erectile dysfunction: a meta-analysis of randomized trials". The Journal of Sexual Medicine. 11 (7): 1626–35. doi:10.1111/jsm.12521. PMID 24684744.
- ^ Cui Y, Zong H, Yan H, Zhang Y (June 2014). "The effect of statins on erectile dysfunction: a systematic review and meta-analysis". The Journal of Sexual Medicine. 11 (6): 1367–75. doi:10.1111/jsm.12497. PMID 24628781.
- ^ Graham DJ, Staffa JA, Shatin D, Andrade SE, Schech SD, La Grenade L, et al. (December 2004). "Incidence of hospitalized rhabdomyolysis in patients treated with lipid-lowering drugs". JAMA. 292 (21): 2585–90. doi:10.1001/jama.292.21.2585. PMID 15572716.
- ^ Iliadis EA, Rosenson RS (January 1999). "Long-term safety of pravastatin-gemfibrozil therapy in mixed hyperlipidemia". Clinical Cardiology. 22 (1): 25–8. doi:10.1002/clc.4960220110. PMC 6655916. PMID 9929751.
- ^ Shek A, Ferrill MJ (July 2001). "Statin-fibrate combination therapy". The Annals of Pharmacotherapy. 35 (7–8): 908–17. doi:10.1345/aph.10315. PMID 11485144. S2CID 23785176.
- ^ "Independent, reliable, relevant and respected". Therapeutic Guidelines (in الإنجليزية الأسترالية). Archived from the original on 8 May 2021. Retrieved 9 May 2021.
- ^ Mazzu AL, Lasseter KC, Shamblen EC, Agarwal V, Lettieri J, Sundaresen P (October 2000). "Itraconazole alters the pharmacokinetics of atorvastatin to a greater extent than either cerivastatin or pravastatin". Clinical Pharmacology and Therapeutics. 68 (4): 391–400. doi:10.1067/mcp.2000.110537. PMID 11061579. S2CID 26375921.
- ^ Neuvonen PJ, Niemi M, Backman JT (December 2006). "Drug interactions with lipid-lowering drugs: mechanisms and clinical relevance". Clinical Pharmacology and Therapeutics. 80 (6): 565–81. doi:10.1016/j.clpt.2006.09.003. PMID 17178259. S2CID 35917120.
- ^ Backman JT, Luurila H, Neuvonen M, Neuvonen PJ (August 2005). "Rifampin markedly decreases and gemfibrozil increases the plasma concentrations of atorvastatin and its metabolites". Clinical Pharmacology and Therapeutics. 78 (2): 154–67. doi:10.1016/j.clpt.2005.04.007. PMID 16084850. S2CID 8715786.
- ^ McKenney JM (May 2005). "Efficacy and safety of rosuvastatin in treatment of dyslipidemia". American Journal of Health-System Pharmacy. 62 (10): 1033–47. doi:10.1093/ajhp/62.10.1033. PMID 15901588.
- ^ أ ب Wiggins BS, Saseen JJ, Page RL, Reed BN, Sneed K, Kostis JB, et al. (November 2016). "Recommendations for Management of Clinically Significant Drug-Drug Interactions With Statins and Select Agents Used in Patients With Cardiovascular Disease: A Scientific Statement From the American Heart Association". Circulation. 134 (21): e468–e495. doi:10.1161/CIR.0000000000000456. PMID 27754879. S2CID 19169932.
- ^ Schwartz JB (February 2009). "Effects of vitamin D supplementation in atorvastatin-treated patients: a new drug interaction with an unexpected consequence". Clinical Pharmacology and Therapeutics. 85 (2): 198–203. doi:10.1038/clpt.2008.165. PMID 18754003. S2CID 23604512.
- ^ Kane GC, Lipsky JJ (September 2000). "Drug-grapefruit juice interactions". Mayo Clinic Proceedings. 75 (9): 933–42. doi:10.4065/75.9.933. PMID 10994829.
- ^ أ ب Ando H, Tsuruoka S, Yanagihara H, Sugimoto K, Miyata M, Yamazoe Y, et al. (November 2005). "Effects of grapefruit juice on the pharmacokinetics of pitavastatin and atorvastatin". British Journal of Clinical Pharmacology. 60 (5): 494–7. doi:10.1111/j.1365-2125.2005.02462.x. PMC 1884940. PMID 16236039.
- ^ أ ب Reddy P, Ellington D, Zhu Y, Zdrojewski I, Parent SJ, Harmatz JS, et al. (September 2011). "Serum concentrations and clinical effects of atorvastatin in patients taking grapefruit juice daily". British Journal of Clinical Pharmacology. 72 (3): 434–41. doi:10.1111/j.1365-2125.2011.03996.x. PMC 3175512. PMID 21501216.
- ^ أ ب Lilja JJ, Kivistö KT, Neuvonen PJ (August 1999). "Grapefruit juice increases serum concentrations of atorvastatin and has no effect on pravastatin". Clinical Pharmacology and Therapeutics. 66 (2): 118–27. doi:10.1053/cp.1999.v66.100453001. PMID 10460065. S2CID 8103490.
- ^ McLachlan A, Ramzan I (1 April 2006). "Meals and medicines". Australian Prescriber. 29 (2): 40–42. doi:10.18773/austprescr.2006.026. Archived from the original on 27 August 2021. Retrieved 10 May 2020.
- ^ أ ب Liberale L, Carbone F, Montecucco F, Sahebkar A (May 2020). "Statins reduce vascular inflammation in atherogenesis: A review of underlying molecular mechanisms". The International Journal of Biochemistry & Cell Biology. 122: 105735. doi:10.1016/j.biocel.2020.105735. PMID 32126319. S2CID 212408322.
- ^ أ ب Rosa GM, Carbone F, Parodi A, Massimelli EA, Brunelli C, Mach F, et al. (May 2014). "Update on the efficacy of statin treatment in acute coronary syndromes". European Journal of Clinical Investigation. 44 (5): 501–515. doi:10.1111/eci.12255. PMID 24601937. S2CID 28738671.
- ^ Furie KL (July 2012). "High-dose statins should only be used in atherosclerotic strokes". Stroke. 43 (7): 1994–1995. doi:10.1161/STROKEAHA.111.633339. PMID 22581818.
- ^ Amarenco P, Bogousslavsky J, Callahan A, Goldstein LB, Hennerici M, Rudolph AE, et al. (August 2006). "High-dose atorvastatin after stroke or transient ischemic attack". The New England Journal of Medicine. 355 (6): 549–559. doi:10.1056/NEJMoa061894. PMID 16899775.
- ^ Gaspardone A, Arca M (1 November 2007). "Atorvastatin: its clinical role in cerebrovascular prevention". Drugs. 67 (1): 55–62. doi:10.2165/00003495-200767001-00006. PMID 17910521.
- ^ Adams SP, Tsang M, Wright JM (March 2015). "Atorvastatin for lowering lipids". Cochrane Database of Systematic Reviews. 2015 (3): CD008226. doi:10.1002/14651858.cd008226.pub3. PMC 6464917. PMID 25760954.
- ^ Canestaro WJ, Austin MA, Thummel KE (November 2014). "Genetic factors affecting statin concentrations and subsequent myopathy: a HuGENet systematic review". Genet Med. 16 (11): 810–9. doi:10.1038/gim.2014.41. PMC 4676271. PMID 24810685.
- ^ أ ب ت ث ج ح خ Deshmukh HA, Colhoun HM, Johnson T, McKeigue PM, Betteridge DJ, Durrington PN, et al. (May 2012). "Genome-wide association study of genetic determinants of LDL-c response to atorvastatin therapy: importance of Lp(a)". Journal of Lipid Research. 53 (5): 1000–11. doi:10.1194/jlr.P021113. PMC 3329377. PMID 22368281.
- ^ أ ب ت ث Thompson JF, Man M, Johnson KJ, Wood LS, Lira ME, Lloyd DB, et al. (2005). "An association study of 43 SNPs in 16 candidate genes with atorvastatin response". Pharmacogenomics Journal. 5 (6): 352–8. doi:10.1038/sj.tpj.6500328. PMID 16103896.
- ^ أ ب ت ث ج Roth BD (2002). The discovery and development of atorvastatin, a potent novel hypolipidemic agent. Progress in Medicinal Chemistry. Vol. 40. pp. 1–22. doi:10.1016/S0079-6468(08)70080-8. ISBN 978-0-444-51054-9. PMID 12516521.
- ^ Roth BD, Blankley CJ, Chucholowski AW, Ferguson E, Hoefle ML, Ortwine DF, Newton RS, Sekerke CS, Sliskovic DR, Wilson M (1991). "Inhibitors of Cholesterol Biosynthesis. 3. Tetrahydro-4-hydroxy-6-[2-(1H-pyrrol-1-yl)ethyl]-2H-pyran 2-one Inhibitors of HMG-CoA Reductase. 2. Effects of Introducing Substituents at Positions Three and Four of the Pyrrole Nucleus". J. Med. Chem. 34 (1): 357–366. doi:10.1021/jm00105a056. PMID 1992137.
- ^ Li JJ, Johnson DS, Sliskovic DR, Roth BD (2004). "Chapter 9. Atorvastatin Calcium (Lipitor)". Contemporary Drug Synthesis. John Wiley & Sons, Inc. pp. 113–125. ISBN 978-0-471-21480-9.
- ^ "Fig. 1. Chemical structure of Atorvastatin Calcium". Researchgate.net. Archived from the original on 21 August 2022. Retrieved 25 May 2022.
- ^ أ ب ت Simons J (20 January 2003). "The $10 Billion Pill Hold the fries, please. Lipitor, the cholesterol-lowering medication, has become the bestselling pharmaceutical in history. Here's how Pfizer did it". Fortune.
- ^ أ ب ت ث Andrew J (28 November 2009). "The fall of the world's best-selling drug". Financial Times. Archived from the original on 10 December 2022. Retrieved 24 November 2015.
- ^ أ ب {{{1}}} patent {{{2}}}
- ^ أ ب Hoefle ML (2000). "The Early History of Parke-Davis and Company" (PDF). Bull. Hist. Chem. 25 (1): 28–34. Archived (PDF) from the original on 20 September 2018. Retrieved 12 March 2020.
- ^ أ ب Petersen M (8 February 2000). "Pfizer Gets Its Deal to Buy Warner-Lambert for $90.2 Billion". The New York Times. Archived from the original on 15 December 2018. Retrieved 18 February 2017.
- ^ Winslow R (24 January 2000). "The Birth of a Blockbuster: Lipitor's Route out of the Lab". The Wall Street Journal. Archived from the original on 7 April 2019. Retrieved 26 October 2011.
- ^ "Approval Letter" (PDF). U.S. Food and Drug Administration (FDA). Archived (PDF) from the original on 24 September 2020. Retrieved 21 June 2019.
- ^ أ ب "Lipitor becomes world's top-selling drug". Crain's New York Business via Associated Press. 28 December 2011. Archived from the original on 29 December 2011. Retrieved 24 November 2011.
- ^ "The Vindication of Roger Newton". Ann Arbor Observer. April 2020. Archived from the original on 17 September 2021. Retrieved 19 August 2022.
- ^ "Lipitor loses patent, goes generic". CNN. 30 November 2011. Archived from the original on 18 January 2017. Retrieved 18 November 2012.
- ^ "PPACA no cost-share preventive medications" (PDF). Cigna. Archived (PDF) from the original on 2 December 2020. Retrieved 30 March 2020.
- ^ "Statin Use for the Primary Prevention of Cardiovascular Disease in Adults: Recommendation Statement". American Family Physician. 95 (2). 15 January 2017. Archived from the original on 3 August 2020. Retrieved 31 March 2020.
- ^ "Recommendation: Statin Use for the Primary Prevention of Cardiovascular Disease in Adults: Preventive Medication". United States Preventive Services Taskforce. 15 November 2016. Archived from the original on 9 May 2022. Retrieved 7 May 2022.
- ^ "SignatureValue Zero Cost Share Preventive Medications PDL" (PDF). Uhc.com. September 2021. Archived (PDF) from the original on 5 February 2022. Retrieved 25 May 2022.
- ^ "Affordable Care Act Implementation FAQs - Set 12". CMS. 22 April 2013. Archived from the original on 5 May 2022. Retrieved 7 May 2022.
- ^ Medical Product Reviews. "Atorvastatin Calcium (Lipitor Tablets) – Uses, Dosage and Side Effects". Archived from the original on 6 October 2013. Retrieved 3 May 2012.
- ^ News Medical (March 2010). "Lipitor – What is Lipitor?". Archived from the original on 8 March 2012. Retrieved 3 May 2012.
- ^ "Pfizer's 180-Day War for Lipitor". PM360. Archived from the original on 12 April 2020. Retrieved 12 April 2020.
- ^ "Price to UK for 28 tablets from £3.25 (10mg) to £10.00 (80mg)". National Health Service. June 2012. Archived from the original on 20 September 2012. Retrieved 31 July 2012.
- ^ "Atorvastatin international". Drugs.com. 4 May 2020. Archived from the original on 3 August 2020. Retrieved 10 May 2020.
- ^ "Lipitor referral". European Medicines Agency (EMA). 17 September 2018. Archived from the original on 20 October 2020. Retrieved 10 May 2020.
- ^ Rapley L (31 May 2012). "Atorvastatin sole funding announced". PharmacyToday.co.nz. Archived from the original on 17 July 2014. Retrieved 16 July 2014.
- ^ أ ب "FDA Statement on Ranbaxy Atorvastatin Recall". U.S. Food and Drug Administration (FDA). 30 December 2012. Archived from the original on 19 April 2014. Retrieved 19 April 2014.
- ^ Loftus P, Weaver C (23 November 2012). "Ranbaxy Recalls Generic Lipitor Doses". The Wall Street Journal. Archived from the original on 17 May 2021. Retrieved 6 March 2021.
- ^ Johnson LA (24 November 2012). "Ranbaxy recalls generic Lipitor doses". The Boston Globe. Associated Press. Archived from the original on 29 December 2017. Retrieved 29 December 2017.
- ^ Loftus P (7 March 2014). "Ranbaxy Recalls More Than 64,000 Bottles of Generic Lipitor in U.S.". The Wall Street Journal. Archived from the original on 21 June 2019. Retrieved 21 June 2019.
- ^ Siddiqui Z, Sikka K (8 March 2014). "Indian drugmaker Ranbaxy recalls more than 64,000 bottles of its generic version of Lipitor". The Washington Post. Archived from the original on 29 December 2017. Retrieved 29 December 2017.
قراءات إضافية
- Maggon K (June 2005). "Best-selling human medicines 2002–2004". Drug Discovery Today. 10 (11): 739–42. doi:10.1016/S1359-6446(05)03468-9. PMID 15922927.
- Simons J (20 January 2003). "The $10 Billion Pill Hold the fries, please. Lipitor, the cholesterol-lowering medication, has become the bestselling pharmaceutical in history. Here's how Pfizer did it". Fortune.
- Winslow R (24 January 2000). "The Birth of a Blockbuster: Lipitor's Route out of the Lab". The Wall Street Journal. Archived from the original on 7 April 2019. Retrieved 26 October 2011.
وصلات خارجية
- "Atorvastatin". Drug Information Portal. U.S. National Library of Medicine.
- CS1 maint: unflagged free DOI
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- CS1 الإنجليزية الأسترالية-language sources (en-au)
- Short description is different from Wikidata
- Template:drugs.com link with non-standard subpage
- Drugs with non-standard legal status
- Articles with changed DrugBank identifier
- ECHA InfoCard ID from Wikidata
- Drug has EMA link
- Drugboxes which contain changes to watched fields
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- جميع المقالات تفتقد المصادر الموثوقة
- جميع المقالات تفتقد المصادر الموثوقة from May 2022
- جميع المقالات تفتقد المصادر الموثوقة from May 2021
- أنيليدات
- ديولات
- فلوروأرينات
- مركبات الأيزوپروپيل
- منتجات فايزر
- پيرولات
- ستاتينات