شيخوخة
| جزء من سلسلة عن |
| تطور ونمو الجسم البشري |
|---|
 |
| المراحل |
| المحطات الحيوية |
| التطور وعلم النفس |

الشيخوخة Ageing أو aging هي عملية الهِرم والتقدم بالعمر التي تصيب الكائنات الحية نتيجة تناميها. [1] التعريفات المؤخرة لعملية الشيخوخة تعتبرها عبارة عن خلل و تلف في عمليات النظام مع مرور الوقت و الزمن ، هذا التعريف يسمح بظهور و وجود انظمة لا تهرم (لاتشيخ) non-ageing systems ، نتيجة تداخلات مضادة للشيخوخة (عندما يمكن إصلاح الخلل المتراكم) . الشيخوخة أصبحت تدرس حاليا كعلم يتناول النواخي الثقافية والاقتصادية و دراسات الوعي و التغيرات الاجتماعية و الديمغرافية أما النواحي الفيزيولوجيا فتوصف بعملية هرم
وتحدث الشيخوخة في جسم معظم الناس مع تقدم السن ـ والغالب بدءاً من الخامسة والستين وفوق ذلك ـ تبدلات تتراجع فيها أعضاء الجسم تدريجياً وتشمل مظهر الإنسان الخارجي وبنية معظم أعضائه ووظائفها، وحالته النفسية والعقلية، يسمى مجموع هذه التبدلات التشيخ senescence الذي ينتهي بحالة الشيخوخة senility.
وليس من الضروري أن يرافق التشيخ كل من تتقدم به السن، لأن تقدم السن شيء والتشيخ شيء آخر.
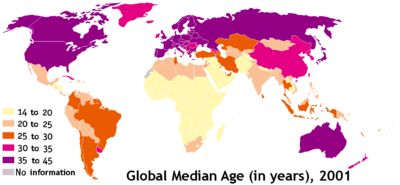
وقد ارتفع وسطي عمر الإنسان وازداد بالتالي عدد الشيوخ وحوادث التشيخ، نتيجة القضاء على كثير من الأوبئة التي كانت تفتك بالبشر كالطاعون والملاريا، ونتيجة تحسن طرائق كشف بعض الأمراض المزمنة وعلاجها كالسل والإفرنجي، كما ازدادت بسبب انتشار الوقاية من كثير من العلل باللقاحات والمصول كشلل الأطفال والشاهوق، ولتقدم طرائق العلاج الطبي والجراحي لكثير من الإصابات المرضية كالأخماج وأمراض القلب، وزيادة الوعي الصحي مع تقدم العلم. وقد قدرت منظمة الصحة العالمية عدد الذين تفوق أعمارهم الستين في عام 2000 بنحو 600 مليون إنسان. ويعتقد أن هذا العدد سيبلغ 1.2 بليون في عام 2025 و2 بليون في عام 2050. [2]
وتتميز الشيخوخة بقابلية متناقصة للاستجابة للضغوطات ، اضطراب في الاتزان Homeostasis الحيوي و زيادة خطورة التعرض لأمراض . نتيجة ذلك يكون الموت هو النتيجة الحتمية للشيخوخة .
الهرم
في علم الأحياء والفيزيولوجيا : تعتبر الهرم (بفتح الهاء و الراء) senescence عبارة عن اجتماع مجموعة عمليات خلل وظيفي (تلف) تلي فترة من التنامي للعضوية . يهتم علم رعاية المسنين بشكل خاص بعملية الهرم هذه و يدخل في ما يدعى : إطالة العمر life extension .
الهرم الخلوي Cellular senescence ظاهرة تحدث فيها فقدان الخلايا لقابلية الانقسام و بالتالي التجدد . كنتيجة لتضرر الدنا في الخلايا (بشكل أساسي الوصول لقصر شديد للتوليمير ) يحدث إما هرم أو تدمير ذاتي (استموات) في حال عدم القدرة على تصحيح الخطأ . يستخدم هنا بكثرة مصطلح شيخوخة aging أو تعمير كمصطلح مرافق و مشابه لمصطلح هرم . مصطلحي هرم و شيخوخة يستخدمان حاليا بشكل متبادل في معظم المقالات .
عوامل حدوث الشيخوخة
وساعد على زيادة حوادث التشيخ كذلك تغير نمط الحياة ولاسيما في بلادنا، فزوال الدور الكبيرة الواسعة التي كان يعيش فيها الإنسان مع أبنائه وأحفاده، وتضم عشرات الأشخاص أحياناً، كان فيها الجد والجدة محاطين بالتكريم والعناية العضوية والنفسية ويمارسان بعض الأعمال البسيطة السهلة، أدى إلى انفصال الأبناء عن آبائهم، وأصبح كبار السن يعيشون منعزلين، حتى إنه يشاهد أحياناً فرد واحد فقط يعيش في منزله. ويعد هذا النمط الجديد من الحياة من أهم أسباب حدوث التشيخ ولاسيما مظاهره النفسية.
تعرف الشيخوخة بمنظر الإنسان الخارجي الذي تبدو على وجهه تجعدات الجلد الواسعة أو رقته، كما تبدو التصبغات مختلفة الحجوم على وجهه ورأسه.
التطور الطبيعي
يتفق عدد من الباحثين، بمن فيهم روز، على أن فهم العلة في نشوء الشيخوخة شرط ينبغي أن يسبق تحققه كشف الأسس الفيزيولوجية للشيخوخة. ويقول هؤلاء الباحثون: إن نظرية التطور تقدم إطارا ضروريا لمعرفة كيف يعمل الجسم وكيف يتوقف عن العمل ـ ولتعرّف الجينات المعنية بالتحكم في مدة الحياة (العمر) life span. ويقول روز عن البحوث في الشيخوخة بوجه عام: «إن الكيمياء الحيوية لها دور قيم فيما نقوم به من عمل، ولكنها لا تقدم أساسا فكريا.»
وتقول النظرية التطورية الأساسية بأن أكثر الأفراد لياقة ـ أي الذين يؤهلهم خليطهم الخاص من الأليلات لأن يكونوا أصلح للبقاء والإنجاب في بيئتهم ـ هم القادرون على إحداث أعظم الأثر في المعين الجيني(3) gene pool للأجيال القادمة. وسوف يتم اصطفاء(4) selection التغيرات الوراثية التي تقوي اللياقة (الصلاحية) fitness (كتلك التي تعمل على تمكين الفرد من أن يكون أسرع فرارا من الخطر) ومن ثم تُستبقى لتصبح شائعة بعد بضعة أجيال. وتُنتخب هذه السمات الوراثية لأن من المحتمل أكثر بقاء حامليها ووفرة ذراريهم، وبذا يسهمون بأعداد كبيرة من أبنائهم للجيل التالي. وبالمثل، سوف يستبعد الاصطفاء الطبيعي الطفرات التي تؤدي إلى الموت الحتمي قبل أن يتم النضج الجنسي. وهكذا لن يخلف الأفراد المصابون بتلك الطفرات المميتة ذرية تنقلها للأجيال التالية.
ومنذ أواخر العقد الأول من القرن التاسع عشر، أخذ الكثير من العلماء يؤيدون فكرة أن الشيخوخة تولدت من أن التخلص من الكبار يزيد لياقة الأفراد الصغار، ربما عن طريق تقليل استنزاف الموارد المتاحة. ويقترح هذا السيناريو أن الشيخوخة مبرمجة (كامنة) في جينات هدفها الأوحد إتلاف الكائن الحي. ولكن هذا الرأي يفقد الآن مؤيديه، وذلك جزئيا لأن معظم الحيوانات لا تعيش في البرية فترة كافية لكي تعطى الفرصة لتصبح معمَّرة. وفي أثناء معظم تاريخنا البشري، نحن أيضا متنا صغارا. وفي المتوسط، يتوقع الشخص الذي يولد اليوم في مجتمع صناعي أن يعيش نحو 75 عاما، في حين كانت الأعمار خلال معظم تاريخنا أقرب إلى الثلاثين أو الأربعين عاما.
وتقول الفرضيات التطورية البديلة بأن الجينات تتحكم في الشيخوخة ولكن الأليلات غير المرغوب فيها لم تنتخب لهذا الغرض على وجه التحديد. فهذه النظريات تؤكد أن جينات الشيخوخة ـ التي تسمى أحيانا جيرونتوجينات gerontogenes ـ أصبحت مستكنة في الكروموسومات (الصبغيات) البشرية لأن الاصطفاء الطبيعي لم يستطع منع انتشارها. فالأليلات المؤذية على وجه التحديد تدوم في نوع من الكائنات إذا لم تكن آثارها الضارة لتظهر إلا بعد بدء التناسل بوقت طويل.
آرومات ليفية (اللون الأزرق) أو خلايا نسيج ضام سوية، مستخلصة من نسيج بشري (في اليسار)، تصبح أكبر حجما كلما نمت لمدة أطول في طبق الزراعة (الاستنبات) (في اليمين). وفي الوقت نفسه، يبطؤ معدل تكاثرها حتى تتوقف الخلايا عن الانقسام في النهاية. وقد استطاع الباحثون في مختبرات عديدة تعرف كثير من الجينات التي يبدو أنها تنظم فقد القدرة على التضاعف. بيد أن ما تفصح عنه هذه النتائج حول كيف يشيخ الجسم ككل فأمر لم يتضح بعد.
بل الأسوأ من ذلك، كما اقترح في الخمسينات<سي.جى وليامز>(من جامعة ولاية نيويورك في ستوني بروك)، أن الأليلات التي تكون مدمرة في الفترة المتأخرة من الحياة سوف يتم تبيُّنها إذا استطاعت، بصورة ما، أن تُظهِر تحسنا في اللياقة مهما كان قدره في مستهل الحياة ـ وهذه ازدواجية تعرف باسم الپليوتروبية(5)(التعددية المظهرية)المتعارضة antagonistic pleiotropy. والجينات التي تحدد التعليمات الخاصة بتخليق هرمونات التناسل يمكن أن تكون من بين تلك المجموعة المخاتلة. ويفترض إس.أوستاد (في جامعة هارڤارد)أن تزايد احتمال الإصابة بسرطان الثدي مع تقدم العمر عند النساء، قد يكون مثالا لهذا: فالتعرض طويل المدى للإستروجين الذي تحتاج إليه النساء للخصوبة يمكن أن يجعل نسيج الثدي عرضة للأورام الخبيثة.
وذلك يشبه ما وجده إى.سى.فنش (في جامعة جنوب كاليفورنيا)من أن مجموعة متنوعة من الهرمونات العادية وغيرها من الجزيئات المنظِّمة قد تضر بالخلايا والأنسجة التي تؤثر فيها. وينظم كل من المهاد التحتاني (ما تحت المهاد)hypothalamus والغدة النخامية pituitary gland وظيفة المبيض، ولكنهما يسهمان أيضا في شيخوخة المبيض في القوارض على الأقل. وفي الوقت نفسه، يبدو أن المبيض ذاته، الذي يبعث بإشارات إلى المهاد التحتاني والغدة النخامية، يُسرِّع من شيخوخة هذين العضوين. ويرى فنش أكثر من ذلك أن الخصائص الپليوتروبية هي دليل على أن الشيخوخة تنشأ، إلى حد ما، عن نشاط الجهاز العصبي وجهاز الغدد الصم وعن التآثرات interactions الحادثة بينهما.
أما الجينات التي تعزز اللياقة المبكرة فليس بالضرورة أن تقوم بتدمير مباشر، في مرحلة متأخرة من الحياة، لكي تسبب التدهور النهائي. وقد اقترح كل من إل.بى.تى.كيركوود (من مجلس البحوث الطبي في لندن)و جى.آر. كتلر (من المعهد القومي للشيخوخة)أن طول العمر يحدث لدى جماعة من السكان إذا ما كانت الأجهزة اللازمة لحفظ الجسم لديهم والتي تخضع للتحكم الوراثي، على درجة كافية من الجودة تضمن للكائن أن يحيا ليُخلِّد النوع وإن كانت عاجزة عن الحفاظ على الجسم إلى الأبد.
الجسد المُستهلَك
يعتقد كيركوود أن معظم الحيوانات لم تُنَمِّ أنظمة حفظ تضمن عدم الفناء، لأن هذا يبدد الطاقة التي يمكن أن توجَّه بشكل أفضل للتكاثر. وحيث إن المخاطر البيئية يمكن أن تقتل الأفراد خلال فترة معقولة يمكن التنبؤ بها، فإن النوع يجب أن يستثمر طاقاته في أنظمة حماية تضمن له حيوية الشباب لهذه المدة المتوقعة وليس أكثر من ذلك. أما باقي مخزون طاقة الكائن فيمكن أن يستغل في زيادة خصوبته.
وعلى نحو ما يحدث في الصناعة من استثمار القليل في إطالة عمر المنتجات التي لن تستخدم إلا لمدة محدودة، يسمي كيركوود نموذجه نظرية الجسد (السُّوما)المُستغنى عنه disposable soma theory. وفي هذه الحالة فإن الخلايا الجسدية somatic cells ـ وهي خلايا الجسم غير التناسلية ـ هي التي يمكن في النهاية أن تُستهلك. وعلى نقيض ذلك، فإن نسبة من الخلايا الجرثومية germ cells لا بد أن تحتفظ بالقدرة على إصلاح نفسها على أفضل وجه وإلا فني النوع.
مراحل العمر
| المصطلح | العمر |
|---|---|
| Denarian | 10 إلى 19 |
| Vicenarian | 20 إلى 29 |
| Tricenarian | 30 إلى 39 |
| Quadragenarian | 40 إلى 49 |
| Quinquagenarian | 50 إلى 59 |
| Sexagenarian | 60 إلى 69 |
| Septuagenarian | 70 إلى 79 |
| Octogenarian | 80 إلى 89 |
| Nonagenarian | 90 إلى 99 |
| Centenarian | 100 to 109 |
| Supercentenarian | 110 وأكبر |
أعراض الشيخوخة
يحدث التشيخ نتيجة تأثر خلايا الجسم بتقدم العمر، فيبطؤ تجدد هيولى الخلايا بشدة، وينقص ماؤها، مما يغير العلاقة بين الماء داخل الخلية وخارجها، وقد ثبت أن الخلايا والوسط خارجها تُراكم في الأشخاص المسنين بعض المواد الضارة كالكلسيوم والأصبغة والبروتينات غير الفعالة والشحوم، في حين تتناقص بعض الأنزيمات كالهكسوكيناز hexokinase والألدولاز aldolase، والأجسام الغنية بالقدرة كحمض الأدينوزين الثلاثي الفسفور adenosine triphosphoric acid (ATP) وهو مادة تدخل في الاستقلاب الخلوي والانقباض العضلي وتركيب الهرمونات القشرية الكظرية وتؤلف المنبع الأساسي لقدرة العضوية.
وتختلف هذه التبدلات باختلاف أنسجة الجسم، وأكثرها خطورة في الإنسان تبدلات الخلايا العصبية، وينجم عن كل هذا هبوط قدرة العضوية على التكيف لدعم ثبات الوسط الداخلي والدفاع ضد الشدات (أو الكرب) stress الخارجية كتبدلات الحرارة وغيرها.
وللوراثة علاقة بزمن ظهور التشيخ، كما لوحظ أن طرائق إنقاص الاستقلاب تؤخر ظهوره كإنقاص الحرارة والحمية، فالحمية المتوازنة كيفياً والناقصة كمياً تطيل العمر في الحيوانات تجريبياً، وقد لوحظ ذلك أيضاً في الإنسان، فالوفيات تزيد بنسبة 20% من مجموع السكان في الأشخاص الذين يزيد وزنهم 10% عن الوزن المثالي.
الجفاف
ولعل إصابة الشيوخ بالتجفاف dehydration من أكثر الإصابات مصادفة، إذ تظهر حالة تجفاف خطرة بعد انخفاض كمية الماء بمدة قصيرة، وإن الوقاية من حدوث مثل هذه الحالة، بالقدر الذي تسمح به حالة المريض، ضرورية؛ وكشفها ومعالجتها بسرعة واجب أيضاً. لأن إنذارها خطر في مثل هذا العمر؛ فقد تسبب عند المسن طوارئ وعائية شريانية وخثارات thrombosis وريدية وأخماجاً تنفسية وخشكريشات eschar.
يطلق على اللوحة السريرية للتجفاف عادة اسم التقلص المفرط التوتر hypertonic contraction، إذ يؤدي النقصان النسبي أو المطلق للوارد من الماء بالنسبة إلى الكمية المفقودة منه من الجسم إلى نقصه في الوسط خارج الخلايا، وظهور فرط توتر hypertonie داخلها، سواء كانت هذه الكمية طبيعية أو زائدة، لأن الكتلة التناضحية لا تنخفض، وتؤدي إعادة توازن التوتر من طرفي الغشاء الخلوي إلى نقص التوتر داخل الخلايا، وليست العلامات السريرية المألوفة لهذا الاضطراب واضحة عند المتقدمين في السن.
ـ يؤلف انخفاض الضغط الشرياني، إذا لم يرافقه توسع في الأوعية، علامة واضحة لنقص الوسط خارج الخلايا، ولابد من معرفة مقدار ضغط المريض قبل وقوع الحادث. فانخفاض ضغط المسن من 190 إلى 140 يعني إصابته بوهط collaps، كما أن إصابته بعدم ثبات الضغط تزيد المشكلة تعقيداً.
لا قيمة في هذا المضمار لتسرع ضربات القلب إذا كان الشيخ مصاباً بحمى، فالحرارة ترتفع في معظم حالات التجفاف، كما أن تقدير العلامات البيولوجية لتركيز الدم hemoconcentration عسير أيضاً، فحينما يرافق التجفاف فقر الدم تكون كمية الهيماتوكريت hematocrit سوية، وكذلك أرقام البروتينات الكلية حينما يشارك التجفاف عوز البروتينات. ويمكن الاعتماد على علاقة بيولوجية، هي ارتفاع مقدار البولة الدموية (اليوريمية) المقترن ببقاء كرياتنين الدم ضمن الحدود الطبيعية. وتشاهد مثل هذه الحالة، على أقل تقدير، حينما لا يكون التجفاف شديداً. ولابد من التذكرة هنا أن كرياتنين البلازما لا يزداد بازدياد العمر.
إن العلامة الأساسية لحدوث تقلص داخل الخلايا هي العطش، لكنها غالباً لا تظهر، ويرجع عدم ظهورها إلى إصابة المريض باضطراب في الوعي يمنعه من التعبير عنها، أو إصابته بسبات coma، أو أنه، على الرغم من وعيه، لا يبدي رغبة في شرب الماء، أو لا يشعر بحاجته إليه، وهذه الحالة الأخيرة كثيرة المصادفة. ولا يعتمد تقدير جفاف المخاطيات على منظر اللسان بل على التلمة اللثوية الخدية gingivojugal.
أما بالنسبة إلى اضطرابات الوعي المصحوبة بارتفاع درجة الحرارة، فيمكن أن يكون سببها غير التجفاف.
وأخيراً تكون العلامة الرئيسة، هي وجود فرط توتر في البلازما يمكن تقديرها بسهولة بارتفاع مقدار صوديوم الدم. ويمكن القول أنه إذا زاد مقدار صوديوم الدم على 145 مليمول في الليتر فهذا يعني نقصاناً في الماء؛ وليس من النادر أن يزيد في التجفاف صوديوم الدم على 160 مليمول، وهذا يدل على نقصان كبير في كمية ماء البدن.
ينجم التجفاف بلوحته السريرية عن نقص في كمية الماء المتناولة وطرح لمقادير طبيعية منه. وتشاهد هذه الحالة عند الشيوخ المسبوتين، والعجزة الذين لا يستطيعون الحصول على الماء وحدهم، وليس لهم من يعينهم، فيفقدون حس العطش، وفي المصابين بإقياء أو باضطراب في البلع الخ..
كما ينجم عن عدم ملاءمة الكميات الواردة لتعويض الكميات المفقودة المتزايدة؛ كإصابة المريض ببوال polyuria أو بتعرق غزير ناجم عن ارتفاع شديد في الحرارة، أو بلهث، أو بضياع السوائل عن طريق جهاز الهضم، ومع هذا فإن السبب الغالب هو نقص في كميات السوائل الواردة وزيادة في كمية فقدانها.
وتظهر في التجفاف لوحة سريرية خطرة بعد زمن يراوح بين عدة ساعات وثلاثة أيام. ويتطلب ظهور خلل الصوديوم زمناً أطول من ذلك بكثير، إلا إذا كان هناك ضياع للسوائل شديد جداً عن طريق جهاز الهضم، أو جهاز البول.
ويجدر القول إن إعطاء كميات زائدة من السوائل أفضل من إعطاء كميات ناقصة على أن يكون الإفراغ الكلوي جيداً، ووظيفة القلب مقبولة.
يعد التجفاف حالة إسعاف يجب البدء بمعالجتها قبل ظهور نتائج الفحوص البيولوجية، وتطرح المداواة عدة أمور في مقدمتها، تحديد الخسارة من السوائل، ويؤلف حجم الماء الكلي قرابة 60% من مجموع وزن الجسم، فتقدير كمية الماء الواجب إعطاؤها لتصحيح الاضطراب هو حاصل مجموع كمية الماء الناقصة مضافاً إليها الكمية اللازمة خلال 24 ساعة قادمة. ويقدر ما يحتاج إليه المسن منها في اليوم، إن لم يكن مصاباً بضياع شديد بالسوائل، بمقدار 1.5 إلى 2ليتر. أما إذا كان هناك فقدان كبير بالسوائل فيجب إضافة مقدار 0.3ل لكل درجة حرارة تزيد على 37 ْ، والخطأ الذي يرتكب عادة هو إعطاء المريض كمية الماء الناقصة دون الالتفات إلى حاجته منها خلال 24 ساعة قادمة. وطريق الفم هو الطريق الطبيعي والسهل لإعطاء السوائل الناقصة بتناول المريض الماء العادي، ويسمح هذا الطريق بأخذ الأطعمة ولاسيما البروتينية منها، ولا يتطلب إلا أن يكون المسن قادراً على الشرب بسهولة ومن يرعاه قريباً منه ونشيطاً.
ويبقى الطريق الوريدي أوثق الطرق في معظم الحالات، واللجوء إليه ضروري حينما يكون المريض مصاباً بالوهط. لذا يلجأ إلى محلول غلوكوزي متساوي التوتر (إسوي التوتر) isotonic إذا كانت الكميات المراد إعطاؤها قليلة، وكان المريض غير مصاب بالداء السكري. ومما تجدر الإشارة إليه هنا أن ارتفاع كمية سكر الدم إلى 1.5غ كثير المشاهدة في التجفاف ولا يدل على إصابة بالسكري.
قد تكون الصفة المميزة للتشيخ ضعف وظيفة الإنجاب ثم توقفها، ويحدث ذلك في المرأة بانقطاع الطمث نتيجة توقف المبيضين عن إفراز هرموناتهما الخاصة، أما في الرجل فتضعف الوظيفة الجنسية ببطء تدريجياً وفي سن أكثر تقدماً، وينجم الضعف كذلك عن نقص هرموني يشمل في الجنسين، عدا الهرمونات الجنسية، هرمونات أخرى كالأنسولين وهرمونات قشر الكظر.
تدني الوظائف الجنسية
تتدنى الوظيفة الجنسية عند الذكور بسبب الاعتلالات الوعائية والداء السكري أو الاعتلال البدئي في وظيفة الجسمين الكهفيين إضافة لتراجع في مقدار الهرمونات المذكرة في هذه السن، كما يتدنى أثر استعمال بعض الأدوية كخافضات الضغط الشرياني أو أدوية القرحة المعدية أو الأدوية النفسية.
كما يشكو معظم النساء من تدني الوظيفة الجنسية بسبب القصور الاستروجيني في هذه السن، وما ينتج عنه من ضمور في القناة التناسلية، ونقص في الرغبة الجنسية.
الأخماج البولية
ةالأخماج البولية كثيرة الحدوث عند المسنين وتؤلف 10% من مجموع الأخماج التي تصيب الإنسان بعد الستين من عمره، وتختلف اللوحات السريرية التي تسببها اختلافاً كبيراً فيما بينها؛ أما المشكلات الأساسية التي تطرحها فهي البحث عن الأسباب، والخطر الناجم عن تأثير الأدوية في عضوية أصبحت ضعيفة في قيامها بوظائفها، والوقاية من حدوث النكس.
تشاهد الأخماج البولية بصورة أساسية عند المرأة، ويزداد تواترها بازدياد سن المريضة، إذ تصيب 10% إلى 15% من النسوة اللواتي تجاوزن الخامسة والستين من عمرهن. ومما يساعد على الإصابة بها التركيب التشريحي للجهاز التناسلي للمرأة، فجراثيم الفرج vulva تلوث البول كما تلوث الإحليل urethra، ويظهر الخمج البولي عند الرجل في حوالي الخمسين من عمره مرافقاً لبدء اضطرابات الموثة prostate، ويصيب 1% من الأفراد بعد الستين من عمرهم.
ينشط الخمج البولي بوجود عائق يسد الطرق البولية، كالإصابة بحصيات بولية lithiasis، أو ورم غدي adenoma، أو ورم تناسلي سليم أو خبيث، أو ورم في الكلوة أو الطرق المفرغة، وتزيد الآفات الكلوية من خطورة الإصابة الخمجية ولاسيما إذا تطلبت إجراء استقصاءات. وغالباً ما يكون عدم الحركة سبباً في ظهور الخمج، ولاسيما إذا كان الشيخ يتناول كميات قليلة من السوائل.
يعد الداء السكري وكبت المناعة immunosuppression المرضي أو الدوائي مع تقدم السن عوامل تزيد من خطورة الأخماج.
تأتي الاشريكية القولونية Escherichia coli في مقدمة الجراثيم المسببة للخمج البولي عند الشيوخ وترى في 75% من الحالات، والمتقلبات proteus، وترى في 10% من الحالات ولاسيما المتقلبات الرائعة المحصية P.mirabilis lithogène منها. أما الكلبسيلا والزوائف pseudomonas فغالباً ما تظهر بعد استعمال دواء ما. أو وضع أجسام غريبة كالقثاطر لفترة طويلة، وتوجّه الإصابة بالجراثيم العقدية streptococcus الأنظار نحو آفة إحليلية urethra أو تناسلية.
يمكن أن تقتصر العلامات السريرية عند المتقدمين بالسن على احساس بحرقة في البول، أو ارتفاع حرارة مديدة ومنفردة، وقد تتظاهر الأعراض ببيلة دموية فحسب. ولا تسمح الأعراض عند ظهورها بتحديد موضع الآفة دوماً، فعند الشيوخ لا تتناسب شدة الأعراض مع خطورة الآفة.
لا يقرر العلاج إلا بعد دراسة هشاشة المريض المسن للتأثيرات العلاجية المنشأ وأخذها في الحسبان، وذلك لانخفاض القدرة الوظيفية لكليتيه لإمكان حدوث تأثيرات متداخلة مع أدوية أخرى.
لا تعطى الصادات إلا بشكل يناسب خطورة الخمج ووظيفة الكلوة والآفات المرافقة. ويجب الابتعاد قدر المستطاع عن المشاركات بين الصادات خشية تزايد السمية.
وإصابة الجهاز البولي التناسلي بنصيب وافر من الاعتلالات في سن الشيخوخة يمكن فهمها إذا قسمت إلى الزمر التالية:
التدني في الوظيفة الكلوية، أي الإصابة بدرجة متفاوتة من القصور الكلوي، وهذا ناتج عن: التدني المتدرج في وظيفة الكليتين الذي يزداد مع تقدم العمر، وهو أمر طبيعي يتبع قانون الاهتراء wear & tear وينصح، لتجنب ظهوره أو تطوره السريع، بـ:
ـ الإقلال من تناول البروتينات والإكثار من تناول السوائل في الغذاء.
ـ تجنب أخذ الأدوية جزافاً إلا بمعرفة الطبيب، إذ أن بعض الأدوية تؤثر تأثيراً سيئاً في الوظيفة الكلوية (مثل بعض أنواع الصادات).
ـ ضرورة معالجة بعض الأمراض الجهازية المؤثرة سلباً على الوظيفة الكلوية كالداء السكري وفرط الضغط الشرياني.
ـ ضرورة مراجعة الطبيب المتخصص في حال ظهور أعراض بولية مثل تعدد البيلات، وعسرة التبول التي قد تنجم عن إصابات الموثة الورمية أو آفة مثانية، كما أن ظهور البيلة الدموية هو عرض هام جداً يجب مراجعة الطبيب فور ملاحظته لأنه قد يدل على إصابة ورمية في المثانة. ومن المعلوم أن الآفات الورمية المثانية والموثية كثيرة الحدوث في هذه السن.
اضطرابات التبول
أما أكثر اضطرابات التبول مشاهدة في سن الشيخوخة فهي:
ـ عند الذكور: يشاهد السلس البولي، وهو نقص التحكم بالبول، وأسبابه عديدة: بولية أو عصبية، وتتطلب هذه الشكوى مراجعة الطبيب لتشخيص السبب والمعالجة، كما يشاهد أيضاً الأسر البولي وصعوبة التبول بسبب إصابات الموثة الورمية السليمة والخبيثة.
ـ عند النساء: كثيرات هنَّ اللواتي يشتكين في هذه السن من أعراض مثانية مزمنة وصعوبة في التبول، ترجع في الغالب للإصابة بالالتهابات البولية السفلية المزمنة التالية لضمور الإحليل وتضيقه، كما تصاب نسبة كبيرة من النسوة بضرب مزعج من السلس البولي، وتستدعي هذه الحالات مراجعة الطبيب المتخصص لأنها في معظمها قابلة للمعالجة والشفاء بإجراءات دوائية أو جراحية حسب الحالة.
فقر الدم
يجب أن يعد كل فقر دم حالة مرضية، على الرغم من أن تعدد أسباب هذا الداء (كسوء التغذية والأخماج وتأثير الأدوية) تتداخل عند المسنين، فتزيد من صعوبة سير التشخيص والمعالجة.
يسبب فقر الدم بعد سن الستين نسبة وفيات لا يمكن إهمالها. وعلى هذا، يجب أن يكون كشف فقر الدم موضع الاهتمام حتى ولو كان «فقر دم شيخياً بسيطاً»، إذ يجب وضع تشخيص صحيح، كلما أمكن ذلك، لإعطاء العلاج الملائم.
يرتكز تشخيص فقر الدم على مقدار الهيموغلوبين (الخضاب) (أقل من 13غ/100سم3 عند الرجل، وأقل من 12غ/100سم3 عند المرأة)، وعلى نتائج الهيماتوكريت (أقل من 42% عند الرجل)، مهما تكن الظروف التي تدعو إلى إجراء صيغة الدم hemogram هذه.
لا يشكل عدد الكريات الحمر محكاً كافياً للتحدث بشكل أكيد عن الإصابة بفقر الدم، فقد يبلغ عدد الكريات الحمر خمسة ملايين، ويكون هناك فقر دم أكيد إذا كانت هذه الكريات الحمر من النوع الصغير microcytaire. وهنالك سبب آخر للوقوع في الخطأ هو التخفيف الدموي hemodilution (أي زيادة المصورة) الذي يسبب انخفاضاً في مقدار الهيموغلوبين والهيماتوكريت وعدد الكريات الحمر، ويجب التفكير بفقر دم كاذب ناجم عن التخفيف الدموي عند كل مريض مستعد للإصابة بفرط حجم المصورة. وهذه الحالة كثيرة المشاهدة بين الأفراد المسنين.
تقدم معرفة آلية فقر الدم مفتاحاً للتشخيص في معظم الحالات. إن إجراء فحوص بسيطة وعملية يسمح بتصنيف فقر الدم ضمن إحدى الفئات الفيزيولوجية المرضية الثلاث الآتية: نقص في تركيب الهيموغلوبين، ونقص في توليد النقي لأرومة الحمر erythroblast، وفقدان كمية من الدم نتيجة لنزيف أو انحلال دموي شديد.
وهناك وسيلة ملائمة توجه التقصي الذي يهدف إلى معرفة أسباب المرض، وذلك بالبدء بتصنيف فقر دم المصاب، حسب حجم الكرية الوسطي، ضمن أحدى المجموعات الثلاث التالية:
ـ المجموعة الأولى: فقر دم كبير الكريات macrocytic، ويكون حجم الكرية الوسطي فيه أكبر من 100 مكرون مكعب.
ـ المجموعة الثانية: فقر دم صغير الكريات microcytic، ويكون حجم الكرية الوسطي فيه أقل من 80 مكرون مكعب.
ـ المجموعة الثالثة: فقر دم سوي الكريات، ويكون حجم الكرية الوسطي فيه بين 80 و100 مكرون مكعب.
وعوز الحديد هو أكثر الأسباب حدوثاً، ويدل هذا العوز في معظم الأحيان على نزف هضمي، رغم كثرة وجود اللاكلوريدية، ونقصان امتصاص جهاز الهضم للحديد.
أمراض الجهاز الهضمي
إن دراسة المري والمعدة والعفج duodenum، من الأمور التي لابد منها للبحث عن قرحة معدية عفجية، أو فتق في الحجاب الحاجز، أو سرطان معدة أو قولون. وقد يظهر أحياناً أن سبب النزف المعدي كامن في تناول حمض الصفصاف salicylic acid، أو مضادات الالتهاب لمدة طويلة. أما معرفة أسباب النزوف المتكررة والناجمة عن البواسير فهي أكثر سهولة.
وترمي المعالجة، إضافة إلى مداواة السبب، إلى تصحيح عوز الحديد، وذلك بإعطاء أملاحه. ولا فائدة من مشاركة الدواء مع الفيتامينات C، لأن عوز الحديد يترافق بعوز في هذا الفيتامين عند المسنين في معظم الأحيان. ويعود مقدار الهيموغلوبين إلى حالته الطبيعية خلال ثمانية أسابيع تقريباً.
ويتأثر الجهاز الحركي بوهن العضلات الناجم عن نقص التغذية، وبهشاشة العظام الناجمة عن نقص الكلس، وتعرضها بذلك للكسور لأقل رض، وأكثر ما يحدث ذلك في عنق الفخذ وفي الفقرات، التي ينجم عن نقص الكلس فيها، عدا ذلك، تكدسها الذي يؤدي إلى قصر العمود الفقري وانحنائه وقصر القامة، وتحدث هذه التبدلات في النساء أكثر مما تحدث في الرجال، نتيجة توقف إفراز الاستروجين الذي من وظائفه تثبيت الكلس على العظام. وتزداد هذه التبدلات حدوثاً وخطورة في المدخنين والكحوليين والمصابين بعوز الكلسيوم وفيتامين د، وساكني الأحياء التي لا تتعرض دورهم فيها للشمس، وفي النساء اللواتي ينقطع طمثهن باكراً.
ينقص صبيب القلب تدريجياً مع تقدم العمر، ويتعلق ذلك بارتفاع الضغط الشرياني وزيادة المقاومة المحيطية الناتجة عن تصلب الأوعية، ويزداد عدد الوفيات بأمراض القلب بعد سن الخامسة والستين وهي عند الرجال أكثر منها عند النساء، ويزيد من حدوثها طريقة التغذية، والتدخين، وتناول الكحول، والبدانة.
ويتأثر جهاز الهضم بنقص إفراز الأنزيمات فتنقص التغذية بسبب ذلك، ولأسباب أخرى منها نقص المضغ إذا كان الشيخ يعاني من مشكلات في أسنانه، ومنها تأثير بعض الأدوية التي يتناولها المريض لإصابته بأمراض أخرى في إنقاص بعض المواد الضرورية لعملية الهضم، وينجم عن ذلك نقص الحديد وفاقة الدم، وما يتلو ذلك من وهن عضلي وتعب عام.
أمراض الجهاز التنفسي
ويتأثر جهاز التنفس خاصة عند سكان المدن بسبب تلوث الهواء بالغازات المنبعثة من عوادم السيارات والمعامل، إضافة إلى تعرض هذا الجهاز إلى كثير من المواد المحسسة الزراعية أو الصناعية أو البترولية المنشأ،مما يعرض المسنين إلى مظاهر الربو والقصور التنفسي الانسدادي المزمن.
وتتأثر الحواس ولاسيما السمع والبصر، فالسمع ينقص بدرجات مختلفة في 50% ممن تجاوزت أعمارهم الخامسة والستين، وذلك لآفة في الأذن الداخلية، أو لإصابة العصب السمعي، وتزيد حوادثه في المصابين بالداء السكري، وبارتفاع الضغط الشرياني، وبالتعرض المديد للضجيج. ويؤدي نقص السمع إلى تعرض المصاب لحوادث السير، وإلى عدم قدرته على التفاهم مع من يحيط به، مما يشعره بالنقص، وينتهي به الأمر أحياناً إلى الميل للعزلة وما يجره ذلك من مشكلات.
أما البصر فينقص أيضاً مع تقدم السن لإصابة الشيوخ بالساد أو بالزرق، ويزداد خطر الإصابة في السكريين لإصابتهم باعتلال الشبكية السكري، ومن أهم أسباب نقص البصر كذلك استحالة اللطخة الصفراء التي تنتهي بفقد البصر.
ومن أكثر مظاهر التشيخ والشيخوخة شأناً المظاهر النفسانية، فالفكر لا يشذ عن القانون الحياتي العام، وهو خاضع لوظائف عصبية شديدة الحساسية لمسيرة تقدم السن، ويميز لتقدم السن من وجهة النظر العصبية النفسانية مظهران مختلفان: الأول هو التشيخ، وهو مسيرة طبيعية ترتبط بالحياة لا يمكن تجنبها أبداً، ولكن زمن ظهورها يختلف من شخص لآخر. والثاني: هو الشيخوخة التي تحدث فيها اضطرابات عصبية ونفسانية مرضية. ويتحول التشيخ في بعض الظروف المرضية من حالة طبيعية إلى شيخوخة مبكرة بدرجات مختلفة، وقد يكون من الصعب تمييز الحدود بين هذين المظهرين، ففي مرحلة التشيخ يطبع تقدم السن الذكاء والنشاط بطابع خاص، إذ يلاحظ المسن ضعفاً تدريجياً في ذاكرته وقدرته على الانتباه، وقدراته العقلية وتخيلاته ونشاطه، وكلل مبادراته وتطلعاته. وأكثر ما يميز عقلية المسن صعوبة اكتساب معارف جديدة، وصعوبة مواجهة الحالات الطارئة وتدبيرها. ويصعب على المسن في الغالب التكيف مع حالته الجديدة ويتعلق ذلك بحالته النفسية وعاداته وطباعه قبل هذه المرحلة التي تتطلب منه إعادة ترتيب اهتماماته لتناسب وسائله وقواه، وعلى الرغم من ضعف الأداء فليس كل شيء سلبياً في هذه السن المتقدمة، والانقطاع عن العمل نهائياً غير محمود، فالتفكير يبقى سليماً جداً لفترة طويلة من الوقت، وعلى نقيض ذلك قد يصبح أحياناً أفضل بما اكتسبه الشخص من خبرات اجتماعية وعملية، وحكمة بعض كبار السن وذكاؤهم وقدرتهم على حل الكثير من المعضلات أمر معروف، أما إذا كانت طبيعة الشخص قبل هذه السن غير مستقرة فتظهر في بداية الأمر المنعكسات الناجمة عن الفراغ كالكآبة والحصر والشعور بالإخفاق وعدم الرضا والانطواء، ويأبى بعضهم الاعتراف بتقدم السن ويرفض الانقطاع عن العمل ولو انه لا يحسنه.
الاضطرابات العقلية
وتسيطر في الشيخوخة الاضطرابات العقلية بشدة في السلوك الاجتماعي، وتفسر بنقص الخلايا الدماغية باستمرار مع ضمور القشرة والمادة البيضاء، ويُرى هذا في معظم حالات الضعف العقلي المترقي الذي يسمى العته الشيخي senile dementia، وهو تطور أكثر عمقاً من التطور البسيط الذي يُرى في عدد من الشيوخ، وقد تكون الآفات الدماغية في هذا العته الشيخي وحده من نوع التنكس الخلوي، أو تكون وعائية بتصلب الشرايين الدماغية مع عدد من بؤر التلين في الجملة العصبية، أو تكون مختلطة بتنكس الخلايا تنكساً بدئياً تالياً لتصلب الشرايين، ولا توجد معالجة توقف سير هذه الآفات المستمر. يبدأ هذا العته في سن الخامسة والستين أو السبعين، وتزداد حوادثه مع طول عمر الإنسان وتشكل قضية اجتماعية اقتصادية مقلقة، لأن شروط الحياة الحديثة في المدن، وتدني الوضع الاقتصادي، وإعطاء الأولويات في الإنفاق على الأمور الحياتية تجعل الأسر أقل احتمالاً لشيوخها المعتوهين الذين غالباً ما يكونون في حالة هياج شبه مستمر.
ومن الأمراض النفسية في الشيخوخة الاكتئاب السوداوي melancholia، وحالات المس، والهذيان delirium المزمن من النوع الاضطهادي، والزور paranoia.
وتشتد الاضطرابات العقلية في الشيخ بالبؤس والارهاق والكحولية والعوز الغذائي أو الإفراط به والعزلة العاطفية والرضوض الجسدية والصدمات العاطفية وحالات الهجر وخيبة الأمل.
يجب أن توَفَّر لكبار السن شروط مادية محترمة في مسكن لائق، وأن يحاطوا بعناية الأهل والأصدقاء، وأن توفر لهم أعمال تتفق وإمكاناتهم، فالبطالة أكثر إيذاءاً من العمل المضني.
أما الاضطرابات النفسانية للتشيخ فتتطلب في الغالب الاستشفاء الذي يتجه إلى دراسة حالة المريض دراسة دقيقة، وتقديم العلاج اللازم بعد ذلك، ولو أن هذه المعالجات لا تمنع من تقدم الضعف العقلي بسرعات مختلفة نحو العته النهائي.
وفي حالات الهياج تستعمل الأدوية الحالة للأعصاب بمقادير قليلة، والمهدئات ضد القلق ومضادات الكآبة (بمقادير قليلة وبحذر) لإصلاح العناصر المؤدية للكآبة، وقد تكون الصدمات الكهربائية ضرورية أحياناً.
تؤثر هذه المعالجات في المزاج والقلق والهياج، ولكنها قليلة التأثير في اضطرابات الذاكرة والانتباه والإعاقة النفسية، وعلى النقيض، فإن الفيتامينات وموسعات الأوعية قد تقدم بعض الفائدة في تحسن الذكاء والتركيز والانتباه، ولكن بعض هذه الأدوية يسبب الهياج ولا يُجنى منها إلا تحسن مؤقت في مسيرة مرضية غير قابلة للتراجع. أما الهرمونات فتستعمل بمقادير قليلة في استطبابات معينة ومحددة، ولا تعطى إلا بإشراف طبي مباشر.
وثمة أمر أخير يجب الانتباه إليه بسبب ما يتعرض له الشيوخ من أمراض عضوية كثيرة، وهو معالجة هذه الحالات بصورة مبكرة وصحيحة، لأن تراكمها يزيد من إعاقة المريض وعدم قدرته على التلاؤم مع ظروف الحياة، ويدفع، إضافة إلى إصاباته هذه، إلى زيادة أعراض التشيخ والتي تدخله في مرحلة البؤس واليأس.
شيخوخة الخلايا
يركز البحث في هذا الاتجاه على استقصاءات في مزارع خلايا بشرية. وكان يعتقد في الخمسينات أن الخلايا البشرية القادرة على التكاثر في الجسم تستطيع أن تتناسخ في المزارع الخلوية بلا نهاية. ولو كان هذا صحيحا لكان يعني أن البشر يشيخون ويموتون ليس بسبب برنامج داخلي لتحلل خلاياهم، ولكن بسبب عمليات تنشأ خارج الخلايا عند مستوى عال من التنظيم الفيزيولوجي.[3]
وقد تداعت هذه المعتقدات عام 1961 عندما قرر L.هايفليك و S. P. مورهيد (اللذان كانا حينذاك في معهد وستار)أن الأرومات الليفية fiberoblasts العادية في الإنسان لها عدد محدد من المرات التي تنقسم فيها. وبصورة أكثر تحديدا، إنها تنقسم عددا مقررا من المرات ـ نحو 50 مرة ـ حيث تستطيع تجمعات من الأرومات الليفية المأخوذة من جنين حديث أن تتضاعف.
ومنذ ذلك الوقت تم التأكد عدة مرات من وجود ما يسمى الآن حد هايفليك Hayflick limit، ومن ثم فإن التحليلات في سبب توقف الخلايا البشرية عن التكاثر في مزارعها، قد تقدم الدليل على انهيار الكائن ككل. «وبفهمنا لماذا تتوقف الخلايا عن التكاثر قد يمكننا فهم بعض الأمور عن الشيخوخة،» هذا ما قاله R.J. سميث (من كلية بايلور الطبية)، ولكنه أضاف قائلا: «إني أعتقد بكل تأكيد أنه سيكون الأمر أكثر صعوبة ـ ربما، على الأقل ألف مرة ـ لفهم الشيخوخة في الفرد السوي من البشر.»
واحتمال أن شيخوخة الخلايا في أوعية المختبر تتعلق بشيخوخة الجسم قد اكتسب دعما من العديد من الاكتشافات. فقد اتضح أن المقدرة على التضاعف تنحدر باطراد مع سن واهبي الخلايا. وبالمثل، فإن الأرومات الليفية من المرضى الذين ابتلوا بمتلازمة ڤيرنر لا تستطيع التناسخ عدد مرات تناسخ خلايا مأخوذة من إنسان عادي في السن نفسه. وكذلك فإن كل طرز الخلايا البشرية التي تمت دراستها حتى الآن ذات حدود خاصة لتكاثرها في مزارع الخلايا.
وقد تعرف الباحثون في بضع السنوات الأخيرة الجينات التي تتغير تأثيراتها بانتظام مع فقدان الأرومات الليفية في المزارع لقدرتها على التضاعف ـ تماما كما هو متوقع فيما لو كان لديها برنامج جيني يؤدي إلى الشيخوخة. ولدى الباحثين برهان على أن جينات في الكروموسومَيْن 1 و 4 تسهم في هذا الفقد لقدرة التضاعف، كما أن J.كمپيسي (التي تعمل حاليا في مختبر لورنس بركلي) قد حددت أن تعطيل الجين c-ƒos يسبق، بل ومن المحتمل أن يؤثر في الكثير من التغيرات الأخرى التي أمكن تعرفها. وعندما يخرس الجين c-ƒos نهائيا تفشل خلايا الأرومات الليفية في مضاعفة حمضها النووي «الدنا»، ومن ثم تفقد قدرتها على الانقسام.
ويشك سميث في أن الجين c-ƒos نفسه قد تهدئه في النهاية عملية أولية إلى حد أبعد. وهو يعبر عن حدسه قائلا: «ما أعتقد أنه يحدث فعلا هو أن الخلايا تنتج مثبطا يوقف بداية تخليق الدنا.» وهو يقول: إنه يظن أنه قد استنسل cloned الجين الخاص بالمثبط، ولذا فإنه سوف يكون قادرا، قريبا جدا، على أن يضع هذه الفكرة موضع الاختبار. ولكنه يعترف بسرعة بأن مفهومه هذا هو واحد من تفسيرات كثيرة ممكنة. «ونحن لم نصل بعد إلى النقطة التي نستطيع عندها فصل السبب عن الأثر، إذ إن نشاط المثبط قد يكون أثرا ثانويا لشيء آخر.»
وأحد احتمالات هذا «الشيء الآخر» هو قِصَر القطع الطرفية telomeres، أي الامتدادات الطويلة من الدنا التي تغطي نهايتي كل كروموسوم وتحميهما من التآكل. وقد وجد B.C .هارلي (من جامعة ماك ماستر في أونتاريو) و W.C.گريدر (من مختبر كولد سبرنگ هاربور)وزملاؤهما أن طول القطع الطرفية يتناقص باطراد في الخلايا الجسدية التي تتضاعف في الجسم، كما أن خلايا الأرومات الليفية في المزارع تتناقص كذلك في أثناء شيخوختها. وفضلا عن ذلك فإن طول القطعة الطرفية ينبئ بقدرة الخلايا على الانقسام أكثر من دلالة سنِّ معطي الخلايا.
ومن المفترض أن القصر يحدث بسبب وجود عيب غريب في الآلية المسؤولة عن تضاعف الدنا في أثناء انقسام الخلية. إنها تزيل جزءا بسيطا من كل نهاية في كل نسخة جديدة تصنعها من الدنا.
وتعني هذه النتائج أن القطع الطرفية يمكن اعتبارها الساعة التي تحدد فقد القدرة التكاثرية للخلايا. ومما يثير الاهتمام أن هارلي و گريدر قررا أن طول القطعة الطرفية يبقى كما هو، بل ربما ازداد زيادة بسيطة في الحيوان المنوي وفي الخلايا المتحولة أو الخالدة التي لا تموت. وهذا البقاء قد يساعدنا في تفسير عدم فقد الخلايا الجرثومية السوية أو الخلايا السرطانية قدرتها على التضاعف.
وهكذا نستطيع أن نقيم الحجة على أن الجسم يتحلل عندما يتحتم أن تفقد الأعضاء قدرتها على تعويض الخلايا التالفة. ومن ناحية أخرى، يرد النقاد بأن الإنسان لا يموت بسبب كف خلايا الأرومات الليفية عن التضاعف، حيث إن الخلايا عادة ما تنقسم انقسامات عديدة عندما يتعرض «مالكها» إلى الفناء. ويشير المتشككون أيضا إلى أن دراسات شيخوخة التضاعف لا يمكن أن تلقي الكثير من الضوء على العمليات المؤدية لتدهور الخلايا التي لا تنقسم، وأبرزها الخلايا العصبية وخلايا عضلة القلب، فهذه الخلايا تعمل عدة سنوات بصورة تدعو للإعجاب.
ومن بين أولئك النقاد نذكر روز الذي يصف العمل في مزارع الخلايا بأنه «جميل تقنيا». ولكنه يصر على أن الباحثين مازالوا في الواقع «يديرون مغازلهم» وأنهم يسبرون probing تكاثر الخلية وحدوده على نحو مفيد، إلا أنه مازال عليهم أن يبينوا أن نتائجهم تكشف أي شيء حول كيفية شيخوخة الإنسان. ويضيف روز: «فلو أن علماء الخلية هؤلاء كانوا يكشفون حقا أي شيء مهم عن شيخوخة الكائنات الحية، لكانوا قادرين على استثمار نتائجهم في تأجيل الشيخوخة، ولكنهم لم يفعلوا ذلك قط، بعد مرور 30 عاما من الدراسة والبحث.»
ويظن سميث أن هذه الانتقادات غير عادلة، وهو يقول: إن التغيرات الوراثية التي شوهدت في خلايا الأرومات الليفية تمثل وجها واحدا فقط من عملية الشيخوخة، ولكن لهذا الوجه الواحد مع ذلك دلالاته الكامنة. وهو يقول: «لعل ما يحدث هو وجود مناطق محلية لا تعمل فيها الخلايا بكفاءة ولا يمكن استبدالها.» وهو يستدل على ذلك بخلايا البطانة الداخلية للأوعية الدموية: «إذا فقدت الخلايا البطانية في منطقة صغيرة من الوعاء الدموي قدرتها على التكاثر، ففنيت أو صارت عاجزة عن أداء وظيفتها، فإن هذا قد يؤدي لعمليات تنتهي بتصلب الشرايين.»وهو يضيف أن فقد القدرة على التكاثر يبدو أيضا أنه مشكلة في جهاز المناعة.
يتساءل سميث قائلا: «أنا غير متأكد أننا نموت بسبب شيء واحد محدد، ولكنني أعتقد أن فقد قدرة الخلايا على التكاثر قد يكون عاملا له سهم مشارك مهم.»ويوافق على ذلك G.V.كريستوفالو ، من الكلية الطبية في پنسلڤانيا وأحد كبار المدافعين عن الدراسات التي تجري خارج الجسم (في المختبر) in vitro. ففي محاضرة له في مؤتمر حديث عن البيولوجيا الجزيئية للشيخوخة، أشار إلى أن الخلايا التي تشيخ في المزارع تبدو مشابهة للخلايا التي تشيخ في الجسم. وهو يؤكد ذلك قائلا: إنه إضافة إلى فقد تلك الخلايا قدرتها التكاثرية تصبح أكبر حجما وتظهر تغيرات في بنيان نواها. ثم قال: «إنني سوف أكون في موقف صعب، لو أخذت أقيم الحجج على أن الخلايا لا تعمل شيئا عدا أنها تشيخ وفق أي تعريف نعتمده للشيخوخة.»
كيف يمكن للباحثين التوفيق بين النتائج الخاصة بخلايا الأرومات الليفية مع النظرية التطورية؟ يرى كثير من الباحثين، ومن بينهم سميث، أن الحد من القدرة التكاثرية قد يكون ناتجا ليس من برنامج خاص بالموت ولكن كوسيلة للدفاع ضد السرطان. وبناء على هذا قد تكون القدرة على التكاثر مثالا آخر للپيليوتروپية المتعارضة، و «البرنامج»الذي يساعدنا على مقاومة السرطان يحول في الوقت نفسه دون الخلود. وبالرغم من أن كثيرا من الناس يمرضون بالسرطان فإن المقاومة المستقرة في داخل أجسامنا تجعلنا أقل عرضة للأورام من الكثير من الحيوانات.
الاختلافات الثقافية
المجتمع
الآثار المعرفية
التأقلم والسعادة
التقاعد
 مقالة مفصلة: تقاعد
مقالة مفصلة: تقاعد
عادة ما يمر المسنون بمرحلة التقاعد، وما يترتب عليهه من آثار سلبية وإيجابية.[4]
التأثير الاجتماعي
التحسن النفسي
شيخوخة ناجحة
نظريات
نظريات حيوية
نظريات غير حيوية
الوقاية من الشيخوخة
 مقالة مفصلة: إطالة الحياة
مقالة مفصلة: إطالة الحياة
في 8 يونيو 2023، اقترحت دراسة جديدة أن نقص التورين قد يلعب دوراً هاماً في حدوث الشيخوخة. حققت الدراسة في تأثير هذا الحمض الأميني على الصحة وطول العمر عبر تجارب معملية على حيوانات مختلفة، وأشارت النتائج إلى أن استعادة فقدان التورين المرتبط بالعمر من خلال المكملات قد حسن العمر الصحي للديدان والقوارض والرئيسيات غير البشرية.[5]
سُمي حمض التورين بهذا الاسم لأنه تم التعرف عليه لأول مرة في بول الثيران- هو أحد أكثر الأحماض الأمينية وفرة الموجودة في البشر والحيوانات المعقدة الأخرى. كما هو الحال مع العديد من الأشياء، تنخفض تركيزات التورين في الدم مع تقدم العمر في الفئران والقرود والبشر، وفي البشر ترتبط المستويات المنخفضة من التورين بمخاطر أعلىلمرض السكري من النوع 2 وارتفاع ضغط الدم والبدانة والالتهابات وأمراض الكبد.[6]
لكن لم يتضح ما إذا كان التورين يؤثر على حدوث الشيخوخة. شرعت هذه الدراسة في التأكد مما إذا كانت وفرة التورين التي تنخفض مع تقدم العمر هي عامل نشط في العملية - أو عامل عابر خلال حدوث الشيخوخة على المدى الطويل.
أظهرت الأبحاث السابقة التي أجريت على أنواع مختلفة من الحيوانات أن نقص التورين في السنوات المبكرة من العمر يؤدي إلى ضعف وظيفي في العضلات والهيكل العظمي والعينين والجهاز العصبي، وجميعها مرتبطة بالاضطرابات المرتبطة بالشيخوخة. في حين أظهرت التجارب السريرية الصغيرة التي تبحث في مكملات التورين نتائج واعدة في الأمراض الأيضية والالتهابية، ظل تأثير تركيزات التورين على صحة الحيوان وطول العمر غير مفهوم بشكل جيد.
لفهم ما إذا كانت وفرة التورين تؤثر على الحياة الصحية بشكل أفضل، قام بارميندر سينج، زميل في مختبر كاباهي في معهد باك، وزملاؤه بقياس تركيزات التورين في الدم في الفئران والقرود والبشر بأعمار مختلفة.
اكتشف الباحثون أنه في القرود البالغة من العمر 15 عامًا، كانت تركيزات التورين في الدم أقل بنسبة 85% من تلك الموجودة في القرود البالغة من العمر 5 سنوات. وبالمثل، انخفضت مستويات التورين بأكثر من 80% على مدى عمر الإنسان. أظهرت الفئران المتقدمة في السن أيضًا انخفاض مستويات التورين، ولاحظ الباحثون أن الفئران التي تفتقر إلى الناقل الرئيسي للتورين كان لها عمر أقصر عند البالغين.
ومع ذلك، كان الانخفاض في مستويات التورين قابلاً للانعكاس من خلال مكملات التورين. في الواقع، زادت المكملات من متوسط عمر الديدان والفئران بنسبة 10-23% و10-12% على التوالي. والجدير بالذكر أن إعطاء الفئران التورين عن طريق الفم بجرعات 500 و1000 ملليجرام لكل كيلوجرام من وزن الجسم يوميًا كان مرتبطًا بتحسين في القوة والتنسيق والوظائف الإدراكية. علاوة على ذلك، فقد أبطأ العديد من السمات المميزة للشيخوخة: فقد قلل من الشيخوخة الخلوية، وحمايته من نقص التيلوميراز، والتغلب على الخلل الوظيفي في الميتوكوندريا، وقلل من تلف الحمض النووي والالتهاب.
أظهرت الفئران في منتصف العمر التي تم تغذيتها بالتورين تحسنًا في أداء العظام والعضلات والبنكرياس والمخ والدهون والأمعاء والجهاز المناعي، ولوحظ أيضًا تأثيرات على طول العمر في القرود وقرود المكاك الريسوسي في منتصف العمر، حيث أثرت مكملات التورين أيضًا بشكل إيجابي على العظام، الصحة الأيضية والمناعية.
تسلط هذه النتائج المقنعة الضوء على إمكانات مكملات التورين كإستراتيجية مضادة للشيخوخة، وهناك ما يبرر إجراء مزيد من البحث. من أجل تحديد ما إذا كانت مكملات التورين تزيد من العمر الافتراضي للأشخاص، ستكون هناك حاجة لإجراء تجارب سريرية على البشر؛ تحتاج أيضًا إلى تحديد المخاطر المحتملة المرتبطة بمكملات التورين، خاصة وأن الجرعات المستخدمة في دراسة سينج وآخرون كانت مرتفعة نسبيًا، مما يؤكد الحاجة إلى توخي الحذر عند اعتبار التورين مكملًا لطولالعمر.
أثناء دعوتهم لإجراء تجارب إكلينيكية على التورين، حذر المؤلفون الرئيسيون للدراسة العامة من عدم تناول المكملات دون إشراف طبي- بما في ذلك عدم المبالغة في تناول مشروبات الطاقة - مشيرين إلى أن هناك طرقًا أخرى لتعزيز المستقلب الطبيعي. وأظهرت الدراسة أن ممارسة التمارين الرياضية لفترة زمنية أدت إلى زيادة تركيز مستقلبات التورين في الدم والتي قد تفسر جزئياً التأثيرات المضادة للشيخوخة الناتجة عن التمارين الرياضية. يمكن أيضًا الحصول على التورين من خلال النظام الغذائي؛ يمكن الحصول على أعلى كميات من التورين من المحا ، وخاصة الأسقلوب وبلح البحر والمحار، كما يمكن العثور على كميات كبيرة من التورين في لحم الديك الرومي والدجاج.
أجريت الكثير من التجارب على الديدان الخيطية في معهد باك. يصف الأستاذ جوردون ليثجو، وهو من بين 56 باحثًا ساهموا في الدراسة، النتائج بأنها مذهلة: "كيف يمكننا أن نرى تأثيرات التورين المضادة للشيخوخة في الديدان، ثم في الفئران ثم الرئيسيات من الجنسين. هذه رسالة قوية حول تأثيرات المستقلبات التي تحدث بشكل طبيعي وما يمكن أن يحدث عندما يتم استعادتها إلى مستويات الشباب. هذه النتائج تمنحني الأمل في أن التدخلات البسيطة والآمنة يمكن أن يكون لها تأثير كبير على الشيخوخة".
بحسب جولي أندرسن، الأستاذة في معهد باك، وهي مؤلفة مشاركة أخرى تعتبر هذه الورقة البحثية انتصارًا كبيرًا لمجال علم الشيخوخة متعدد التخصصات. "على سبيل المثال، تم تضمين صحة العظام في هذه البحث. بالنسبة للجزء الأكبر، لا يتحدث الأشخاص المهتمون بصحة العظام إلى الأشخاص الذين يدرسون جوانب أخرى من الشيخوخة. هذه الدراسة تكسر الجدران بين الخميرة والديدان والفئران والرئيسيات، كما تقول أندرسن: "إنه مثال رائع لكيفية تحقيق اختراقات من خلال كونك متعدد التخصصات".
قاد عالم الأبحاث د. مانيش شامولي، الكثير من أعمال على الديدان والخلايا العصبية المذكورة في الورقة البحثية، وأصبح المؤلف الثاني للدراسة. يقول شامولي: "يبدو أن التورين قد يعمل، جزئيًا، من خلال زيادة نشاط مركب الميتوكوندريا 1، وليس مفاجأة عند النظر في العديد من السمات المميزة للشيخوخة التي تنطوي على خلل في الميتوكوندريا".
سيجري شامولي مزيدًا من الأبحاث حول الديدان لتحديد آليات عمل التورين المحددة. ويضيف شامولي: "هذه الورقة قوية جدًا لأنه قد أعيد إنتاج النتائج ذاتها في العديد من المعامل؛ كان هناك 34 منظمة بحثية مسجلة في الورقة، وأضاف: "مدرجًا فريقًا يضم علماء من جامعة كولومبيا بمدينة نيويورك، وجامعة واشنطن في سياتل وجامعة هارفارد في بوسطن ومعهد ماساتشوستس للتكنولوجيا في الولايات المتحدة، إلى جانب منظمات في نيودلهي، الهند وأستراليا وألمانيا وإيطاليا وفرنسا والمملكة المتحدة وسنغافورة وتركيا.
أبحاث
إبطاء الشيخوخة
بحسب دراسة أُجريت في كلية الملك بلندن وأُعلن نتائجها في مايو 2025، يبدو أن المادة الكيميائية الموجودة بشكل أساسي في الشوكولاتة الداكنة تعمل على إبطاء معدل الشيخوخة البيولوجية لدى البشر، لكن ليس من الواضح ما إذا كان تناول الشوكولاتة مفيداً بشكل عام. قد تحتوي الشوكولاتة على مادة كيميائية ذات خصائص مضادة للشيخوخة، لكن يجب عدم المبالغة في تناولها. بحسب رامي سعد من كلية الملك بلندن: "تحتوي الشوكولاتة الداكنة على الكثير من الأشياء، ولكل شيء إيجابيات وسلبيات". المادة الكيميائية المذكورة هي الثيوبرومين، معروفة على الأرجح بتأثيرها القاتل على الكلاب. لكن ثبت أيضاً أنها تُطيل عمر سلالة واحدة من الديدان البسيطة، وهناك بعض الأدلة على فوائدها الصحية للبشر. لمعرفة المزيد عن هذه الفوائد المحتملة، حلل سعد وزملاؤه بيانات 500 امرأة من دراسة أُطلق عليها اسم TwinsUK. وقد قاست هذه الدراسة مستويات عدد من المكونات في الدم، بما في ذلك الثيوبرومين. كما بحثت الدراسة في التغيرات الوراثية - وجود أو غياب علامات كيميائية على الحمض النووي تُغيّر نشاط الجينات - في خلايا الدم. يرتبط بعض هذه التغيرات بالشيخوخة، ويمكن استخدامها لتقدير ما إذا كان "العمر البيولوجي" للشخص أعلى أو أقل من عمره الزمني.[7]
تقول جوردانا بيل، عضوة الفريق في كلية الملك بلندن: "وجدنا صلة بين مستويات الثيوبرومين في الدم والتقديرات الجينية للعمر البيولوجي". الأشخاص الذين لديهم مستويات ثيوبرومين أعلى كانوا أكثر عرضة لأن يكون عمرهم البيولوجي أقل من عمرهم الزمني. ثم قام الفريق بتحليل بيانات مماثلة من 1160 فرداً من دراسة أجريت في ألمانيا تسمى KORA، ووجدوا نفس الارتباط. من نقاط قوة الدراسة الأخيرة أنها تعتمد على قياسات مباشرة للثيوبرومين في الدم، بدلاً من تقارير الناس عن كمية الشوكولاتة التي تناولوها، مثلاً. لكن هذا يعني أيضاً أن الفريق لا يستطيع الجزم بمصدر الثيوبرومين. يمكن أن يتكون الثيوبرومين من تحلل الكافيين، مع أن هذا لا يُنتج سوى كميات ضئيلة منه. يقول سعد إن المصدر الرئيسي للثيوبرومين في النظام الغذائي هو مواد الكاكاو الصلبة. الشوكولاتة الداكنة غنية بالمواد الصلبة، بينما تحتوي شوكولاتة الحليب على مستويات أقل، بينما لا تحتوي الشوكولاتة البيضاء على أي منها. ويضيف سعد: "لا أتوقع أن نحصل على كمية كبيرة من الثيوبرومين من قطعة ميلكي بار".
يؤكد كل من بيل وسعد على أنه لا ينبغي اعتبار نتائجهما دليلاً على أن تناول المزيد من الشوكولاتة الداكنة سيطيل العمر. فقد تكون الآثار السلبية لمكونات أخرى، مثل السكر، تفوق أي آثار مفيدة. ويضيف بيل أن هناك حاجة إلى مزيد من الدراسات لتأكيد النتائج، لكن الفريق لا يملك التمويل اللازم لإجرائها. يقول ستڤ هورفاث من جامعة كاليفورنيا في لوس أنجلوس، الذي طور مقياس الشيخوخة الجيني الذي يستخدمه الفريق: "من المؤكد أن هذا يعزز التزامي بتناول الشوكولاتة الداكنة، لكنني أختار نسخة الكيتو التي لا تحتوي على سكر". مع ذلك، يقول مايكل وينك من جامعة هايلدلبرگ بألمانيا، الذي أجرى الدراسة على الديدان، إن هناك بعض العيوب. أحدها أن الشوكولاتة تحتوي على العديد من المواد الكيميائية المعروفة باسم الپولي فينولات، والتي قد تُعزز تأثير الثيوبرومين. ويضيف سعد قائلاً: "لا أعتقد أن بحثنا قادر على كشف ما إذا كان الأمر يتعلق بالثيوبرومين وحده أو ما إذا كان الثيوبرومين يتفاعل مع شيء آخر".
معيار الشيخوخة
طب الشيخوخة
 مقالة مفصلة: طب الشيخوخة
مقالة مفصلة: طب الشيخوخة
وكان من نتائج الاهتمام بالمسنين وحياتهم أن انبثقت شعبتان علميتان تتعلقان بهما، أطلق على الأولى طب الشيخوخة أو طب الشيوخ geriatrics وتعنى بشؤونهم الطبية المحضة أي بأمراضهم. والثانية علم الشيخوخة أو درس معضلات التشيخ gerontology وتهتم بشروط حياتهم السريرية والبيولوجية والتاريخية والاجتماعية السوية والمرضية.
انظر أيضا
- التحكم في الحركة في الشيخوخة
- شيخوخة المخ
- الشيخوخة في اوروپا
- Biodemography
- Biological immortality
- وفاة
- Endocrinology of Development
- Gerontology
- متوسط العمر المتوقع
- List of life extension-related topics
- Longevity
- الذاكرة والشيخوخة
- شيخوخة السكان
- تقاعد
- هرم (شيخوخة)
- نظرية الخلايا الجذعية والشيخوخة
- قراءة كتابين عن الشيخوخة
- لماذا يشيخ البشر
- Ageing brain
- Ageing movement control
- Ageing of Europe
- Ageing studies
- Anti-ageing movement
- Biodemography of human longevity
- Biogerontology
- Biological immortality
- Biomarkers of ageing
- Clinical geropsychology
- Death
- DNA damage theory of aging
- Epigenetic clock
- Evolution of ageing
- Genetics of ageing
- Gerontechnology
- Gerontology
- Gerascophobia
- List of life extension-related topics
- Longevity
- Mitochondrial theory of ageing
- Neuroscience of ageing
- Old age
- Particulates
- Pollutants
- Population ageing
- Progeria
- Rejuvenation
- Stem cell theory of ageing
- Supercentenarian
- Thermoregulation in humans
- Transgenerational design
مرئيات
| نقص حمض التورين قد يكون سبباً في الشيخوخة وقصر العمر، يونيو 2023. |
الهوامش
- ^ Bowen RL, Atwood CS (2004). "Living and dying for sex. A theory of aging based on the modulation of cell cycle signaling by reproductive hormones". Gerontology. 50 (5): 265–90. doi:10.1159/000079125. PMID 15331856.
- ^ عدنان تكريتي، إبراهيم حقين وليد النحاس. "الشيخوخة". الموسوعة العربية. Retrieved 2011-07-12.
- ^ اتجاهات في البيولوجيا لماذا نشيخ؟ مجلة العلوم
- ^ Panek, Paul E.; Hayslip, Bert (1989). Adult development and ageing. San Francisco: Harper & Row. ISBN 0060450126.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ^ "Taurine deficiency as a driver of aging". science.org. 2023-06-08. Retrieved 2023-06-17.
- ^ "Taurine deficiency: New research identifies possible driver for aging". longevity.technology. 2023-06-08. Retrieved 2023-06-17.
- ^ "Key component of dark chocolate might have an anti-ageing effect". newscientist.com. 2025-05-01. Retrieved 2025-05-12.
المصادر
- Bass, S.A. (2006). Gerontological Theory: The Search for the Holy Grail. The Gerontologist, 46, 139-144.
- Bath, P.A. (2003). Differences between older men and woman in the Self-Rated Health/ Mortality Relationship. The Gerontologist, 43 387-94
- Charles, S.T.; Reynolds, C.A.; Gatz, M. (2001). "Age-related differences and change in positive and negative affect over 23 years". Journal of Personality and Social Psychology. 80 (1): 136–151. doi:10.1037/0022-3514.80.1.136. PMID 11195886.
- Mather, M.; Carstensen, L. L. (2005). "Ageing and motivated cognition: The positivity effect in attention and memory" (PDF). Trends in Cognitive Sciences. 9 (10): 496–502. doi:10.1016/j.tics.2005.08.005. PMID 16154382.
- Masoro E.J. & Austad S.N.. (eds.): Handbook of the Biology of Ageing, Sixth Edition. Academic Press. San Diego, CA, USA, 2006. ISBN 0-12-088387-2
- Moody, Harry R. Ageing: Concepts and Controversies. 5th ed. California: Pine Forge Press, 2006.
- Zacks, R.T., Hasher, L., & Li, K.Z.H. (2000). Human memory. In F.I.M. Craik & T.A. Salthouse (Eds.), The Handbook of Ageing and Cognition (pp. 293–357). Mahwah, NJ: Erlbaum.
- A small-cell lung cancer genome with complex signatures of tobacco exposure Nature 463, 184-190 (14 January 2010)
قراءات إضافية
- VITALITY AND AGING: IMPLICATIONS OF THE RECTANGULAR CURVE. James F. Fries and Lawrence M. Crapo. W. H. Freeman and Company, 1981.
- MODERN BIOLOGICAL THEORIES OF AGING. H. R. Warner, R. N. Butler, R. L. Sprott and E. L. Schneider. Raven Press, 1987.
- LONGEVITY, SENESCENCE, AND THE GENOME. Caleb E. Finch. University of Chicago Press, 1990.
- MOLECULAR BIOLOGY OF AGING: PROCEEDINGS OF A UCLA COLLOQUIUM, HELD AT SANTA FE, N. M., MARCH 4-10, 1989. Edited by Caleb E. Finch and Thomas E. Johnson. Wiley-Liss, 1990.
- REVIEW OF BIOLOGICAL RESEARCH IN AGING, Vol. 4. Edited by Morton Rothstein. Wiley-Liss, 1990.
- EVOLUTIONARY BIOLOGY OF AGING. Michael R. Rose. Oxford University Press, 1991.
- Scientific American, December 1992
وصلات خارجية
 Media related to Aging at Wikimedia Commons
Media related to Aging at Wikimedia Commons- American Psychological Association's Office on Aging
- EPSRC funded research consortium dedicated to extending quality life
- Laboratory of Endocrinology, Aging, and Disease [1]