الهرمون المحفز للدرقية
| الهرمون المحفز للدرقية، ألفا | |||||||
|---|---|---|---|---|---|---|---|
| المعرفات | |||||||
| الرمز | CGA | ||||||
| الرموز البديلة | HCG, GPHa, GPHA1 | ||||||
| NCBI gene | 1081 | ||||||
| HGNC | 1885 | ||||||
| OMIM | 118850 | ||||||
| RefSeq | NM_000735 | ||||||
| UniProt | P01215 | ||||||
| بيانات أخرى | |||||||
| Locus | Chr. 6 q14-q21 | ||||||
| |||||||
| الهرمون المحفز للدرقية، بيتا | |||||||
|---|---|---|---|---|---|---|---|
| المعرفات | |||||||
| الرمز | TSHB | ||||||
| NCBI gene | 7252 | ||||||
| HGNC | 12372 | ||||||
| OMIM | 188540 | ||||||
| RefSeq | NM_000549 | ||||||
| UniProt | P01222 | ||||||
| بيانات أخرى | |||||||
| Locus | Chr. 1 p13 | ||||||
| |||||||
الهرمون المحفز للدرقية إنگليزية: Thyroid-stimulating hormone (ويُعرف أيضاً بإسم thyrotropin, thyrotropic hormone, TSH أو hTSH for human TSH) هو هرمون نخامي يحفـّز الغدة الدرقية لانتاج الثيروكسين (T4)، ثم ثلاثي اليودوثيرونين (T3) الذي يحفظ استقلاب جميع أنسجة الجسم تقريباً.[1] هو هرمون پروتيني سكري تنتجه الخلايا الموجهة للدرقية في الغدة النخامية الأمامية، التي تنظم الوظائف الصماء للغدة الدرقية.[2][3] عام 1916، وجد بنت م. ألن وفليپ إ. سميث أن الغدة النخامية تحتوي على مادة موجهة للدرقية.[4]
يُفرز الهرمون المحفز للدرقية (TSH) من الجزء الأمامي من الغدة النخامية بتأثير من الهرمون المطلق للدرقية (TRH) من تحت المهاد المخي، والذي يعمل على تحفيز نمو الغدة الدرقية وإفراز الهرمونات منها. العلاقة بين هذا الهرمون وهرمون الغدة الدرقية علاقة وثيقة، فعندما يقل إفراز هرمونات الغدة الدرقية يزداد إفراز TSH، والذي بدوره يحفز الغدة الدرقية على إفراز هذه الهرمونات، وعندما يرتفع مستوى هرمونات الغدة الدرقية فإن ذلك يؤدي الى تثبيط إفراز TSH، ويفرز هذا الهرمون بقدر متباين خلال اليوم، حيث يكون أعلى تركيزاً خلال الليل، وأقل تركيزاً بين الساعة الخامسة والسادسة مساء.
يستخدم تحليل الهرمون المحفز للدرقية في فحص حديثي الولادة لتشخيص قصور الغدة الدرقية المبكر. كما يستخدم لاكتشاف وتشخيص أمراض الغدة الدرقية، ومتابعة العلاج في حالات قصور الغدة الدرقية أو فرط نشاطها. وفي حالات فرط نشاط الغدة الدرقية تفرز الغدة كميات كبيرة من T3 و T4، وبالتالي يقل إفراز الغدة النخامية للهرمون لا يقل مستوى TSH في الدم. في المقابل يزداد إفراز TSH في حالات قصور الغدة الدرقية كمحاولة لتحفيز الغدة الدرقية على إفراز المزيد من هذه الهرمونات. في حال اظهر الفحص ارتفاعا في معدل الـ TSH فذلك يعني قلة نشاط الغدة الدرقية أي أنها لا تستجيب بالشكل المطلوب للتنشيط الذي يحدث عن طريق TSH، وهو ما يدفع الغدة النخامية إلى إفراز كميات متزايدة من هذا الهرمون لتحفيزها على أداء وظيفتها. كما يدل ارتفاع معدل الـTSH الى وجود ورم في الغدة النخامية ويجعلها تفرز الهرمون بشكل متزايد من دون ضبط.[5]
انخفاض معدل الهرمون المحفز للدرقية يعني زيادة نشاط الغدة الدرقية بشكل كبير، حيث تعمل الهرمونات المفرزة منها على تثبيط عمل إفراز الهرمون المحفز للدرقية من الغدة النخامية، أو وجود ضرر في الغدة النخامية يمنعها من إفراز كميات كافية من الهرمون المحفز للدرقية. تنظم وظائف الغدة الدرقية بآلية التغذية العكسية عن طريق الدماغ، فعندما تكون مستويات هرمون الغدة منخفضة، تنتج منطقة ما تحت المهاد في الدماغ هرمون يعرف باسم هرمون الثيروتروبين (TRH)، الذي يجعل الغدة النخامية (الموجودة في قاعدة الدماغ) تفرج عن الهرمون المحفز للدرقية، الذي يحفزها لإطلاق المزيد من هرمون T4. يتم التحكم في الغدة الدرقية من قبل الغدة النخامية وتحت المهاد، وأي اضطراب يحدث في الغدة النخامية، يمكن أن يؤثر أيضا على وظيفة الغدة الدرقية ويسبب مشاكلها. إلا أن الغدة الدرقية، كغيرها من أعضاء الجسم، هي عرضة للكثير من الأمراض التي تؤثر عليها وعلى توازن الهرمونات التي تفرزها في الجسم؛ ومن المعروف إن مشاكل الغدة الدرقية الصحية صعبة ومزعجة، فيضطر المريض إلى تناول العلاجات على المدى الطويل أو اللجوء إلى التدخل الجراحي واستئصال الغدة الدرقية في حال لم تفلح العلاجات الدوائية، وهي الخطوة الأخيرة التي يلجأ اليها الأطباء نظراً لأهمية وجود هذه الغدة في الجسم ودورها الحيوي.
الفسيولوجيا
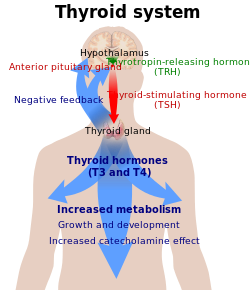
مستويات الهرمون
الهرمون المحفز للدرقية (الذي يبلغ عمره النصفي حوالي ساعة) يحفظ الغدة الدرقية على إفراز هرمون الثيروكسين (T4)، الذي يؤثر بشكل طفيف على الاستقلاب. يتحول الـ T4 إلى ثلاثي اليودوثيرونين (T3)، وهو هرمون نشط يحفز الأيض. يحدث ما يقارب 80% من هذا التحول في الكبد وأعضاء أخرى، و20% في الغدة الدرقية ذاتها.[1]
يثمتص الهرمون المحفز للدرقية على مدار عمره لكنه يصل لمستويات مرتفعة بصفة خاصة أثناء فترات النمو والتطور السريعة، وكذلك عند التعرض للضغوط النفسية.
في تحت المهاد، في قاعدة المخ، يُنتج الهرمون المطلق لموجه الدرقية (TRH). يحفظ هذا الهرمون الغدة النخامية الداخلية على إنتاج الهرمون المحفز للدرقية.
كما يُنتج تحت المهاد هرمون السوماتوستاتين، الذي يتمتع بتأثير عكسي على إنتاج الغدة النخامية للهرمون المحفز للدرقية، حيث يخفض أو يثبط إطلاقه.
تركيز هرمونات الدرقية (T3 وT4) في الدم ينظمه إطلاق الغدة النخامية للهرمون المحفز للدرقية؛ عندما تكون تركيزات T3 وT4 منخفضة، يزيد إنتاج الهرمون المحفز للدرقية، وبالمثل، عندما تكون تركيزات T3 وT4 مرتفعة، ينخفض إنتاج الهرمون المحفز للدرقية. يعتبر هذا مثالاً على حلقة الإرتجاع السلبي.[7] أي عدم ملاءمة للقيم المقاسة، على سبيل المثال الإنخفاض الطبيعي للهرمون المحفز للدرقية مع انخفاض طبيعي لـT4 قد يكون إشارة على مرض مركزي و a TSH to TRH pathology. الإرتداد العكسي لـ T3 (RT3) مع القيم المنخفضة-الطبيعية للهرمون المحفز للدرقية، T3، T4، يعتبر مؤشراً لمتلازمة مرض الدرقية السوية، والذي يتطلب أيضاً التحقق من الإصابة بالتهاب الغدة الدرقية المزمن (SAT) مع مخرجات الهرمونات subpotent. عدم وجود الأجسام المضادة لدى المرضى الذين يعانون من التهاب الغدة الدرقية ذاتية المناعة في الماضي قد يكون مريباً لتطوره إلى SAT حتى في وجود الهرمون المحفز للدرقية بنسب طبيعية نظراً لعدم وجود حالات تعافي معروفة من من المناعة الذاتية.
من أجل التفسير السريري لنتائج المختبر من المهم أن نعرف بأن الهرمون المحفز للدرقية يُطلق بطريقة نابضة[8][9][10] مما يؤدي إلى تأثير الإيقاع اليومي والموجات فوق الصوتية على تركيزاته في الدم.[11]
الوحدات الفرعية
الهرمون المحفز للدرقية هو پروتين سكري ويتألف من وحدتين فرعيتين، ألفا وبيتا.
- الوحدة الفرعية α (ألفا) ، على سبيل المثال وحيدة ألفا لهرمونات الپروتين السكري) وهو مطابق تقريباً موجهة الغدد التناسلية المشيمائية (hCG)، الهرمون المنشط للجسم الأصفر (LH)، والهرمون المنبه للجريب (FSH). يعتقد أن الوحدة الفرعية ألفا هي المنطقة المستجيبة المسؤولة عن تحفيز السيكليز أدينيلات (المساهم في توليد cAMP).[12] يوجد في سلسلة ألفا 92 تسلسل حمض أميني.
- الوحدة الفرعية بيتا β (TSHB) هي وحدة فرعية مميزة للهرمون المحفز للدرقية، وبالتالي تحدد تخصص مستقبله.[13] يوجد في السلسلة بيتا 118 تسلسل حمض أميني.
مستقبل الهرمون المحفز للدرقية
يوجد مستقبل الهرمون المحفز للدرقية بصفة أساسية على الخلايا الجريبية الدرقية.[14] تحفيز المستقبل يزيد من إنتاج وإمتصاص T3 وT4. يحدث هذا خلال عملية تحفيز من 6 خطوات في تخليق هرمون الدرقية: (1) زيادة تنظيم نشاط ناقل الصوديوم-اليود (NIS) على الغشاء basolateral الخلايا الجريبية، وبالتالي تزيد التركيزات الخلوية لليود (حبس الكربون). (2) تحفيز اليودنة في الثيروگلوبولين في التجويف الجريبي، پروتين طليعي لهرمون الدرقية. (3) تحفيز تصريف رواسب التايروسين الميود. يؤدي هذا إلى تشكل الثيروكسين (T4) وثلاثي الثيروكسين (T3) الذي يظل ملتصقاً بپروتين الثيروگلوبولين. (4) زيادة الإدخال الخلوي لپروتين الثيروگلوبولين الميودن عبر الغشاء القمي رجوعاً إلى الخلية الجرابية. (5) تحفيز التحلل الپروتيني للثيروگلوبولين الميودن لتشكيل ثيروكسين حر (T4) وثلاثي الثيروكسين (T3). (6) إفراز الثيروكسين (T4) وثلاثي الثيروكسين (T3) عبر الغشاء basolateral للخلايا الجريبية لدخول الدورة الدموية. يحدث هذا بواسطة آلية غير معروفة.[15]
تحفيز الأجسام المضادة لمستقبل الهرمون المحفز للدرقية المحاكي للهرمون المحفز للدرقية والإصابة بمرض گريڤز. بالإضافة إلى ذلك، تظهر موجهة الغدد التناسلية المشيمائية بعض التفاعل المتبادل لمستقبل الهرمون المحفز للدرقية، وبالتالي يمكن أن تحفز إنتاج هرمونات الغدة الدرقية. أثناء الحمل، التركيزات المرتفعة بشكل مستمر لموجهة الغدد التناسلية المشيمائية إلى قد تؤدي إلى حالة مؤقتة تسمى "فرط الدرقية الحملي".[16] يعتبر هذا أيضاً آلية أورام الأرومة الغاذية الحملية التي تزيد إنتاج هرمونات الدرقية.
فحص الهرمون المنبه للغدة الدرقية
لفهم طريقة عمل فحص الهرمون المنبه للغدة الدرقيةعلينا أن تعرف أولاً كيفية عمل الغدة الدرقية باختصار. تقوم الغدة الدرقية، المتواجدة في الجزء الأمامي من العنق، باٍنتاج الهرمونات T4 أو T3 التي تقوم بالاٍشراف على عملية الأيض في الجسم. كما أن هنالك نظام تغذية ارتجاعية دقيق جداً الذي يقوم بالاٍشراف على اٍفراز كمية دقيقة من هرمونات الغدة الدرقية، الكافية لحاجات الجسم الأيضية. تقوم الغدة النخامية باٍفراز الهرمون المحفز للدرقية الذي يعمل على تحفيز الغدة الدرقية لاٍفراز الهرمونات (T4) و(T3).
عندما يرتفع مستوى هذه الهرمونات فوق الحد اللازم ينخفض مستوى الهرمون المحفز للدرقية والعكس صحيح، حيث يرتفع مستوى الهرمون المحفز للدرقية عند اٍنخفاض مستوى الهرمونات (T4) و(T3). يفرز الوطاء الهرمون المطلق لموجهة الدرقية (TRH) الذي يقوم بالاٍشراف على اٍفراز الهرمون المحفز للدرقية من الغدة النخامية.
هنالك حالتين أساسيتين من العمل الغير السليم للغدة الدرقية:
- فرط الدرقية – والمسمى بالتسمم الدرقي (thyrotoxicosis)
- قصور الدرقية (hypothyroidism) – حيث لا تقوم الغدة باٍنتاج كميات كافية من الهرمونات.
الأدوية التي تؤثر على نتيجة الفحص
- الأدوية التي تقلل من مستوى الهرمون المحفز للدرقية: الأسپرين، الدوپامين، السترويدات القشرية.
- ألأدوية التي تزيد من مستوى الهرمون المحفز للدرقية: الليثيوم، يوديد الپوتاسيوم.
النتائج
| الفئة | النسبة الطبيعية |
|---|---|
| رجال | تختلف نتائج هذا الفحص من مختبر لآخر. حيث يجب النظر اٍلى نموذج المختبر من أجل معرفة مجال القيم السليمة الخاصة بالمختبر. |
| النساء | 35-5.5 ميلي وحدة دولية/لتر. |
| الأطفال | 35-5.5 ميلي وحدة دولية/لتر |
للحصول على نتيجة ذات معنى لفحص الهرمون المحفز للدرقية فاٍنه دائماً ما يتم القيام بفحص اٍضافي لمستوى الـ(T4) الحر (FT4) (Free T4).
- المستوى السليم: يشير المستوى السليم للهرمون المحفز للدرقية عادة اٍلى عدم وجود مشكلة في الغدة الدرقية. هنالك حالات نادرة جداً التي يظهر بها قصور الدرقية برغم وجود مستوى سليم للهرمون المحفز للدرقية، ولكن ليست هنالك حاجة بشكل عام للقيام بفحوصات اٍضافية اٍلا عند وجود اٍشتباه بمشكلة معينة.
- مستويات عالية: تشير المستويات العالية للهرمون المحفز للدرقية المصحوبة بمستويات منخفضة من الـ(FT4) اٍلى وجود قصور درقي النابع من خلل في الغدة الدرقية.
تشير المستويات العالية للهرمون المحفز للدرقية و(FT4) اٍلى وجود اٍفراز مفرط من الغدة النخامية، وخاصة عقب ورم حميد في الغدة النخامية. في هذه الحالة يمكن فحص وحيدات خاصة الوحدات الفرعية ألفا للهرمون المحفز للدرقية من أجل اٍقرار التشخيص.
- مستويات منخفضة: تشير المستويات المنخفضة من الهرمون المحفز للدرقية المصحوبة بمستويات عالية من (FT4) أو (FT3) اٍلى فرط الدرقية والتي يمكن أن تكون ناتجة عن اٍلتهاب الغدة الدرقية المزمن، تناول مفرط لليود أو الثيروكسين. عند مرضى گريڤز وتضخم الغدة الدرقية، تكون هنالك مستويات سليمة من(FT4) ومستويات عالية من (FT3) وهذا ما يسمى بالتسمم الدرقي. [17]
يمكن أن تظهر مستويات منخفضة للهرمون المحفز للدرقية مع مستويات سليمة من (FT4) أو (FT3) عند المرضى المصابون بقصور الدرقية وكذلك عند المرضى الذين يعانون من مرض خطير آخر غير متعلق بتاتا بالغدة الدرقية.
تشير المستويات المنخفضة للهرمون المحفز للدرقية و(FT3) اٍلى قصور الدرقية النابعة من خلل في عمل الغدة النخامية أو الوطاء. تظهر أحيانا قيم مشابهة لهذه الهرمونات عند المرضى الذي يعانون من مرض شديد آخر الغير متعلق بالغدة الدرقية.
تحذيرات
عامة
قد يحدث نزيف دموي تحت الجلد في موضع أخذ عينة الدم (يمكن وضع ثلج في حال حدوثه).
أثناء الحمل
يكون هرمون المحفز للدرقية مُثبطاً في الأسابيع الأولى للحمل (حتى الأسبوع ال 12).
أثناء الرضاعة
لا توجد مشاكل خاصة.
الأطفال والرضع
لا توجد مشاكل خاصة. يتم فحص مستوى الهرمون المحفز للدرقية بشكل روتيني عند جميع الأطفال فوراً بعد الولادة.
التطبيقات
التشخيص
قد تتباين المجالات المرجعية للهرمون المحفز للدرقية بشكل ضئيل، تبعاً لطريقة التحليل، ولا تساوي بالضرورة التشخيص القاطع لخلل الغدة الدرقية. في المملكة المتحدة، تشير القواعد الإرشادية الصادرة من قبل رابطة الكيمياء الحيوية السريرية إلى أن المجال المرجعي هو 0.4-4.0 mIU/mL.[18] وتقول الأكاديمية الوطنية للكيمياء الحيوية السريرية أن المجال المرجعي المتوقع للبالغين قد يقل إلى 0.4–2.5 µIU/mL، لأن الأبحاث أظهرت أن القياس الأولي لمستوى الهرمون المحفز للدرقية لدى البالغين يزيد في الـ20 عام [التالية]، خاصة إذا زادت الأجسام المضادة الدرقية"..[19]
تركيزات الهرمون المحفز للدرقية لدى الأطفال يكون أعلى بشكل طبيعي عنه لدى البالغين. عام 2002، أوصت الرابطة الوطنية للكيمياء الحيوية السريرية بأن الحدود المرجعية المرتبطة بالعمر تبدأ من 1.3 إلى 19 µIU/mL لدى الأطفال عند الميلاد، لتتراجع إلى 0.6–10 µIU/mL في الأسبوع الأول من العمر، 0.4–7.0 µIU/mL في عمر 14 شهر وتنخفض تدريجياً أثناء الطفولة والبلوغ حتى تصل لمستوياتها لدى البالغين، 0.3–3.0 µIU/mL.[20]
تشخيص مرض
قد تقاس تركيزات الهرمون المحفز للدرقية كجزء من اختبار وظيفة الدرقية لدى المرضى المشتبه بإصابتهم بارتفاع (فرط الغدة الدرقية) أو انخفاض (قصور الغدة الدرقية) هرمونات الدرقية. يعتمد تأويل النتائج على تركيزات الهرمون المحفز للدرقية وT4. في بعض الحالات قد يكون من المفيد أيضاً قياس T3.
| المصدر الباثولوجي | مستوى الهرمون المحفز للدرقية | مستوى هرمون الدرقية | الحالات المحفزة للمرض |
|---|---|---|---|
| الوطاء/النخامية | مرتفع | مرتفع | ورم الغدة النخامية الحميد (ورم غدي) أو مقاومة هرمون الدرقية |
| الوطاء/النخامية | منخفض | منخفض | قصور الدرقية الثانوي أو قصور الغدة الدرقية "المركزي" |
| فرط الدرقية | منخفض | مرتفع | فرط الدرقية الأولي على سبيل المثال مرض گريڤز |
| قصور الغدة الدرقية | مرتفع | منخفض | قصور الدرقية الخلقي، قصور الدرقية الأولي على سبيل المثال التهاب الدرقية المزمن |
الآن، يعتبر الهرمون المحفز للدرقية أيضاً أداة الفحص الموصى بها لمرض الغدة الدرقية. جعلت التطورات الحديثة في زيادة حساسية اختبار الهرمون المحفز للدرقية منها أداة فحص أفضل من T4 الحر.[3]
المتابعة
مجال الهدف العلاجي للهرمون المحفز للدرقية لدى المرضى ضمن المجالات العلاجية يتراوح بين 0.3 و3.0 μIU/mL.[21]
للمرضى المصابين بفرط إفراز هرمون الثيروكسين، يعتبر قياس الهرمون المحفز للدرقية وحده كافياً بشكل عام. زيادة الهرمون المحفز للدرقية فوق المجال الطبيعي يشير إلى وجوب إستبدال العلاج أو إلى كونه غير متوافقاً. ويشير الانخفاض الكبير في الهرمون المحفز للدرقية إلى الإفراج في العلاج. في كلا الحالتين، يلزم تغيير الجرعة. كذلك قد تعتبر القيم المنخفضة أو المنخفضة-الطبيعية إشارة لمرض في الغدة النخامية عند عدم استبدال الدواء.
بالنسبة لمرضى فرط الدرقية، عادة ما تراقب نسب الهرمون المحفز للدرقية وT4. وينبغي أيضاً أثناء الحمل، ملاحظة أن قياسات الهرمون المحفز للدرقية لا تعتبر دلالة جيدة على الارتباط الشهير لتوافر الهرمون الدرقي لدى الأم بالتطور الوراثي العصبي لدى الأبناء.[22]
تزداد مستويات الهرمون المحفز للدرقية بمرور العمر.[23]
صعوبات مع تفسير قياس الهرمون المحفز للدرقية
- الأجسام المضادة الغيرية (والتي تشمل الأجسام المضادة المؤنسنة المضاد للفئران (HAMA) وعامل الروماتويد (RF))، والذي يرتبط بشكل ضعيف مع الأجسام المضادة الحيوانية في الاختبار، مما يسبب نتيجة مرتفعة للهرمون المحفز للدرقية (أو منخفضة، الأقل شيوعاً) عن المستوى الحقيقي للهرمون المحفز للدرقية.[24][25] على الرغم من تصميم لوحات الفحص المعملية القياسية لإزالة المستويات المعتدلة من الأجسام المضادة المتغايرة، إلا أنها تفشل في إزالة مستويات الأجسام المضادة الأعلى. وجدت "د. بومان (من مايو كلينك) وزملائها أن 4.4% من مئات العينات التي اختبرتها كانت متأثرة بالأجسام المضادة الغيرية... السمة المميزة لهذه الحالة هي وجود تناقض بين قيمة الهرمون المحفز للدرقية وT4 الحر، والأكثر أهمية التناقض بين القيم المعملية وحالة المريض. يجب على علماء الغدد، على وجه الخصوص، التنبه لهذا."
- الهرمون المحفز للدرقية-الدقيق- ترتبط الأجسام المضادة الداخلية بالهرمون المحفز للدرقية مما يقلل من نشاطها، ومن ثم تحتاج الغدة النخامية لإنتاج المزيد من الهرمون المحفز للدرقية من أجل الحصول على المستوى الكامل من نشاط الهرمون المحفز للدرقية.[26]
- متزامرات الهرمون المحفز للدرقية - الاختلافات الطبيعية لجزيء الهرمون المحفز للدرقية، والي يتمتع بنشاط أقل، ومن ثم تحتاج الغدة النخامية لإنتاج المزيد من الهرمون المحفز للدرقية من أجل الحصول على المستوى الكامل من نشاط الهرمون المحفز للدرقية..[27][28]
العلاجية
الدواء التخليقي المسمى بألفا TSH المؤنسن المؤشب (rhTSHα أو اختصاراً rhTSH) أو ألفا ثيروتروپين (INN) تصنعه شركة جنزيزم تحت الاسم التجاري ثيروجين Thyrogen. يستخدم الثيروجين لمعالجة وظائف الغدد الصماء للخلايا المشتقة من الغدة الدرقية، كجزء من تشخيص وعلاج سرطان الغدة الدرقية.[29]
الهامش
- ^ أ ب Merck Manual of Diagnosis and Therapy, Thyroid gland disorders.
- ^ The American Heritage Dictionary of the English Language, Fourth Edition. Houghton Mifflin Company. 2006. ISBN 0-395-82517-2.
- ^ أ ب Sacher, Ronald; Richard A. McPherson (2000). Widmann's Clinical Interpretation of Laboratory Tests, 11th ed. F.A. Davis Company. ISBN 0-8036-0270-7.
{{cite book}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ Magner J (June 2014). "Historical note: many steps led to the 'discovery' of thyroid-stimulating hormone". European Thyroid Journal. 3 (2): 95–100. doi:10.1159/000360534. PMC 4109514. PMID 25114872.
- ^ T3 وT4 وTSH أبرزها هرمونات الغدة الدرقية، أي خلل في معدلها يؤدي إلى خلل في وظائف الجسم، مجلة المستشفى العربي
- ^ References موجود في مقال الصورة على:Commons:File:Thyroid system.png#References.
- ^ Estrada JM, Soldin D, Buckey TM, Burman KD, Soldin OP (Mar 2014). "Thyrotropin isoforms: implications for thyrotropin analysis and clinical practice". Thyroid. 24 (3): 411–23. doi:10.1089/thy.2013.0119. PMC 3949435. PMID 24073798.
- ^ Greenspan SL, Klibanski A, Schoenfeld D, Ridgway EC (Sep 1986). "Pulsatile secretion of thyrotropin in man". The Journal of Clinical Endocrinology and Metabolism. 63 (3): 661–8. doi:10.1210/jcem-63-3-661. PMID 3734036.
- ^ Brabant G, Prank K, Ranft U, Schuermeyer T, Wagner TO, Hauser H, Kummer B, Feistner H, Hesch RD, von zur Mühlen A (Feb 1990). "Physiological regulation of circadian and pulsatile thyrotropin secretion in normal man and woman". The Journal of Clinical Endocrinology and Metabolism. 70 (2): 403–9. doi:10.1210/jcem-70-2-403. PMID 2105332.
- ^ Samuels MH, Veldhuis JD, Henry P, Ridgway EC (Aug 1990). "Pathophysiology of pulsatile and copulsatile release of thyroid-stimulating hormone, luteinizing hormone, follicle-stimulating hormone, and alpha-subunit". The Journal of Clinical Endocrinology and Metabolism. 71 (2): 425–32. doi:10.1210/jcem-71-2-425. PMID 1696277.
- ^ Hoermann R, Midgley JE, Larisch R, Dietrich JW (20 November 2015). "Homeostatic Control of the Thyroid-Pituitary Axis: Perspectives for Diagnosis and Treatment". Frontiers in Endocrinology. 6: 177. doi:10.3389/fendo.2015.00177. PMC 4653296. PMID 26635726.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Lalli E, Sassone-Corsi P (Oct 1995). "Thyroid-stimulating hormone (TSH)-directed induction of the CREM gene in the thyroid gland participates in the long-term desensitization of the TSH receptor" (PDF). Proceedings of the National Academy of Sciences of the United States of America. 92 (21): 9633–7. doi:10.1073/pnas.92.21.9633. PMC 40856. PMID 7568187.
- ^ Porcellini A, Messina S, De Gregorio G, Feliciello A, Carlucci A, Barone M, Picascia A, De Blasi A, Avvedimento EV (Oct 2003). "The expression of the thyroid-stimulating hormone (TSH) receptor and the cAMP-dependent protein kinase RII beta regulatory subunit confers TSH-cAMP-dependent growth to mouse fibroblasts". The Journal of Biological Chemistry. 278 (42): 40621–30. doi:10.1074/jbc.M307501200. PMID 12902333.
- ^ Parmentier M, Libert F, Maenhaut C, Lefort A, Gérard C, Perret J, Van Sande J, Dumont JE, Vassart G (Dec 1989). "Molecular cloning of the thyrotropin receptor". Science. 246 (4937): 1620–2. doi:10.1126/science.2556796. PMID 2556796.
- ^ Boron, Walter; Boulpaed, Emile (2012). Medical Physiology (2nd ed.). Philadelphia: Elsevier Saunders. p. 1046. ISBN 978-1-4377-1753-2.
{{cite book}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ Fantz CR, Dagogo-Jack S, Ladenson JH, Gronowski AM (Dec 1999). "Thyroid function during pregnancy". Clinical Chemistry. 45 (12): 2250–8. PMID 10585360.
- ^ فحص الهرمون المنبه للغدة الدرقية (TSH)، وب طبيب
- ^ Use of thyroid function tests: guidelines development group (2008-06-01). "UK Guidelines for the Use of Thyroid Function Tests" (Web Page). Retrieved 2018-04-30.
- ^ Baloch Z, Carayon P, Conte-Devolx B, Demers LM, Feldt-Rasmussen U, Henry JF, LiVosli VA, Niccoli-Sire P, John R, Ruf J, Smyth PP, Spencer CA, Stockigt JR (Jan 2003). "Laboratory medicine practice guidelines. Laboratory support for the diagnosis and monitoring of thyroid disease". Thyroid. 13 (1): 3–126. doi:10.1089/105072503321086962. PMID 12625976.
- ^ Baskin HJ, Cobin RH, Duick DS, Gharib H, Guttler RB, Kaplan MM, Segal RL (2002). "American Association of Clinical Endocrinologists medical guidelines for clinical practice for the evaluation and treatment of hyperthyroidism and hypothyroidism" (PDF). Endocrine Practice. 8 (6): 457–69. PMID 15260011.
- ^ Baskin; et al. (2002). "AACE Medical Guidelines for Clinical Practice for Evaluation and Treatment of Hyperthyroidism and Hypothyroidism" (PDF). American Association of Clinical Endocrinologists. pp. 462, 465.
- ^ Korevaar TI, Muetzel R, Medici M, Chaker L, Jaddoe VW, de Rijke YB, Steegers EA, Visser TJ, White T, Tiemeier H, Peeters RP (Oct 2015). "Association of maternal thyroid function during early pregnancy with offspring IQ and brain morphology in childhood: a population-based prospective cohort study". The Lancet Diabetes & Endocrinology. 4: 35–43. doi:10.1016/S2213-8587(15)00327-7. PMID 26497402.
- ^ Surks MI, Hollowell JG (2007). "Age-specific distribution of serum thyrotropin and antithyroid antibodies in the US population: implications for the prevalence of subclinical hypothyroidism". The Journal of Clinical Endocrinology and Metabolism. 92 (12): 4575–82. doi:10.1210/jc.2007-1499. PMID 17911171.
- ^ Morton A (June 2014). "When lab tests lie ... heterophile antibodies". Australian Family Physician. 43 (6): 391–393. PMID 24897990.
- ^ Garcia-Gonzaleza E, Aramendia M, Alvarez-Ballano D, Trincado P, Rello L (April 2016). "Serum sample containing endogenous antibodies interfering with multiple hormone immunoassays. Laboratory strategies to detect interference". Practical Laboratory Medicine. 4 (1): 1–10. doi:10.1016/j.plabm.2015.11.001.
- ^ Hattori N, Ishihara T, Shimatsu A (Jan 2016). "Variability in the detection of macro TSH in different immunoassay systems". European Journal of Endocrinology. 174 (1): 9–15. doi:10.1530/EJE-15-0883. PMID 26438715.
- ^ Beck-Peccoz P, Persani L (Oct 1994). "Variable biological activity of thyroid-stimulating hormone". European Journal of Endocrinology. 131 (4): 331–40. doi:10.1530/eje.0.1310331. PMID 7921220.
- ^ Sergi I, Papandreou MJ, Medri G, Canonne C, Verrier B, Ronin C (Jun 1991). "Immunoreactive and bioactive isoforms of human thyrotropin". Endocrinology. 128 (6): 3259–68. doi:10.1210/endo-128-6-3259. PMID 2036989.
- ^ Duntas LH, Tsakalakos N, Grab-Duntas B, Kalarritou M, Papadodima E (2003). "The use of recombinant human thyrotropin (Thyrogen) in the diagnosis and treatment of thyroid cancer". Hormones. 2 (3): 169–74. doi:10.14310/horm.2002.1197. PMID 17003018.
وصلات خارجية
- CS1 errors: unsupported parameter
- CS1 maint: unflagged free DOI
- Protein pages needing a picture
- Genes on human chromosome 6
- Genes on human chromosome 1
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- Articles with hatnote templates targeting a nonexistent page
- پروتينات سكرية
- هرمونات پپتيدية
- هرمونات النخامية الأمامية
- هرمونات بشرية
- الغدة الدرقية
- هرمونات المحور الوطائي-النخامي-الدرقي