نقيلة

| النقيلة Metastasis | |
|---|---|
| الأسماء الأخرى | المرض النقيلي |
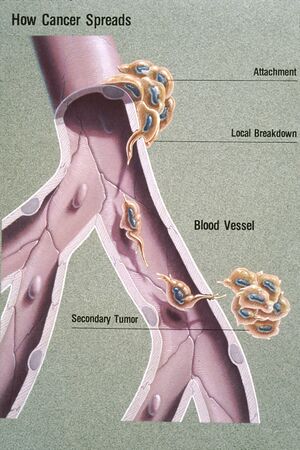 | |
| رسم يوضح الإنبثاث الدموي المنشأ. | |
| النطق |
|
| التخصص | علم الأورام |
النقيلة أو الانبثاث أو هجرة الخلايا السرطانية Metastasis، هي انتشار العامل الممرض من الموقع الأولي أو الابتدائي إلى موقع مختلف أو ثانوي في جسم العائل؛[1] عادة ما يستخدم المصطلح للإشارة إلى انبثاث الأورام السرطانية.[2] ومن ثم، يُطلق على المواقع الممرضة الجديدة، اسم النقائل.[3][4] وتتميز بصفة عامة ن الغزو السرطاني، الذي يعتبر امتداداً مباشراً وتداخلاً من قبل الخلايا السرطانية داخل الأنسجة المجاورة.[5]
يحدث السرطان بعد حدوث تغيراً وراثياً للخلايا لتستمر في الانقسام وإلى أجل غير مسمى. هذا الانقسام الغير منضبط عبر الانقسام الفتيلي ينتج تغايراً ورمياً أولياً. وفي النهاية فإن الخلايا التي تشكل الورم تخضع للتحول النسيجي، يليه خلل في التنسج ثم فقد التمايز الخلوي، مما ينتج عنه حدوث نمط ظاهري خبيث. تسمح هذه الخباثة بالانتشار داخل الدورة الدموية، ويعقبه غزو للموقع الثاني من أجل حدوث التسرطن.
تُعرف بعض الخلايا السرطانية بالخلايا الورمية المنتشرة التي لديها القدرة على اقتحام جدران الأوعية الدموية أو اللمفاوية، مما يمكنها من الانتشار عبر مجرى الدم لتصل إلى الأماكن والأنسجة الأخرى داخل الجسم.[6] تُعرف هذا العملية (على التوالي) باسم الانتشار الدموي أو اللمفاوي. بعد وصول الخلايا الورمية للاستقرار في موقع آخر بالجسم، تعيد اقتحام الجدران أو الأوعية للاستمرار في الانقسام، لتشكل في النهاية ورماً آخر يمكن التعرف عليه سريرياً.[citation needed] يُعرف هذا الورم الجديد بالورم النقيلي (أو الثانوي). الانبثاث هو أحد العلامات المميزة للأورام السرطانية، والتي تفرقها عن الأورام الحميدة.[7] يمكن لمعظم السرطانات الانتشار، على الرغم من حدوث ذلك بدرجات مختلفة. ويعتبر سرطان الخلايا القاعدية، من أقل السرطانات انتشاراً داخل الجسم..[7]
عند انبثاث الخلايا الورية، يُطلق على الورم الجديد اسم الورم الثانوي أو النقيلي، وتكون خلايا مشابهة لخلايا الورم الأولي.[8] يعني هذا أنه في حالة انبثاث سرطان الثدي إلى الرئتين، فإن الورم الثانوي يتألف من خلايا ثديية شاذة، وليست خلايا رئوية شاذة. في هذه الحالة يسمى الورم المتكون في الرئة سرطان الثدي النقيلي، وليس سرطان الرئة. الانبثاث هو عنصر رئيسي في أنظمة تحديد مراحل السرطان مثل نظام تصنيف TNM، حيث يرمز الحرف "M" إلى النقيلة أو الانبثاث. في تصنيف مراحل السرطان، يضع الانبثاث السرطان في المرحلة الرابعة. وفي هذه المرحلة تقل احتمالات العلاج الشافي بدرجة كبيرة، وفي حالة انتشار السرطان في عضو ما، عادة ما يتم إزالته بالكامل.
الأعراض والعلامات
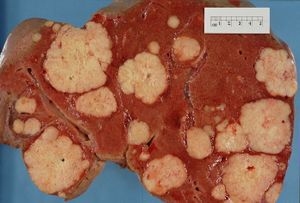
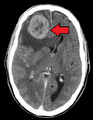
تختلف أعراض وعلامات النقائل باختلاف موقع الورم. في البداية، تُصاب الغدد الليمفاوية المجاورة في وقت مبكر. وأكثر المواقع عرضًة للانتشار من الأورام الخبيثة الصلبة[9] هي الرئتين، الكبد، الدماغ والعظام.
- في الغدد الليمفاوية، العَرَض الشائع هو اعتلال العقد اللمفية
- الرئتين: السعال، ونفث الدم وضيق التنفس[9]
- الكبد: تضخم الكبد، الغثيان، واليرقان
- العظام: آلام العظام[9]، وكسور في العظام المتضررة
- الدماغ: الأعراض العصبية مثل الصداع، التشنجات، والدوار
على الرغم من أن السرطان في مراحله المتقدمة قد يسبب الألم[9]، إلا أنه غالبًا ما لا يكون العرض الأول. وقد لا تظهر أي أعراض عند بعض المرضى. عندما يُصاب عضو ما بسرطان منتشر فإنه يبدأ في الانكماش حتى تنفجر الغدد الليمفاوية له، أوتتحلل.
الفسيولوجيا المرضية
العوامل المؤثرة
الانبثاث هو سلسلة معقدة من الخطوات التي تغادر فيها الخلايا السرطانية موقع الورم الأصلي وتهاجر إلى أجزاء أخرى من الجسم عبر مجرى الدم، والجهاز اللمفاوي، أو الانتشار المباشر. للقيام بذلك، تبتعد الخلايا الخبيثة عن الورم الرئيسي وترتبط ببروتينات وتكسرها مما يشكل المنطقة المحيطة خارج الخلية (ECM)، والتي تفصل بين الورم والأنسجة المجاورة. بواسطة تكسير هذه البروتينات، تصبح الخلايا السرطانية قادرة على اختراق المنطقة المحيطة بالخلية والهروب. لايكون موقع الانبثاث عشوائيًا دائمًا، فهناك أنواع مختلفة من السرطان تميل إلى الانتشار إلى أعضاء وأنسجة معينة بمعدل أعلى مما كان متوقعًا بالافتراضات الإحصائية وحدها[10]. على سبيل المثال؛ يميل سرطان الثدي إلى الانبثاث إلى العظام والرئتين. ويبدو أن هذه الخصوصية تتم بواسطة جزيئات إشارة قابلة للذوبان مثل الكيموكينات (منشطات كيميائية)[11]، وتحوُّل عامل النمو بيتا. يقاوم الجسم الورم الخبيث عن طريق مجموعة متنوعة من الآليات من خلال فئة من البروتينات المعروفة باسم مثبطات الانبثاث[12]، والتي يُعرف منها عشرات[13].
تقوم الخلايا البشرية بثلاثة أنواع من الحركة: الحركة الجماعية، حركة متوسطية، وحركة أميبية. تبدل الخلايا السرطانية في كثير من الأحيان بين أنواع مختلفة من الحركة. ويأمل بعض الباحثين في مجال السرطان لإيجاد العلاجات التي يمكن أن توقف أو على الأقل تبطيء انتشار السرطان عن طريق عرقلة أحد أو كلا النوعين من الحركة[14].
وقد اكتشف باحثو السرطان الدارسين للظروف اللازمة للانبثاث أن واحدًا من الأحداث الهامة المطلوبة هو نمو شبكة جديدة من الأوعية الدموية، تُدعى تولُّد أوعية الورم[15]. لذا فقد وُجد أن مثبطات تكوُّن الأوعية الدموية تمنع نمو الانبثاث.
هناك عدة أنواع مختلفة من الخلايا حاسمة لنمو الورم. على وجه الخصوص، ثبت أن الخلايا الأولية البطانية لها تأثير قوي على نمو الأوعية الدموية المصابة. ومن هذه النتيجة تثبت أهمية الخلايا البطانية الأولية [16][17] في توليد الأوعية الدموية للسرطان والانبثاث. علاوة على ذلك، يؤدي اجتثاث الخلايا البطانية الأولية من نخاع العظام إلى انخفاض كبير في نمو الورم وتكوُّن الأوعية الدموية. لذلك، فإن الخلايا البطانية الأولية مهمة جدًا في بيولوجيا الورم وهي أحد الأهداف العلاجية الجديدة حاليًا[18].
مسارات الانبثاث
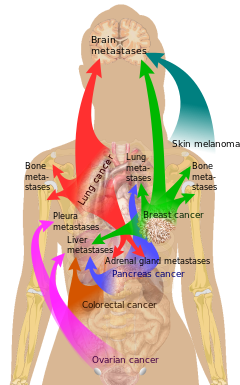
الانتقال الجوفي
يمكن أن يحدث انتشار الورم الخبيث في تجاويف الجسم عن طريق اختراق التجاويف مثل التجويف البريتوني، الجنبي، التاموري، أو تحت العنكبوتية. على سبيل المثال، يمكن أن تنتشر أورام المبيض عبر التجويف البريتوني لتصل إلى الكبد.
الاتنشار اللمفاوي
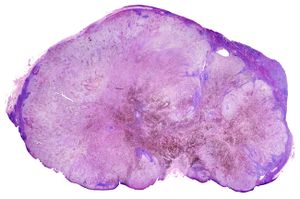
يسمح الانتشار اللمفاوي بنقل الخلايا السرطانية إلى الغدد الليمفاوية، وبالتالي، إلى أجزاء أخرى من الجسم. وهذا هو الطريق الأكثر شيوعًا لانبثاث الأورام الخبيثة. في المقابل، من غير المألوف للساركوما أن تنتشر عبر هذا الطريق. ومن الجدير بالذكر أن الجهاز الليمفاوي يصب في نهاية المطاف في الجهاز الوريدي عن طريق الوريد المفرد، وبالتالي يمكن لهذه الخلايا المنبثة أن تنتشر عن طريق الدم.
الانتشار الدموي
هذا هو الطريق النموذجي لانبثاث الساركوما، وهو أيضًا الطريق المفضل لأنواع معينة من السرطان، مثل تلك التي تنشأ في الكلى (سرطان الخلايا الكلوية). تُصاب الأوردة أكثر في كثير من الأحيان من الشرايين بسبب رقة جدرانها، كما يميل الانبثاث إلى اتباع نمط التدفق الوريدي.
الانغراس
قد تنتشر الخلايا السرطانية إلى الغدد الليمفاوية (العقد الليمفاوية للمنطقة المصابة) بالقرب من الورم الرئيسي. وهذا ما يسمى التورط العقدي. "العقد الإيجابية" هو المصطلح الذي يمكن أن يستعمله الأطباء المتخصصين لوصف حالة المريض، وهذا يعني أن العقد اللمفاوية للمريض بالقرب من الورم الرئيسي أصبحت إيجابية للورم الخبيث. من الممارسات الطبية الشائعة للاختبار أخذ خزعة من اثنين على الأقل من العقد الليمفاوية بالقرب من موقع الورم أثناء العملية الجراحية من أجل الفحص أو إزالة الورم.
لا يعد انتشار السرطان إلى الغدد الليمفاوية القريبة من الورم الرئيسي انبثاث، على الرغم من أنه علامة سيئة في تقدم المرض. النقل عن طريق الأوعية اللمفاوية هو الطريق الأكثر شيوعًا للانتشار الأوّلي للسرطانات.
استهداف الأعضاء
هناك ميل لبعض الأورام للانتشار في أعضاء معينة. وقد ناقش ستيفن باجيت هذا الأمر لأول مرة تحت مُسمّى نظرية "البذور والتربة" منذ أكثر من قرن، في عام 1889. على سبيل المثال، عادةً ينتشر سرطان البروستاتا للعظام. بطريقة مماثلة، يميل سرطان القولون للانتشار إلى الكبد. وفي كثير من الأحيان ينتشر سرطان المعدة إلى المبيض في النساء، ومن ثَمّ يُدعى ورم كروكنبرگ.
ِوفقًا لنظرية "البذور والتربة"، فمن الصعب على الخلايا السرطانية البقاء خارج منطقة الورم الأصلية، لذلك من أجل الانتشار يجب أن تجد مكانًا لها ذو خصائص مماثلة[20]. على سبيل المثال، تنتشر الخلايا السرطانية بالثدي، والتي تجمع أيونات الكالسيوم من حليب الثدي، إلى أنسجة العظام، حيث يمكن جمع أيونات الكالسيوم من العظام. وكذلك ينتشر سرطان الجلد الخبيث إلى المخ، ربما لأن الأنسجة العصبية والخلايا الصباغية تنشآن من نفس خط الخلية في الجنين[21].
في عام 1928، تحدى جيمس يوينگ نظرية "البذور والتربة"، واقترح أن انتشار الورم الخبيث يحدث بمحض الطرق التشريحية والميكانيكية. وقد استخدُمت هذه الفرضية مؤخرًا للإشارة إلى عدة فرضيات حول دورة حياة الخلايا السرطانية (CTCs) والافتراض بأن أنماط الانتشار يمكن أن تُفهم على نحو أفضل من خلال نظرية "التصفية والتدفُّق"[22].
الانبثاث والسرطان الأولي
هناك نظرية بأن الانبثاث يتزامن دائمًا مع السرطان الأوّلي، ولكن أكثر من 10٪ من المرضى في وحدات الأورام سيكون لديهم انبثاث دون الكشف عن الورم الرئيسي. في هذه الحالات، يشير الأطباء إلى الورم الرئيسي باسم "المجهول" أو "الغامض"، ويكون المريض مُصابًا بسرطان مجهول المنشأ (CUP) أو الأورام الأوّلية غير المعروفة (UPT)[23]. تشير التقديرات إلى أن 3٪ من جميع حالات السرطان ذات منشأ غير معروف[24]. وقد أظهرت الدراسات أنه إذا لم يكشف الاستجواب البسيط عن مصدر السرطان (سعال دموي "ربما الرئة"، والتبول الدموي "ربما المثانة")، فإن التصوير المعقد قد لا يكشفه أيضًا.[24] في بعض هذه الحالات قد يظهر الورم الرئيسي في وقت لاحق. سمح استخدام الكيمياء النسيجية المناعية للأطباء بإعطاء هوية لكثير من هذه النقائل. ومع ذلك، نادرًا ما يوضح تصوير المنطقة المشار إليها الورم الرئيسي. في حالات نادرة (على سبيل المثال، سرطان الجلد)، لم يتم العثور على الورم الرئيسي، حتى عند تشريح الجثة. وبالتالي فإنه يُعتقد أن بعض الأورام الأوّلية يمكن أن تتراجع كليًا، ولكن يستمر الانبثاث.
المواقع الأوّلية الأكثر شيوعًا
- الرئة
- الثدي
- الجلد: الورم الميلانيني (أورام الجلد الأخرى نادرا ما تنتقل)
- القولون
- الكلى
- البروستاتا
- البنكرياس
- الكبد
- عنق الرحم[25][26]
التشخيص
تشبه الخلايا في الورم النقيلي تلك الموجودة في الورم الرئيسي. فبمجرد فحص الأنسجة السرطانية تحت المجهر لتحديد نوع الخلية، يمكن للطبيب عادة أن يقول ما إذا كان هذا النوع من الخلايا يوجد طبيعيًا في جزء الجسم الذي تم أخذ عينة الأنسجة منه.
على سبيل المثال، تملك خلايا سرطان الثدي الشكل نفسه سواء وُجدت في الثدي أو انتشرت إلى أجزاء أخرى من الجسم. لذا، إذا أُخذت عينة من ورم في الرئة يحتوي على خلايا تشبه خلايا الثدي، يحدد الطبيب أن الورم في الرئة هو ورم ثانوي. ومع ذلك، فإن تحديد الورم الرئيسي يمكن أن يكون صعبًا جدًا في كثير من الأحيان ، ويمكن أن يحتاج اختصاصي الباثولوجيا لاستخدام العديد من التقنيات المساعدة، مثل الكيمياء النسيجية المناعية، اختبار FISH، وغيرها. وعلى الرغم من استخدام هذه التقنيات، يظل الورم الرئيسي مجهولًا في بعض الحالات.
يمكن الكشف عن السرطان النقيلي في نفس وقت الورم الرئيسي، أو خلال أشهر أو سنوات تالية. وعندما يُعثَر على ورم ثانوي في مريض عُولِج من السرطان من قبل، فإنه كثيرًا ما يكون انبثاثًا أكثر منه ورم أوّلي آخر.
كان يُعتقد في السابق أن معظم الخلايا السرطانية لديها إمكانات انتقال منخفضة وأن هناك خلايا نادرة تنمّي القدرة على الانتقال من خلال حدوث طفرات جسدية[27]. ووِفقًا لهذه النظرية، يكون تشخيص السرطانات النقيلية ممكنًا فقط بعد حدوث الانبثاث[28].
لم تثبُت نظرية الطفرة الجسدية لحدوث الانبثاث في السرطانات البشرية. بدلًا من ذلك، يبدو أن الحالة الوراثية للورم الرئيسي تعكس قدرة السرطان على الانتشار. حدّد البحث بمقارنة التعبير الجيني بين السرطانات الغدّية الأولية والمنتشرة، مجموعة فرعية من الجينات والتي يمكن أن تميز الأورام الأولية من الأورام النقيلية، يُطلق عليها اسم "الدليل النقيلي." لُوحظ أيضًا تعبير هذه الجينات المرتبط بالانبثاث في بعض الأورام الأولية، مشيرًا إلى إمكانية تحديد الخلايا التي لديها قدرة على الانبثاث في وقت واحد مع تشخيص الورم الرئيسي[29].
ارتبط هذا الدليل النقيلي بسوء التشخيص، وكان للانبثاث من سرطان الثدي، الورم الأرومي النخاعي وسرطان البروستاتا أنماط تعبير مماثلة من هذه الجينات المرتبطة بالانبثاث.
أعطى تحديد هذا الدليل النقيلي الأمل في تحسين تشخيص السرطانات المرتبطة بالانبثاث، وأيضًا تثبيط انتقال السرطانات.
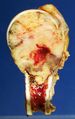
-
قطاع من عظمة العضد يظهر طوليًا، موضحًا انبثاث سرطاني كبير (الورم الأبيض بين رأس وجسم العظمة)
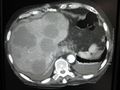
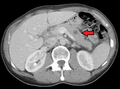
-
صورة أشعة مقطعية لانبثاثات متعددة بالكبد
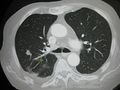
-
صورة أشعة مقطعية لانبثاث في الرئة
-
انبثاث ثبُت عن طريق خزعة من الكبد (الورم (سرطانة غدية)- ثلثي الصورة بالأسفل). صبغة الهيماتوكسيلين والإيوسين
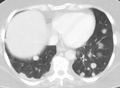
-
سرطان منتشر في الرئتين
العلاج
يتم تحديد العلاج ومدى البقاء على قيد الحياة إلى حد كبير من خلال ما إذا كان السرطان لا يزال في موقعه الأصلي أو انتشر إلى أماكن أخرى في الجسم. فإذا انتقل السرطان إلى أنسجة أو أعضاء أخرى، عادةً ما يزيد بشكل كبير احتمال موت المريض. يمكن لبعض أنواع السرطان مثل سرطان الدم، أو الأورام الخبيثة في المخ أن تؤدي إلى الوفاة دون أن تننشر.
بمجرد انتشار السرطان فإنه قد لا يزال علاجه ممكنًا بالجراحة الإشعاعية، العلاج الكيميائي، العلاج الإشعاعي، العلاج البيولوجي، العلاج الهرموني، والجراحة، أو مزيج من هذه التدخلات ( "العلاج متعدد الوسائط"). يتعمد اختيار العلاج على عدد كبير من العوامل، بما في ذلك نوع السرطان الأولي، حجم وموقع الانبثاث، عُمْر المريض وصحته العامة، وأنواع العلاجات المُستخدمة سابقًا. غالبًا ما يكون علاج المرضى الذين شُخِّصت إصابتهم بسرطانات مجهولة المنشأ ممكنًا حتى دون تحديد موقع الورم الرئيسي.
نادرًا ما تتمكن العلاجات الحالية من علاج السرطان المنتشر لمواقع عديدة، على الرغم من إمكانية علاج بعض الأورام مثل سرطان الخصية وسرطان الغدة الدرقية.
الأبحاث
على الرغم من القبول على نطاق واسع بفكرة أن يكون الانبثاث نتيجة لهجرة الخلايا السرطانية، إلا أن هناك فرضية تقول أن بعض أنواع الانبثاث هي نتيجة العمليات الالتهابية من الخلايا المناعية غير الطبيعية[30]. وأيضًا يشير وجود السرطان المنتشر في حالة عدم وجود الأورام الأولية أن الانبثاث لا يحدث دائمًا من هجرة الخلايا الخبيثة من الأورام الأولية[31].
التاريخ
في مارس 2014، اكتشف الباحثون أقدم مثال كامل للإنسان المُصاب بالسرطان النقيلي. وُجدت الأورام في هيكل عظمي يبلغ من العمر 3000 سنة، عُثِر عليه في عام 2013 في مقبرة في السودان يعود تاريخها إلى 1200 قبل الميلاد. تم تحليل الهيكل العظمي باستخدام التصوير الشعاعي والمجهر الإلكتروني. ونُشرت هذه النتائج في صحيفة المكتبة العامة للعلوم[32][33][34].
التسمية
الانبثاث Metastasis هي كلمة يونانية تعني "النزوح"، مُكوَّنة من μετά، "مُجاوِر"، وστάσις، "وَضْع".
انظر أيضاً
- تأثير مباعد
- نقيلة دماغية
- متلازمة براون-سيكوار
- هجرة الخلايا الجماعية
- Contact normalization
- Disseminated disease
- أنماط الفئران لنقيلة سرطان الثدي
- تصوير مقطعي بابتعاث البوزيترونات (PET)
المصادر
- ^ "Metastasis", Merriam–Webster online, accessed 20 Aug 2017.
- ^ "What is Metastasis?". Cancer.Net. 2 February 2016.
- ^ Klein CA (September 2008). "Cancer. The metastasis cascade". Science. 321 (5897): 1785–7. doi:10.1126/science.1164853. PMID 18818347.
- ^ Chiang AC, Massagué J (December 2008). "Molecular basis of metastasis". The New England Journal of Medicine. 359 (26): 2814–23. doi:10.1056/NEJMra0805239. PMC 4189180. PMID 19109576.
- ^ "Invasion and metastasis". Cancer Australia. 2014-12-16. Retrieved 2018-10-26.
- ^ Maheswaran S, Haber DA (2010-02-01). "Circulating tumor cells: a window into cancer biology and metastasis". Current Opinion in Genetics & Development. 20 (1): 96–99. doi:10.1016/j.gde.2009.12.002. ISSN 0959-437X. PMC 2846729. PMID 20071161.
- ^ أ ب Kumar V, Abbas AK, Fausto N, Robbins SL, Cotran RS (2005). Robbins and Cotran pathologic basis of disease (7th ed.). Philadelphia: Elsevier Saunders. ISBN 978-0-7216-0187-8.
{{cite book}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ "O que é a metástase?". Dr. Felipe Ades MD PhD - Oncologista (in البرتغالية البرازيلية). 2018-07-24. Retrieved 2018-10-23.
- ^ أ ب ت ث National Cancer Institute: Metastatic Cancer: Questions and Answers. Retrieved on 2008-11-01 Archived 2015-02-26 at the Wayback Machine
- ^ Don X. Nguyen and Joan Massagué, Genetic determinants of cancer metastasis, Nature, 2007. http://www.nature.com/nrg/journal/v8/n5/pdf/nrg2101.pdf
- ^ Zlotnik A., Burkhardt A. M., Homey B., Homeostatic chemokine receptors and organ-specific metastasis, Nature reviews, 2007
- ^ Yvette Drabsch, Peter ten Dijke, TGF-β Signaling in Breast Cancer Cell Invasion and Bone Metastasis, J Mammary Gland Biol Neoplasia (2011) 16:97–108
- ^ Yoshida BA, Sokoloff MM, Welch DR, Rinker-Schaeffer CW. J Natl Cancer Inst. (21). doi:10.1093/jnci/92.21.1717. PMID 11058615.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ^ Matteo Parri, Paola Chiarugi. "Rac and Rho GTPases in cancer cell motility control" 2010 Archived 2015-07-24 at the Wayback Machine
- ^ Weidner N, Semple JP, Welch WR, Folkman J. N Engl J Med. (1). doi:10.1056/NEJM199101033240101. PMID 1701519.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ^ Science (5860). Bibcode:2008Sci...319..195G. doi:10.1126/science.1150224. PMID 18187653.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير5=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول5=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help) - ^ Genes & Development (12). doi:10.1101/gad.436307. PMC 1891431. PMID 17575055 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1891431.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير5=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول5=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help) - ^ Cancer Research (18). doi:10.1158/0008-5472.CAN-10-1142. PMC 3058751. PMID 20807818 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3058751.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مؤلف1=ignored (help); Unknown parameter|مؤلف2=ignored (help) - ^ List of included entries and references is found on main image page in Commons: Commons:File:Metastasis sites for common cancers.svg#Summary
- ^ Cancer Metast Rev. 1 (1). doi:10.1007/BF00049477 – via link.springer.com.
{{cite journal}}: Cite has empty unknown parameter:|الناشر=(help); Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help); Unknown parameter|المسار=ignored (help) - ^ Robert Weinberg, The Biology of Cancer, cited in Basics: A mutinous group of cells on a greedy, destructive task, by Natalie Angier, New York Times, 3 April 2007 Archived 2018-01-16 at the Wayback Machine
- ^
Nature Reviews Cancer. 12 (7). doi:10.1038/nrc3287. PMID 22912952.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|التاريخ=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help); Unknown parameter|المؤلف2=ignored (help); Unknown parameter|المؤلف3=ignored (help) - ^ J Natl Compr Canc Netw. 9 (12). PMID 22157556.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|السنة=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help); Unknown parameter|المؤلف=ignored (help) - ^ أ ب Briasoulis E, Pavlidis N. Oncologist (3). PMID 10388044.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help); Unknown parameter|مسار=ignored (help) - ^ Metastasis.
{{cite book}}: Cite has empty unknown parameters:|lay-date=,|subscription=,|nopp=,|last-author-amp=,|name-list-format=,|lay-source=,|registration=, and|lay-summary=(help) - ^
{{cite web}}: Empty citation (help) - ^ Poste G, Fidler IJ. Nature. 283 (5743). Bibcode:1980Natur.283..139P. doi:10.1038/283139a0. PMID 6985715.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|التاريخ=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help) - ^ Ramaswamy S, Ross KN, Lander ES, Golub TR. Nature Genetics. 33 (1). doi:10.1038/ng1060. PMID 12469122.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|التاريخ=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help) - ^ Nature. 415 (6871). doi:10.1038/415530a. PMID 11823860.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|displayauthors=ignored (|display-authors=suggested) (help); Unknown parameter|التاريخ=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help); Unknown parameter|المؤلف1=ignored (help); Unknown parameter|المؤلف2=ignored (help); Unknown parameter|المؤلف3=ignored (help) - ^ F1000Research. 5. doi:10.12688/f1000research.8055.1. PMC 4847566. PMID 27158448 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4847566.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|التاريخ=ignored (help); Unknown parameter|الصفحات=ignored (help); Unknown parameter|العنوان=ignored (help); Unknown parameter|المسار=ignored (help)CS1 maint: unflagged free DOI (link) - ^ Oncoscience (5). doi:10.18632/oncoscience.159. ISSN 2331-4737. PMC 4468332. PMID 26097879 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4468332.
{{cite journal}}: Missing or empty|title=(help); Unknown parameter|الأخير=ignored (help); Unknown parameter|الأول=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|تاريخ=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help) - ^ Reuters.
- ^ BBC.
- ^ International Business Times.
وصلات خارجية
| Classification | |
|---|---|
| External resources |
Medical information about metastatic cancer
- CS1 errors: unsupported parameter
- CS1 البرتغالية البرازيلية-language sources (pt-br)
- CS1 errors: missing title
- CS1 errors: bare URL
- CS1 errors: empty citation
- CS1 maint: unflagged free DOI
- الصفحات بخصائص غير محلولة
- Short description is different from Wikidata
- Articles with unsourced statements from March 2017
- علم أمراض السرطان
- علم الأورام