لاميڤودين
 | |
| البيانات السريرية | |
|---|---|
| أسماء أخرى | L-2',3'-dideoxy-3'-thiacytidine |
| فئة السلامة أثناء الحمل |
|
| مسارات الدواء | Oral |
| رمز ATC | |
| الحالة القانونية | |
| الحالة القانونية | |
| بيانات الحركية الدوائية | |
| التوافر الحيوي | 86% |
| ارتباط الپروتين | Less than 36% |
| Elimination half-life | 5 to 7 hours |
| الإخراج | Renal (circa 70%) |
| المعرفات | |
| |
| رقم CAS | |
| PubChem CID | |
| DrugBank | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.132.250 |
| Chemical and physical data | |
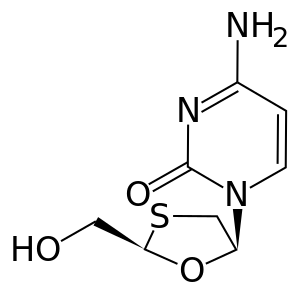
| التركيب | C8H11N3O3S |
| الكتلة المولية | 229.26 g/mol |
| 3D model (JSmol) | |
| |
لاميفودين
Lamivudine (2',3'-dideoxy-3'-thiacytidine , يعرف ب 3TC) وهو فعالnucleoside analog reverse transcriptase inhibitor (nRTI).
و يسوق بواسطة GlaxoSmithKline بالأسماء Zeffix, Heptovir, Epivir, و Epivir-HBV.
Lamivudine أستعمل لعلاج hepatitis B المزمن بجرعة ضئيلة لعلاج HIV. و هو يحسن seroconversion of e-antigen positive hepatitis B و يحسن أيضا histology staging للكبد. الإستعمال المستمر لل lamivudine يؤدى لسوء الحظ الى بروز فصيل مقاوم من hepatitis B virus (YMDD) mutant. و بالرغم من ذلك , فان lamivudine مازال يستعمل على نطاق واسع, نظرا لأنه يتحمل جيدا من قبل المرضي.
التاريخ
Lamivudine أبتكر بواسطةBernard Belleau عندما كان يعمل لدىMcGill University and Nghe Nguyen-Ga at the Montreal-based IAF BioChem International, Inc. laboratories in 1989. وقد طور أول الأمر كعقار مضاد للفيروسات ,و أكتشفت فعالية العقار لعلاج HIV بمزجه مع AZT بواسطةYung-Chi (Tommy) ChengفىYale University. و رخص أخيرا الى the British pharmaceutical company Glaxo بعد إستقطاع نسبة 14% للملكية.
Lamivudine قد أجيز بواسطة هيئة الأغذية و الأدوية الفيدرالية (FDA) في 17 نوفمبر 1995 للإستعمال مع zidovudine (AZT) و مرة أخرى2002 كعقار ذو جرعة وحيدة. وهو العقار الخامس المضاد للفيروسات بالأسواق, و كان آخر NRTI لمدة ثلاثة سنوات بينما تحولت عملية إقرار الدواء إلى protease inhibitors. تبعا ل التقرير السنوى للمصنعين عام 2004 , فإن الترخيص سيصبح منتهيا في الولايات المتحدة في 2010, بينما في أوروبا عام 2011 .
نظرية العمل
Lamivudine هوanalogue of cytidine. إنه يستطيع تثبيط كلا النوعين الأنواع (1 و 2) من HIV reverse transcriptase وأيضا the reverse transcriptase of hepatitis B. وهو يحتاج الى تجرى له عملية الفسفرة phosphorylated الىtriphosphate form قبل أن يصبح فعالا. 3TC-triphosphate أيضا يثبط الخلوى DNA polymerase.
Lamivudine يستعمل عن طريق الفم, ويمتص سريعا مع توافر حيوى 80%.بعض الأبحاث تقترح أن lamivudine يخترقblood-brain barrier. Lamivudine ويعطى بالإشتراك مع zidovudine, الذى يعد هكذا شديد التجانس it is highly synergistic. Lamivudine علاج يظهر zidovudine حساسية للفصائل السابقة المقاومة للفيروسHIV . mutagenicity tests show that lamivudine should not show mutagenic activity in therapeutic doses.
Physical Interaction with Tenofovir DF
Lamivudine shows brownish coloration with tenofovir disoproxil fumarate, reason behind this is still unknown.
المقاومة
- See also: resistance mutation
In HIV, high level resistance is associated with the M184V/I mutation in the reverse transcriptase gene. GlaxoSmithKline claimed that the M184V mutation reduces "viral fitness", because of the finding that continued lamivudine treatment causes the HIV viral load to rebound but at a much lower level, and that withdrawal of lamivudine results in a higher viral load rebound with rapid loss of the M184V mutation; GSK therefore argued that there may be benefit in continuing lamivudine treatment even in the presence of high level resistance, because the resistant virus is "less fit". The COLATE study has suggested that there is no benefit to continuing lamivudine treatment in patients with lamivudine resistance.[1] A better explanation of the data is that lamivudine continues to have a partial anti-viral effect even in the presence of the M184V mutation.
In hepatitis B, lamivudine resistance was first described in the YMDD locus of the HBV reverse transcriptase gene. The HBV reverse transcriptase gene is 344 amino acids long and occupies codons 349 to 692 on the viral genome. The most commonly encountered resistance mutations are M204V/I/S. Other resistance mutations are L80V/I, V173L and L180M.[2]
الجرعات
For adults with HIV (or children over 12), the dose is 300mg once daily, or 150mg twice a day. Lamivudine is never used on its own in the treatment of HIV.
For the treatment of adults with hepatitis B, the dose is 100mg once daily. If co-infected with HIV, then the dose is as for HIV.
For a child 3 months to 12 years old, about 1.4-2 mg per lb. of body weight twice a day, no more than 150 mg per dose.
الجرعات الزائدة
Little is known about the effects of overdosage with lamivudine.
الصور التجارية

- Epivir 150 mg or 300 mg tablets (GlaxoSmithKline; US and UK) for the treatment of HIV;
- Epivir-HBV 100 mg tablets (GlaxoSmithKline; US only) for the treatment of hepatitis B;
- Zeffix 100 mg tablets (GlaxoSmithKline; UK only) for the treatment of hepatitis B.
Lamivudine is also available in fixed combinations with other HIV drugs:
- Combivir (with zidovudine);
- Epzicom/Kivexa (with abacavir);
- Trizivir (with zidovudine and abacavir).
المراجع
- ^ Fox Z, Dragsted UB, Gerstoft J; et al. (2006). "A randomized trial to evaluate continuation versus discontinuation of lamivudine in individuals failing a lamivudine-containing regimen: The COLATE trial". Antiviral Therapy. 11: 761–70. PMID 17310820.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ Koziel MJ, Peters MG (2007). "Viral hepatitis in HIV infection". N Engl J Med. 356 (14): 1445–54. doi:10.1056/NEJMra065142.
الروابط الخارجية
- Epivir (manufacturer's website)
- Epivir-HBV (manufacturer's website)
- Epivir drug label/data at DailyMed from U.S. National Library of Medicine, National Institutes of Health.
- Epivir-HBV drug label/data at DailyMed from U.S. National Library of Medicine, National Institutes of Health.
- ECHA InfoCard ID from Wikidata
- Infobox-drug molecular-weight unexpected-character
- Pages using infobox drug with unknown parameters
- Articles without EBI source
- Chemical pages without ChemSpiderID
- Articles without KEGG source
- Articles without InChI source
- Articles without UNII source
- Articles containing unverified chemical infoboxes
- مثبطات ترانسكريپتاز العكسي المضاهية للنيكليوسيد
- الأدوية الأساسية حسب منظمة الصحة العالمية