ثلاثي أكسيد الزرنيخ
(تم التحويل من Arsenic trioxide)
ثلاثي أكسيد الزرنيخ Arsenic trioxide هو مركب كيميائي له الصيغة As2O3 ، ويكون على شكل بلورات بيضاء. وهذا الأكسيد الهام تجارياً للزرنيخ هو السابق الرئيسي لمنتجات الزرنيخ الأخرى، بما فيها مركبات الزرنيخ العضوية. ويـُنتج منه نحو 50,000 طن سنوياً.[3] والكثير من استخداماته هي موضع جدل بسبب السمية العالية لمركبات الزرنيخ.

| |
| |
| الأسماء | |
|---|---|
| أسماء أخرى
Arsenic(III) oxide,
Arsenic sesquioxide, Arsenicum album, Arseneous oxide, Arseneous anhydride, White arsenic[1] | |
| Identifiers | |
| رقم CAS | |
3D model (JSmol)
|
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.014.075 |
| رقم EC |
|
PubChem CID
|
|
| رقم RTECS |
|
CompTox Dashboard (EPA)
|
|
| InChI | InChI={{{value}}} |
| SMILES | |
| الخصائص | |
| الصيغة الجزيئية | As2O3 |
| كتلة مولية | 197.841 g/mol |
| المظهر | White solid |
| الكثافة | 3.74 g/cm3 |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 2 g/100 ml (25°C) see text |
| قابلية الذوبان | soluble in dilute acids and alkalies, practically insoluble in organic solvents [2] |
| الحموضة (pKa) | 9.2 |
| البنية | |
| البنية البلورية | cubic (α)<180°C monoclinic (β) >180°C |
| الشكل الجزيئي | See Text |
| Dipole moment | Zero |
| الكيمياء الحرارية | |
| الإنتالپية المعيارية للتشكل ΔfH |
−657.4 kJ/mol |
| Standard molar entropy S |
? J.K–1.mol–1 |
| فارماكولوجيا | |
| رباط البروتينات | 75% bound |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
Very toxic (T+) Carc. Cat. 1 Dangerous for the environment (N) |
| توصيف المخاطر | R45, R28, R34, R50/53 |
| تحذيرات وقائية | S53, S45, S60, S61 |
| NFPA 704 (معيـَّن النار) | |
| الجرعة أو التركيز القاتل (LD, LC): | |
LD50 (الجرعة الوسطى)
|
14.6 mg/kg (rat, oral) |
| مركبات ذا علاقة | |
أنيونات أخرى
|
Arsenic trisulfide |
كاتيونات أخرى
|
Phosphorus trioxide Antimony trioxide |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
- ينحل ثالث أكسيد الزرنيخ بالماء والمحلات الأخرى بصعوبة، لكنه ينحل في الأحماض والقلويات مشكلاً الأملاح الموافقة حسب المعادلات:
- As2O3 + 6NaOH → 2Na3AsO3 + 3H2O
- As2O3 + 6HCl → 2AsCl3 + 3H2O
- يوجد ثالث أكسيد الزرنيخ بشكلين حسب البنية البلورية له، إحداهما مكعبة وهي ثابتة عند درجات الحرارة العادية، وأخرى أحادية الميل تكون ثابتة عند درجات حرارة فوق 221°س.
التحضير
- يوجد أكسيد الزرنيخ الثلاثي في الطبيعة.
- يحضر مخبرياً إما من حرق فلز الزرنيخ بالهواء حسب المعادلة:
- 2As + 3/2O2 → As2O3
- يحضر أكسيد الزرنيخ الثلاثي صناعياً من تحميص معدن الزرنيخ الذي يوجد غالباً على شكل كبريتيد مع فلز الحديد حسب المعادلة:
- 2FeAsS + 5O2 → Fe2O3 + As2O3 + 2SO2
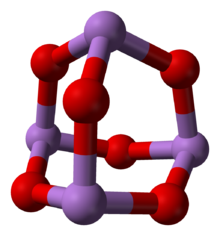
البنية
(cubic) |
(monoclinic) |
(monoclinic) |
الاستخدامات
- يعد أكسيد الزرنيخ الثلاثي مصدراً لإنتاج جميع مركبات الزرنيخ الأخرى.
الاستخدامات الطبية
التواجد الطبيعي
السمية
المصادر
Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4
الهامش
- ^ Shakhashiri BZ, "Chemical of the Week: Arsenic", University of Wisconsin-Madison Chemistry Dept.
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Sabina C. Grund, Kunibert Hanusch, Hans Uwe Wolf "Arsenic and Arsenic Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, VCH-Wiley, 2008, Weinheim.
وصلات خارجية
- Case Studies in Environmental Medicine: Arsenic Toxicity
- IARC Monograph – Arsenic and Arsenic Compounds
- International Chemical Safety Card 0378
- NIOSH Pocket Guide to Chemical Hazards
- NTP Report on Carcinogens – Inorganic Arsenic Compounds
- Use of Arsenic Trioxide in Multiple Myeloma Treatment
- The use of Arsenic trioxide in medicine.
- قالب:Inrs
- Institute of Chemistry Austria, speciallised on arsenic and various arsenic compounds
