أكسيد الباريوم
أكسيد الباريوم هو مركب كيميائي له الصيغة BaO ، ويكون على شكل بلورات بيضاء مسامية لكنها كثيفة.
| |
| الأسماء | |
|---|---|
| أسماء أخرى
Barium monoxide
Barium protoxide Calcined baryta | |
| Identifiers | |
| رقم CAS | |
| ECHA InfoCard | 100.013.753 |
| رقم RTECS |
|
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | BaO |
| كتلة مولية | 153.33 g/mol |
| المظهر | white solid |
| الكثافة | 5.72 g/cm3, solid |
| نقطة الانصهار | |
| نقطة الغليان | |
| قابلية الذوبان في الماء | 3.48 g/100 mL (20 °C) 90.8 g/100 mL (100 °C) |
| قابلية الذوبان | soluble in ethanol, dilute mineral acids and alkalies; insoluble in acetone and liquid ammonia |
| البنية | |
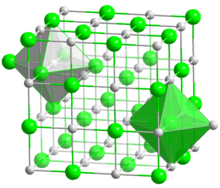
| البنية البلورية | cubic, cF8 |
| الزمرة الفراغية | Fm3m, No. 225 |
| هندسة إحداثية |
Octahedral |
| المخاطر | |
تبويب الاتحاد الاوروپي (DSD)
|
Harmful (Xn) |
| توصيف المخاطر | R20/22 |
| تحذيرات وقائية | (S2), S28 |
| NFPA 704 (معيـَّن النار) | |
| نقطة الوميض | non-flammable |
| مركبات ذا علاقة | |
أنيونات أخرى
|
هيدروكسيد الباريوم فوق أكسيد الباريوم |
كاتيونات أخرى
|
أكسيد الكالسيوم أكسيد السترونتيوم |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص
- يتفاعل مع الماء (حلمهة) بشكل عنيف مشكلاً هيدروكسيد الباريوم .
- ينحل مركب أكسيد الباريوم في كل من الميثانول والإيثانول بشكل جيد وناشر للحرارة.
التحضير
يحضر مركب أكسيد الباريوم من التفكك الحراري لـكربونات الباريوم . عملية التحضير هذه تجري صناعياً وبدرجات حرارة عالية (1450°س) ، ولتخفيض درجات الحرارة اللازمة للتفكك تتم إضافة مسحوق هباب الفحم إلى جملة التفاعل ، مما يساعد في عملية تفكك الكربونات وذلك بسبب سحب الغاز الناتج من التفاعل وهو هنا ثنائي أكسيد الكربون ، فينزاح ثابت توازن التفاعل نحو الاتجاه المباشر. بإضافة الكربون يتفاعل غاز ثنائي أكسيد الكربون معه مشكلاً غاز أحادي أكسيد الكربون، بالتالي يكفي الوصول إلى 1100°س لحدوث عملية التفكك والحصول على الناتج.
- BaCO3 → BaO + CO2
- CO2 + C → 2CO
أكسيد الباريوم المنتج تقنياً بهذه الطريقة يحوي على آثار من هباب الفحم.
الاستخدامات
- استخدم مركب أكسيد الباريوم سابقاً في تحضير فوق أكسيد الباريوم ، الذي يستخدم لتحضير الماء الأكسجيني.
- يستخدم في تحضير هيدروكسيد الباريوم.
- يعد مركب أكسيد الباريوم من المجففات القاعدية الجيدة.
السلامة
مركب أكسيد الباريوم سام.
المصادر
Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4
